化学原料药含量测定方法首选容量分析法-原料药含量测定首选容量分析的最主要原因
物理检查(外观性状)化学检查(定性定量)物化检查(仪器分析)原料药主要在纯度;制剂主要在含量测定,重量(或容量差异),以及相关药剂学检查(片剂溶出、生物利用率等;注射剂澄明度、热源等)。稳定性试验(预测有效期)。一切遵药典和有关药品质量标准进行。并对包装进行检查。
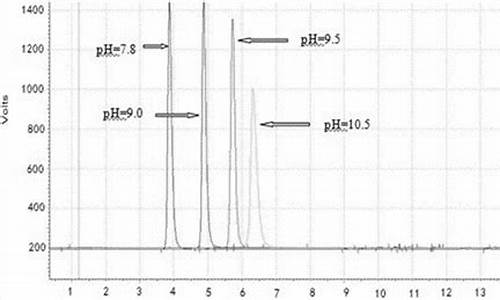
在做一原料药含量电位滴定测定时,本来应该是一个等当点,但有的出现2个-3个等当点,反应原理是酸碱中和
这是非水滴定,酸碱中和反应,方程式就是咖啡因加高氯酸=咖啡因高氯酸盐,加入冰醋酸是为了防止氢离子水和,降低高氯酸酸性,加醋酐有两个目的1是可以消除系统中微量水分,2是使原料药中伯胺和仲胺杂质乙酰化,使之失去碱性,单独滴定咖啡因,利用高氯酸非水滴定可以滴定产物中的伯胺、仲胺、叔胺。
原料药生产所用原料是否也必须每批留样?其留样时间如何确定?
你好,尊敬的用户,
1、确定设置电位滴定方法中的终止条件是一个等当点;
2、等当点理解错误(只有当终点的一阶导数大于方法中设置的阈值时,才是我们所要的等当点) ——这其中有可能是在滴定时出现了几个杂峰,而把杂峰误认为等当点。
3、如是第二条,请修改电位滴定方法中评估和识别的参数——设定一些限制条件,从而得到你想要的结果。
如仍有疑问,欢迎向企业知道提问。
262氯靛酚测定抗坏血酸与液相色谱法测定的主要区别是什么
例如,片剂在压片后进行内包装,压片结束后检测鉴别、含量均匀度等理化项目,而内包装之后仅取样检测微生物限度,最后成品放行的检验报告数据采用压片之后的理化项目数据和内包装之后的微生物限度数据,这样做是否可行? 答:放行,系指对一批物料或产品进行质量评价,作出批准使用或投放市场或其他决定的操作。一般情况下,如果企业对成品进行质量评价,能够确认中间产品的关键质量属性到成品时未发生变化,中间产品的检验结果能够代表成品放行前的检验结果,则可以引用中间产品的检验数据和结果。 企业如果采用这种方式,则必须对中间产品的关键质量属性到成品状态时的变化情形进行科学研究或评价,确保中间产品的检验数据能够代表最终包装完成的成品。应当注意,并非所有中间体的关键质量属性到最终放行时都不会产生变化。 2.问: 答:《药品生产质量管理规范(2010年修订)》明确要求制剂生产用每批原辅料和与药品直接接触的包装材料均应当有留样,并对留样作出了详细要求,而对于原料药则没有详细规定,但在第十二条(七)中明确规定:物料和最终包装的成品应当有足够的留样,以备必要的检查或检验。 原辅料留样的目的是为了能够有追溯性,一旦上市或未上市产品出现问题,企业能够从物料角度查找分析可能产生的原因。因此,企业还是应当根据其对成品质量影响的情形进行分析,从而决定是否留样、如何留样并形成操作规程。一般而言,原料药生产所用的起始物料、对原料药质量有直接或关键影响的那些关键物料均应当留样。 3.问:我们生产最终灭菌的大容量注射剂,从配制到灭菌的时限,工艺规程描述为不超过12小时,但实际工作中最多也超不过8小时,那么,12小时的时限是否必须要通过验证?8小时的时限也是否必须要通过验证? 答:《药品生产质量管理规范(2010年修订)》第五十七条规定:应当尽可能缩短药液从开始配制到灭菌(或除菌过滤)的间隔时间。应当根据产品的特性及贮存条件建立相应的间隔时间控制标准。 灭菌工艺的有效性不仅与灭菌参数有关,还与待灭菌物品的微生物负荷量有关。建立间隔时间控制标准的目的是为了控制待灭菌产品的微生物负荷量,使灭菌工艺能够达到相应的效果。 药液的微生物负荷量会随着时间的延长而增加。企业根据灭菌工艺能力确定可接受的最大微生物负荷量之后,应根据产品特性和贮存条件考察、建立并控制药液从配制至灭菌的时间,以控制微生物负荷量在可接受的最大范围之内。 问题中工艺规程规定的时限应当是经过验证的。如果最长的12小时时限已经过验证,根据实际工作情况,在其他条件不变的情形下,将时限缩短至8小时可不再验证。 4.问:检验人员须经过与所从事的检验操作相关的实践培训且通过考核。是不是药企的QC只要经过公司内部的岗位培训并考核合格就能上岗,不再需要经过药检或药品监管部门认可的机构培训后发证上岗? 答:《药品生产质量管理规范(2010年修订)》对检验人员提出了要求:质量控制实验室的检验人员至少应当具有相关专业中专或高中以上学历,并经过与所从事的检验操作相关的实践培训且通过考核。 该规范没有强制规定企业的检验人员需经过药检或药监部门认可的机构培训后发证上岗,其注重的是培训的有效性,企业应确保培训后检验人员检验的准确性。企业可采取理论培训、实践培训、或者师傅带徒弟等多种方式,也可以采取委托第三方机构进行培训的方式对检验人员进行培训,但必须注意,培训和考核仅仅是确保检验结果准确性的手段。
药物分析笔记:胺类药物的分析
分析方法不同。
1、262氯靛酚测维C,采用的是滴定法,属于容量分析,此法要求维C样含量高,比如维C原料药。容易法操作简单、成本低、重复性好、需配标液。
2、液相色谱法测维C,与上面方法相比,属于两类不同分析方法,色谱法优势在于分离,所以液相色谱法更适合维C混合物,比如维生素片剂,蔬菜、水果中维C含量、饮料、食品等中维C含量。色谱法操作复杂、仪器设备昂贵,色谱法常用外标法定量,需对照品。
芳胺类药物的分析
1、 基本结构与化学性质:
(一)盐酸普鲁卡因:
1、 芳伯氨基特征:重氮化偶合反应
2、 酯键易水解:光、热、碱,
3、 产物为对氨基苯甲酸(paba)。
4、 游离碱难溶水且碱性弱:非水滴定法,
5、 亚硝酸钠法测定含量。
(二)对乙酰氨基酚:
1、水解产物呈芳伯氨基特性:酸性中易水解
2、水解产物易酯化:水解后产生醋酸
3、与三氯化铁呈色: 紫外、红外、均可
2、 鉴别试验:
1、 重氮化偶合反应:盐酸普鲁卡因、对乙酰氨基酚(水解成对氨基酚)
2、 三氯化铁反应:对乙酰氨基酚水液加三氯化铁显蓝紫色。
3、 水解产物的反应:
4、红外吸收光谱
3、 对乙酰氨基酚的杂质检查:
1、 乙醇溶液的澄清度与颜色:检查中间体对氨基酚的有色氧化产物。
2、 有关物质:药典用薄层色谱法检查对氯乙酰苯胺。
3、 对氨基酚:中间体或水解产物,
4、 毒性大。有芳胺反应,而
5、 对乙酰氨基酚没有。
4、 盐酸普鲁卡因注射液中对氨基苯甲酸的检查:药典规定检查水解产物对氨基苯甲酸小于1.2%。5、 含量测定:
(一)、亚硝酸钠滴定法:有芳伯氨基的药物(普)以及水解后有芳伯氨基的药物(对)均可测定。
测定条件:
1、加入溴化钾(2g):加速反应。
2、加入强酸加速反应:反应加快、重氮盐酸性中稳定、防偶氮氨基化合物生成。
3、室温10---30 c 温度太高,亚硝酸逸出
4、滴定管尖端插入液面下滴定:避免滴定过程中亚硝酸挥发和分解。
(二)、紫外分分光度法:对乙酰氨基酚
苯乙胺类药物的分析
1、 基本结构与典型药物:肾上腺素
2、 鉴别试验:
1、 三氯化铁反应 :
2、氧化反应:盐酸异丙肾上腺素偏酸性下与碘迅速氧化。
3、甲醛--硫酸反应 :
4、紫外特征吸收与红外吸收谱:
3、 酮体检查:四种都需检查酮体,
4、 酮体在310nm处有最大吸收,
5、 小于0.06% 。
6、 含量测定:
(一)非水溶液滴定法:冰醋酸为溶剂,醋酸汞消除氢卤酸干扰,结晶紫指示终点。三种
(6) 溴量法:盐酸去氧肾上腺素及注射液用此法。
要点:防游离溴及碘逸出,溴过量2%,空白试验。
氨基醚衍生物药物的分析
1、 基本结构与性质:遇光分解盐酸苯海拉明:
2、 鉴别试验:
1、 与硫酸反应显色:二苯甲氧基反应
2、水解反应:遇酸水解生成二苯基甲醇
3、与硝酸银反应形成沉淀 :
4、紫外红外吸收光谱
三、含量测定:
1、非水溶液滴定法:~原料药为盐酸盐,冰醋酸中加醋酸汞后与高氯酸生成苯海拉明高氯酸盐 ,不能用于片剂测定,受硬酯酸镁干扰。
2、 酸性染料比色法:为分光光度法,
3、 灵敏度高。片剂含量测定及片剂溶出度的测定。实验关键要有合适ph,提取是否完全,要求高。
4、 阴离子表面活性剂滴定法:容量分析法,
5、 准确度高,
6、 用于注射液的含量测定。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。