原料药生产批件是什么-原料药生产批件
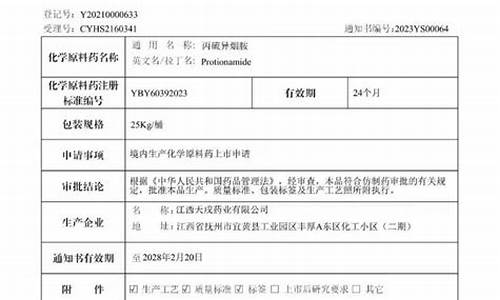
原料药拿到批件后,每个品种都必须申请GMP认证。而制剂只需认证1次就行了。 不同的是,原料药一般省局认证就可以,下批件的品种每个都必须申请认证。原料药的GMP证书是按照品种写的,制剂是按照剂型写的,具体的可以查询药智网,回答满意请您采纳,谢谢。
进口中药材,中药饮片、原料药应具有哪些证书和批件?
这个说起来就有点多了。下面大概说下国产品种。
每一个药品都需要获得药监局核发的生产批文才能够生产并上市销售。这里说的生产批文包括了LZ上面说的“药品注册证、药品注册批件、药品再注册批件”等等,某个品种第一次注册的时候核发的是药品注册批件,以前还会有配套的药品注册证(现在没有这个东西了),那么只要这个“药品注册批件”在有效期内,该品种都是可以生产的。注册批件有效期只有5年,当注册批件过期了就需要再注册,一般是提前半年申请再注册,药监局受理该申请后会发一个受理通知书(这个受理通知书是没有实际意义的,仅仅表示受理该申请,至于能不能通过还需要审核),审核通过才会核发药品再注册批件,有了这个再注册批件,该品种的就又有了5年的有效期。以此类推,每隔五年都需要重新注册。药品补充申请批件是指对该品种的一些补充申请核发的批件,这里说的补充申请的内容就很多了,生产厂家更名,药品变更有效期,生产地址变更,增加规格等等,都属于补充申请的范围,需要具体问题具体分析了。综上所述,只要具备了在有效期内的生产批文,该品种就能生产。如果之前的注册批件过期了,新的再注册批件还没有下来,仅有申请再注册的受理通知书,这期间是不能生产的。
哪些药品可以生产?
进口原料药、中药材、中药饮片应具有《进口药品注册证》(或《医药产品注册证》)或《进口药品批件》,应符合药品进口手续,应有口岸药品检验所的药品检验报告。进口药品注册证》或《医药产品注册证》、《进口药品检验报告书》或《进口药品通关单》和首次进口的《进口药品检验报告单》。
2.进口药材:《进口药材批件》。
3.《注册证》、《批件》的有效期、生产国、进口包装的标签上应注明药品的名称、注册证号,并有中文标识。
4.复印件应有供货单位质量管理机构的原印章。
5.所规定的范围内,需批批进口检验的,应按规定索要批《进口药品检验报告
6.相关的管理文件。
重庆康刻尔制药有限公司的基本信息
丰原药业:公司是全国第二大扑热息痛原料药生产商(第一鲁安药业未上市,产能4万吨),旗下利康药业扑热息痛产能已达2万吨。
诚意药业:止咳药退烧药最佳补涨,退烧原料药(扑热息痛)。
亚宝药业:退烧药+止咳化痰+降血压+新冠特效药+抗癌一类新药上20元。
亨迪药业:公司布洛芬原料药为解热镇痛类,相关制剂产品可用于有发烧症状的新冠患者的退烧治疗。布洛芬原料药全国产能第二,45%出口,21年作为湖北省抗疫重点药品产业链生产企业。
贵州百灵:家中常备的非处方退烧药,咳嗽药。
尔康制药:公司主营对乙酰胺基酚(原料药)。
汉商集团:对乙酰胺基酚通过一致性评价。
西点药业:复方氨酚烷胺胶囊包含对乙酰胺基酚,适用于感冒发烧。
润都股份:主营布洛芬缓释胶囊。
粤万年青:对乙酰胺基酚片获得注册批件。
东北制药:对乙酰胺基酚通过一致性评价。
新华制药:布洛芬原料药全球产能第一。
筹建原料药生产企业
公司现有产品剂型为片剂和胶囊剂,其中片剂生产能力可达10亿片,胶囊生产能力可达5亿粒。现在康刻尔公司有制剂产品注册批件21个,原料药生产注册批件3个,形成降血糖类、降压类、降血脂类、呼吸系统类、抗生素类、抗过敏类、肝胆用药类等多个系列产品群。公司生产的格列美脲片(力贻萍片),国家二类新药,保护期8年是国家五部委评定的国家级重点新产品。该产品现已行销国内除台湾省以外的各省市,其销售额在全国同类产品中名列前茅。我司研制开发的康尔贝宁和伉尔舒宁口腔崩解片,其特点是入口即化,无需服水,快速高效,口感清甜。重庆康刻尔是国内第一个获得该系列生产注册批件的制药公司,在2004年度权威部门评选出的全国500个新产品中列122位,其中在新药中名列第10。
化工厂能否生产原料药
可以按照下面的步骤办理,仅供参考:
第一步:先到省级药监部门办理备案。
第二步:按照省级药监部门的批示,进行企业的筹建。
第三步:筹建完毕后,申请省级药监部门到企业审核;审核通过后,发给企业《药品生产许可证》。
第四步:企业凭生产许可证办理工商注册,至此企业就是一个制药厂了。
第五步:企业进行药品注册。取得生产批件后,进行GMP认证。
药品招标生产厂商需提供哪些资质材料
如果你想将化工产品当成原料药卖,那么必须按照国家对药品的要求进行研究和申报,并且工厂要通过GMP,获批后才是原料药,才能按照原料药销售。如果化工厂生产的化工产品没有国家批准的原料药批件,那么只能作为化工产品销售,尽管这种化工产品与原料药结构相同和质量相同。
两种资质,一种是企业资质,一种是产品资质
详细如下
企业资质①
企业法人营业执照②
药品生产许可证③
组织机构代码证④
商标注册证⑤
税务登记证(地税)⑥
税务登记证(国税)⑦
增值税纳税申报表⑧
药品GMP证书
产品资质①
药品注册批件(原料药)
②
省级药品检验报告(原料药
最近三批次) ③
新药证书 ④
药品注册批件(制剂)⑤
国家药品标准⑥
省级药品检验报告(制剂
最近三批次)⑦
产品说明书原件⑧
药品生产工艺流程图(包装设计稿)⑨
原料来源证明(公司没有原料药批件之品种)
物价文件册①
生产企业所在地省级物价 ②
企业自主定价文件 ③
招标所在地物价备案文件
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。