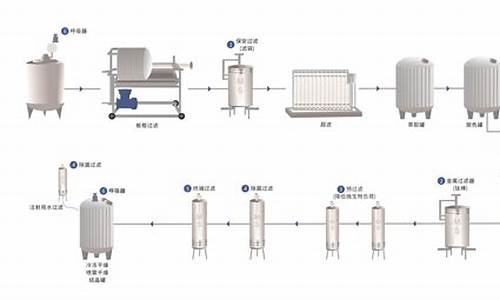
原料药的工艺流程-原料药的工艺流程是什么
中成药每个厂家之间的价格都会有波动,究其原因,主要有:
1.成本不同。同样的药品,包装好的就是比包装差点的要贵,广告投入多的肯定比少的要贵,这里的成本高啊,不贵点怎么收回成本后盈利呢,药厂也得有利润才能发展下去啊。
2.成分不同。同一个名字的药,使用的中药原料药不一样,价格就不一样,一个是正宗的道地药材,一个是非道地药材,有效成分含量上肯定存在差异,价格当然是道地的贵了
3.制药工艺流程有别。两家药厂,一家使用现代化的机器生产,运用高新仪器设备,另一家还是传统的人工操作,增加了药品污染的机率,制得的成药肯定是前者贵些了。
4.地域性差异。同一厂家产的同一中成药,在上海卖的价格和在新疆边境地区卖的价格也会有价格差阿,因为得考虑当地的购买能力啊。
所以,中成药各个厂家的药品价格相差很多,十几元不足为奇,有的差价都是几倍甚至十几倍。主要影响因素就这些吧,能想到的
另外,北京同仁堂专卖道地的真药,药材好,自然价格贵喽。
gmp认证怎么申报
化学制药工业的特点如下:
高度的科学性、技术性
生产分工细致、质量要求严格
生产技术复杂、品种多、剂型多
生产的比例性、连续性
高投入、高产出、高效益
化学制药工业的有哪些特点?
原料药品种众多,其生产方法各不相同,有全合成法,有发酵法兼用提炼技术,有合成法兼用生物技化学制药学生参观术,有发酵产品再进行化学加工,也有主要采用分离提纯方法。
原料药生产的一般特点是:
①生产流程长、工艺复杂。
②每一产品所需的原辅材料种类多,许多原料和生产过程中的中间体是易燃、易爆、有毒或腐蚀性很强的物质,对防火、防爆、劳动保护以及工艺和设备等方面有严格的要求。
③产品质量标准高(纯度高、杂质可允许的含量极微),对原料和中间体要严格控制其质量。
④物料净收率很低,往往几吨至上百吨的原料才生产一吨产品,因而副产品多,三废也多。
⑤药物品种多、更新快、新药开发工作的要求高、难度大、代价高、周期长。制剂生产则需要有适合条件的人员、厂房、设备、检验仪器和良好的卫生环境以及各种必需的制剂辅料和适用的内、外包装材料相配合。
求:蛋白质生产工艺流程相关知识介绍。
一、申报企业到省局受理大厅提交认证申请和申报材料
相关材料:
1 药品GMP认证申请书(一式四份)
填写细节要求:
a、企业名称、注册地址、生产地址应与《药品生产许可证》一致;
b、企业法人、企业负责人应与《药品生产许可证》一致;
注意:企业填报的联系人应熟悉企业生产、质量管理情况,****应有效、快捷。
c、企业申请认证范围应在《药品生产许可证》生产许可范围;
d、企业申请认证剂型应与该品种的注册批件剂型一致;
e、中药丸剂申请认证时应展开,如:丸剂(蜜丸、水蜜丸、水丸、浓缩丸、微丸、糊丸、蜡丸) ;
注意:相近剂型的确认-----喷雾剂和气雾剂、合剂和口服液、口服液和口服溶液剂等等
f、认证品种中有青霉素类、头孢菌素类、激素类、抗肿瘤药、避孕药、放射品应注明;
g、原料药认证应注明原料药名称;
h、既有口服也有外用的制剂,外用的应在制剂后注明外用。
i、医用氧企业认证申请范围应注明气态、液态;
j、中药饮片企业认证申请范围应明确饮片的炮制方法,如:中药饮片〔净制,切制,炮炙(炒、烫、煅、制炭、蒸、煮、炖、燀、酒制、醋制、盐制、姜汁炙、蜜炙、油炙、水飞、煨),粉碎(不包括直接口服饮片),包括毒性饮片的净制、切制、炒制与蒸煮制〕;
k、企业申请认证范围有中药前处理及提取车间的应予以注明;
m、企业申请认证范围有动物脏器、组织的洗涤、提取车间的应予以注明。
注意:企业中药前处理及提取委托生产的应在安监处办理相关委托手续。
2 GMP认证之《药品生产企业许可证》和《营业执照》复印件
复印件细节要求:a.证照应在有效期内b.《药品生产许可证》生产范围应涵盖认证申请范围,否则不予受理c.属新增生产线、生产地址、生产范围的,应在《药品生产许可证》变更完成后申请认证注意: 企业首次认证或新增生产线、生产范围的,认证时须报送该范围三批试生产记录复 印件。
3 GMP认证之药品生产管理和质量管理自查情况
细节要求:
a.企业概况和历史沿革情况应包含以下内容:
企业原名或前身,改为现公司的时间,企业占地面积,建筑面积、绿化面积,绿化率等;通过GMP认证的情况;本次申请认证车间的竣工时间,面积,净化级别及面积,年设计生产能力,车间生产品种的情况等。
b.企业GMP实施情况应包含以下内容:
前次认证缺陷项目的改正情况,到期认证的应提供原认证GMP证书复印件及缺陷项目的整改情况;
人员培训情况;
企业负责人、生产、质量管理人员及其他技术人员情况;
本次认证品种相对应的车间及生产线情况;
原料药应分别写明合成及精制车间情况;
如有原料药多品种共用生产线情况,应详细说明;
本次认证各剂型生产线车间分布情况;
本次认证品种车间洁净级别;
仓储情况并注明阴凉库情况和危险品库情况;
化验室情况;
公用设施,水、电、汽供应情况;
工艺用水制备情况;
空气净化系统情况;
物料管理情况;
卫生管理情况;
生产管理情况;
质量管理情况;
安全消防情况;
三废处理情况。
4GMP认证之药品生产企业组织机构图
细节要求:a.应有合理的组织机构图,并注明各部门名称、相互关系、部门负责人;b.企业质量管理部门应由企业负责人直接领导c.质量管理部门负责人与生产部门负责人不能兼任
5 药品生产企业负责人、部门负责人简历;依法经过资格认定的药学及相关专业技术人员、工程技术人员、技术工人登记表,并标明所在部门及岗位;高、中、初级技术人员占全体员工的比例情况表。
5 GMP认证之相关人员5.1 药品生产企业负责人、部门负责人简历注:企业负责人、部门负责人简历应包括受教育情况、每一时段工作情况,特别是从事药品生产、经营情况。 新条款要求主管生产和质量的企业负责人、部门负责人都应具医药或相关专业大专以上学历; 中药制剂企业主管生产和质量的企业负责人、部门负责人应具有中药专业知识。5.2 依法经过资格认定的药学及相关专业技术人员、工程技术人员、技术工人登记表,并标明所在部门及岗位表格要求:姓名,学历,毕业学校,专业,职称,职务,从药年限等5.3 高、中、初级技术人员占全体员工的比例情况表
6 GMP认证之药品生产企业生产范围剂型和品种表
6.1 药品生产企业生产范围全部剂型和品种表;
有青霉素类,头孢菌素类,性激素类避孕药,激素类,抗肿瘤类品种的应予注明
表格要求:表中应包含通用名,规格,剂型,批准文号等字段
6.2 申请认证范围剂型和品种表(注明常年生产品种);
有青霉素类,头孢菌素类,性激素类避孕药,激素类,抗肿瘤类品种的应予注明
表格要求:表中应包含通用名,规格,剂型,执行标准,批准文号等字段,并注明常年生产品种
6.3 生产批件(或新药证书)等有关文件资料的复印件;
6.4 常年生产品种的质量标准;
[注:中药饮片生产企业需提供加工炮制的全部中药饮片品种表;申请认证炮制加工范围和炮制加工品种表(注明常年生产品种),包括依据标准及质量标准等;]
7 GMP认证之药品生产企业周围环境图、总平面布置图、仓储平面布置图、质量检验场所平面布置图(含动物室)
7 药品生产企业周围环境图、总平面布置图、仓储平面布置图、质量检验场所平面布置图(含动物室)
详细要求:
周围环境图、总平面布置图要求:
a.药品生产企业周围环境图应注明企业周围道路、 相邻建筑物、 相邻单位的名称。
b.药品生产企业总平面布置图应注明所有车间位置、名称或车间编号,并注明申请认证车间位置、名称或车间编号,常年风向。
仓储平面布置图要求:
注明注明企业仓储位置,注明危险品库位置;
需注明合格品库、不合格品库、阴凉库、危险品库等位置;
应注明原料库、成品库、包材库、标签库及特殊管理药品库位置;
中药制剂企业应注明中药材库、净药材库位置。
质量检验场所平面布置图要求:
注明质检场所位置;
质量检验场所平面图需注明理化室、仪器室、留样室等各功能间位置;
微生物限度测定室、阳性菌室、无菌室、生物效价检测室应注明位置及洁净级别。
8 GMP认证之药品生产车间概况及工艺布局平面图
8 药品生产车间概况及工艺布局平面图
应包括所在建筑物每层用途和车间的平面布局、建筑面积、洁净区、空气净化系统等情况。其中对β-内酰胺类、避孕药、激素类、抗肿瘤类、放射品等的生产区域、空气净化系统及设备情况进行重点描述;
·
8.1 生产车间工艺布局平面图
应注明生产车间各功能间名称;
中药前处理车间、中药提取车间、动物脏器,组织洗涤车间,也应有工艺布局平面图;
应注明各功能间空气洁净度等级;
应标明人流物流流向
·
8.2 生产车间工艺设备平面图
应注明生产车间各功能间使用设备名称;
中药提取车间使用设备较大、占用多层空间时应标明每层设备;
部分设备辅机与主机不再同一洁净级别的应注明。
原料药应有合成工序、精制工序设备平面图;
企业的工艺设备应与所生产品种工艺相匹配;
激素类、抗肿瘤类药物使用的独立设备应标明。
·
8.3 空气净化系统的送风、回风、排风平面布置图
洁净车间风管平面图中送风口、回风口和排风口的应明确标识;
送风管、回风管、排风管应该清晰明确
常见问题:
企业质量检验场所洁净区送风、回风、排风平面布置图是最易漏报项。
空气净化系统送风图不清晰
空气净化系统送风图送风不够
空气净化系统送风图管道不全
空气净化系统送风管道图未按要求
空气净化系统回排风图不清晰
洁净区、普区间无缓冲
洁净区与厕所共用回风
9 GMP认证之申请认证型或品种的工艺流程图,并注明主要过程控制点及控制项目
本次申请认证剂型、品种工艺流程图应齐全;
应有工艺控制点及控制项目;
中药制剂工艺含前处理及提取的应有前处理提取工艺流程图;
生化制剂工艺含前处理的应有前处理工艺流程图;
原料药应包括全部批准生产工艺;
工艺流程图应注明工艺过程的洁净级别;
工艺流程应与质量标准一致 。
10 GMP认证之药品生产企业(车间)的关键工序、主要设备、制水系统及空气净化系统的验证情况;检验仪器、仪表、衡器校验情况
10 药品生产企业(车间)的关键工序、主要设备、制水系统及空气净化系统的验证情况和检验仪器、仪表、衡器校验情况
细节描述:
关键工序验证应能代表申请认证品种、剂型的整个生产过程。如:企业同时有中药制剂和化药制剂验证时应选中药制剂进行验证,应包括中药前处理及提取;
主要设备验证应包括设备验证情况应与工艺流程图和设备平面图上的内容相匹配;
共用设备应有清洗验证情况;
制水系统验证应包括整个使用点验证情况;
空气净化系统验证应包括每一个功能间;
本次申请认证剂型及原料药所有品种都应验证。
11 GMP认证之检验仪器、仪表、量具、衡器校验情况
相关细节:
企业应按照质量检验标准的要求配备成品的所有质量检验仪器;
需要委托检验的,应符合《国食药监安[2004]108号:关于药品GMP认证过程中有关具体事宜的通知》要求,并且受托方应有计量认证证书;
应有相关仪器、仪表、衡器的校验情况,包括校验日期、校验周期和校验单位等。
12 GMP认证之药品生产企业(车间)生产管理、质量管理文件目录
12 GMP认证之药品生产企业(车间)生产管理、质量管理文件目录
注意:有特殊要求的药品等的管理文件,
如毒麻物料管理相关文件
13 GMP认证之企业符合消防和环保要求的证明文件
gmp认证细节:
消防证明应是公安消防部门出具的相关证明或证书,其他任何证明无效;
环保证明应是环保监测部门出具的废水、废渣、废气的监测报告,环评部门出具的环评报告不予认可。
二、省局药品安全监管处对申报材料形式审查 (5个工作日)
三、认证中心对申报材料进行技术审查 (10个工作日)
四、认证中心制定现场检查方案(10个工作日)
五、省局审批方案 (10个工作日)
六、认证中心组织实施认证现场检查 (10个工作日)
七、认证中心对现场检查报告进行初审 (10个工作日)
八、省局对认证初审意见进行审批(10个工作日)
九、报国家局发布审查公告(10个工作日)
原料药投产安全先要办的手续有哪些
抗生素发酵工业在生物工程中占据重
要比重。由于它又是一个高能耗,大排放
量的产业,因此许多企业在随着发展大顿
位发酵罐组,建立多个发酵生产线,以适应
多品种和规模化的过程中,都将遇到土地、
能源、排污处理等方面的突出矛盾,上一个
新发酵车间,需要增加很多的动力配套,如
按照常规的单一功能块进行平面布局设
计,势必投人大笔资金扩改建空压站、供排
水等等辅助厂房及设施,放大或增加许多
远距离的输送管网,而这些工程的实施无
不受到多种条件的制约。其一,工程总投
资加大,施工涉及面广,工期拉长;其二,土
地、水资源、环境保护是国民经济可持续发
展的重要素,扩容量受限制。欲实施涉及
到方方面面棘手的社会问题不易解决。
寻找发酵工程综合功能模式设计的研
究变成了十分有意义而现实的课题,笔者
依据工艺总平衡设计与配套的辅助工程有
机结合,统筹总平方案,在有限的空地上建
造一座多功能、立体布局的发酵工程综合
厂房。该厂房集发酵、供配电、空压站、循
环水、集污处理分流排放等多个功能块边
叠一整体,使得在同等生产规模下,达到建
筑占地最少,节省能耗,排水排污量最小,
工艺管线最短,调控方便,投资较省之目
的。为今后建立“全能量”工程设计进行初
步尝试。
2多功能模式的理论依据
现以设计八个100砰发酵罐,三级发
酵工艺的四环类抗生素发酵车间技改项目
为例,经平衡计算,高峰期需要:
空气量:750耐/min(标准)
O
.
25MPa表压
冷却量:790万kcal(其中发酵410万
keal/h,
压缩空气380万keal/h)
排水量:约2000t小(指使用江水冷却
时)
2
.
1关键设备的选型与设计对策
(1)本项目拟选用国内外先进可靠的
空气透平机420耐/min的二台和200时/
min的双螺杆压缩机一台(自动调压,1忍
调量),因为这二种机型无脉冲震动,基础
简单,对发酵厂房及设备不会产生破坏性
影响,所以空压站可与主车间连体。
三台机组不同组合,能提供每分钟
100至1040立方米的多个分档供气量,以
适应发酵生产的不同需要。该系统因工艺
条件要求,选择排气压力较高的空压机,若
空气有余量,可提供给临近用气单位,或降
压与旧空气系统并网。
(2)由于新扩建车间不在旧厂区,远离
江边水源,更无大排水量设施,因此供排水
问题欲加突出。南方气候炎热,本地区夏
季水温高在达30一30℃,持续时间很长,
此时期江水和自来水均不可用于发酵罐冷
却,应改用冷冻水。到了冬天,自来水温度
只有10一巧℃,故可选用温差5一4℃,补
·
25·
药工程设计1999年第2期
充水量只有1%的喷射式低温冷却塔(新
型设计)二台,每台循环量为1000m3八,即,
二台总冷量大于8000万kcal小,能满足冷
天发酵车间和空压站空气后冷器的总需冷
量;热天循环水出水温度28一29℃,只能
用于发酵物料消后冷却,压缩空气一级冷
却及氨机冷凝器冷却。
在选择循环水冷却塔系统时,不就忽
视水质处理技术,只有辅以先进的水处理
技术,支持在线监控,才能保证优质的循
环水不被污染。循环水取代江水之后,各
系统冷却器管内长期不积垢,稳定了传热
系数。
循环水取代江水,实现了发酵工程闭
路循环冷却(见图1),减少了生产排水量
95%以上,解决了排放系统的难题。从工
程需冷量平衡计算已知,高峰期发酵系统
410万keal/h,压缩空气系统380万keal/h
(其中一级冷却200万kcal八,二级冷却
115万kcal小,其余为油冷及压缩机冷
量)。水的调配方案是,冬天(冷天)全部采
用巧℃以下的循环水冷却;夏天(热天)除
了发酵罐物料消后冷却降温和压缩空气一
级冷却用循环水外,其它的均采用由氨机
制冷站提供的零上低温水,此时正好将有
大量富余的循环水提供给氨机氨冷凝器冷
却之用。如图1所示,该闭路系统全部由
阀门切换控制。但必须说明的是,由于发
酵车间随罐批数的以及生周期的不同,用
水量变动大,同时冷热季节过渡期间动力
用水量变化也大,最终直接影响了循环水
的供应量频繁波动。设计中将热水泵电机
附加变频调速器,并以冷水池的水位控制
信号平滑地调节热水泵电机转速,达到平
稳运行,平衡供水,据实测,该措施比起用
手动阀门截流调节,单机节电在50%以
上。
注:
_材坏水心级___冷冻水心级
lll冷功功p堪堪
火火火只只只只只只只只只只只只只只只只又又又又又又又又又又卜一——一一一(池池池纸机冷提忍忍忍忍忍玲玲戈戈戈戈}}}}}}}一一一一一一一一一
}}}}}}}}}}}}}}}}}}}}}}}}}
}}}
卜.
…………………一一一.,奋找J一一
卜卜...
一一
’
(((((((((((((\\\\\\\\\\\\\\\\\卫卫lllllllllllllllll}}}}}}}}}热热热热热热热热热热热热热热热热热热热热一一水水水水囚囚囚.囚...........池池池池池池池池池池池池池池池池池池口口口
图l
(3)确保发酵空气的无菌是发酵工程
设计至关重在的任务,笔者特此全面选用
精度等级0.01um的高分子膜过滤器,革
除庞大的总过滤器,取消车间内复杂的无
·
26。
菌气公共管网,设计发酵单体罐空气净化
系统(见图2)。该设计的实施可减少空气
阴力降O.03MPa;节省多个总过滤器及其
公共管道的占用平面。
医药工程设计1999年第2期
...
}岁\\\\\
(一,二级)
图2
2
.
2总平设计的原则
综合功能厂房根据各厂允许建设的空
地面积和地形,可以设计成长短形,“门”
或“L’’状。本项目为“L’,形,如图3所示,
其具体布置分述如下:
(l)空压站:靠东面,位于本地区主风
向头,远离锅炉和运输干道,环境干净,空
压机安装在二楼,辅机在底层。
(2)空压机吸气口:利用螺旋梯空心中
佳柱及厂房内墙角建3个20米高的吸气
通道(超过10米高的设计标准),吸口尽量
远离发酵高空排气(汽)管,本图相距25
米。依附于构筑物的吸气风道十分牢固,
并且可以建得很高,测试表明空气细菌浓
度比地面下降2乃,为发酵空气净化创造
了极有利条件。
(3)空压站毗连发酵主车间,压缩空气
经冷却、加热直接接人车间空气总管,路程
大幅度缩短。这不仅减少管道阻力,更重
要的是使压缩空气不因四季间或昼夜间环
境气温的急剧变化的影响,稳定了空气的
湿度的调控。
(4)循环水:在西面高楼顶建造大型凉
水塔和冷水池,它与空压机吸口距离务必
拉大,本图二者相距50米。热水池、泵房
及控制中必设在底层。
高层建塔,大气对流强烈,同时冷水池
的高位落差14米的重力能减少了冷水泵
的动力耗,可取得事半功倍的经济效益。
(5)集污分流:预防发酵染菌污染源扩
散,制止活菌体的肆意排放,尤其染噬菌体
的排放,也是发酵工程设计的中心内容之
一。这在过去常被设计者忽视的“GMP”
对原料药生产,尤其抗生素生产的环境污
染提出很高标准。对此我们采取的设计措
施正如图3所示,发酵罐的排气分离器各
自独立,一二级罐用补料罐各自集中排放,
让分离的废液和取样口排液注人南北集污
池,待消毒灭菌后汇流到污水处理站。这
种设计方案虽然分离系统多,管路敷设相
对复杂,但它却保证了各种发酵罐在消毒
排汽或发酵气时候十分畅通,不会因为由
于罐与罐之间,管路与管路之间差压所引
起的倒压和交叉污染,实践证明它比集中
总管总排气分离的设计优越。
3设计效果
依照以上构想方案和理论根据所设计
的大型发酵工程已连续运行四年,各类设
备运行平稳,各大工艺参数均达到设计水
平,水、电、气等调控灵活方便,所有冷却水
管都不积垢,环境、地沟干净,空气净化可
靠,发酵生产工艺稳定。
.
27·
药工程设计1999年第2期
该工程综合设计有效的解决了土地不
足,水源匾乏,排放困难、环境污染等技改
项目所面临的重大难题,使工程施工得以
顺利进行。
——~一一二尸尸
/////////////产产
{{{{{{{{{{{{{{{{{{{{{{{{(((((((((((((((((((((((((((((((((((((吸吸吸吸吸吸吸净困团。。〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔〔廿廿廿廿少少少少{{{不不不不班班班班班班班班班班·{{{{{{{{{{{{{{{{{lllllllllllllllllllll氏」二日‘‘门门门门门门门门In月月月「1尸尸
图3北向立面图
4遗留的课题空。
大部分耗气(氧)菌的发酵热高,发酵假设各排汽出口处为0.IMPa表压,
罐温多在28一32℃之间,要求冷却水温度计得热量为4900kcal八,平均204万kcal/
一般不低于15℃。南方高温季节很长,平h。若将热量集中回收,制备成85℃的热
均气温高,水温也高,一年间真正发酵生产水,提供给热水型澳化锉吸收式制冷机,热
能全程使用循环水的时间只有四个月,其力系数取0.4,则能产生10℃的冷水81.6
它时间则改用零上冷冻水冷却。此阶段循万kca!小,占发酵需冷量的20%,相当于
环水只供作物料消后冷却,压缩空气后冷节约一台44kcal小标准制冷量氨机进行
及氨冷之用。因该车间习惯于实罐消毒,零上工况调节的效果,所以节能效益十分
故消后冷却热常使循环水回水瞬间增加巨可观。
大的热负荷,若能改为连消式艺,则可避免纵然废热蒸汽回收制冷不足于解决发
热荷的波动幅度,全程使用循环水的时间酵车间的需冷量,但若使其10℃的冷水在
将延长。冷天与循环水并网,或在热天时候与冷冻
从全能量利用着想,本项目依据理论水站提供的6℃的冷冻水并网使用,其方
计算和实际运行记录,发酵消耗蒸汽高峰案是完全可行的,此乃实现发酵工程综合
约8t小,日平均耗汽量150吨。按照提供功能全能量设计之目的,其主要工艺流程
0
.
4MPa表压的蒸汽和现行实罐消毒工艺如图4所示,三种冷却水的并网操作主要
测算,每日真正用于物料直接加温来菌并是1阀常开(全年回收热制冷),2、3阀随
附加设备热散失,总共只耗掉55吨蒸汽,使用期不同交换开关,回水阀也相应开关。
这意味着尚有95吨的蒸汽是用在各种物废热蒸汽回收利用在技术上的最大困
料消毒的保温(恒温维持);各种物料管路难是要求回收量的均衡性,实际生产过程
的消毒;各管口汽封保护等方面。这部分发酵消毒排汽是随机性。如果一个车间有
蒸汽约80吨呈饱和状态从排汽管白白排足够发酵罐,24小时内有计划地安排消
·
28·
医药工程设计1999年第2期
}}}}}}}}}}}}}}}}}}}}}
其其它炭热落汽汽汽逻逻丛丛丛丛丛丛丛丛丛冷冷冷冷冷冷冷盛盛卜塔塔
只只只只只只只只只只只只只只只之之之之彩444必乏乏乏乏乏
}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}}
冷冷冷冷冷月月卜池池
}}}}}}}}}}}}}}}}}}}}}}}}
岁岁岁刽刽
。。。冷。站’
lll
图4
毒,则容易解决以上问题。但象本项目中
发酵罐大而数量不多,种子、补料罐用各种
管路的消毒次数相对较少而且集中,因此
首先应该解决高峰的低谷期余热回收调节
装置和庞大的蓄能(热水)贮罐。它的最终
目的是使澳化铿制冷机能够平稳运行,和
其它供冷水系统并网之后,能与发酵生产
工艺协调。这是本项设计的遣留课题,尚
待探索之中,其意义是不言而喻的。
药厂包装车间实习总结
原料药投产安全先要办的手续有:
1、安全生产许可证申请:申请单位需向当地安全生产监管部门提交申请材料,包括企业基本情况、生产工艺流程、安全管理制度等,经审核符合要求后颁发安全生产许可证。
2、环境影响评价:根据国家环境保护法规定,投产前需要进行环境影响评价,评估项目对环境的影响程度,制定环境保护措施。
3、安全评估:对生产过程中可能存在的安全风险进行评估,制定相应的安全管理措施,确保生产过程中的安全。
药品生产质量管理规范简介
药厂包装车间实习总结
刚入厂,首先让我们了解药厂厂区布局,车间布局,熟悉相关原则,给我们介绍各个车间生产的药品和车间***。然后就是各个部门管理人员给我们讲解车间工艺,安全,消防知识和企业文化,让我们熟悉了药品生产工艺流程,本文主要是关于总结,实习,车间,我们,知识,自己,社会,工作,学习,岗位, 的,希望大家尊重原创者的知识产权。
刚入厂,首先让我们了解药厂厂区布局,车间布局,熟悉相关原则,给我们介绍各个车间生产的药品和车间***。然后就是各个部门管理人员给我们讲解车间工艺,安全,消防知识和企业文化,让我们熟悉了药品生产工艺流程(从原料到成品),学习了各车间物料流程,加强了gmp知识和安全知识的学习,把理论与实践相结合。在我们培训了这些知识后久把我们分配到了各个车间开始车间实习。
我被分配到四车间,和我一起的还有2名应届毕业生。这个车间是2000年建的车间,我们刚到车间时,我们主任给我们说进入车间的注意事项,然后给我们介绍车间主要生产的药品。这个车间主要生产紫杉醇特素,vc;醋酐等原料药,...主任给我们分配岗位,我一开始被分配在胶塞铝盖清洗灭菌岗位,跟着陈新的师傅学习了很多关于胶塞机和铝盖机的工艺的知识与清洗操作。发现,就那样小小的一个胶塞铝盖需要那么多的工艺流程才可以灭菌成功。后来主任又从新岗位,我被分到包装。在包装虽然不像别的岗位那么需要工艺知识,但我在包装学习的很开心。我们每个新学员和包装的师傅们关系很融洽。就这样通过我们大家共同努力,我们完成了一次次的任务。我们每个新学员都由衷的开心。
转载请著名来自:( 计生工作总结 )
在为期几个月的实习里,就像和上班族一样上班,天天早上七点半起床,八点三十准时到车间换好工作服开始进入工作状态,实习过程中我遵守公司的各项制度,没发生过重大事故,虚心向有经验的师傅学习,认真的完成领导下达的工作任务,并把在学校里所学的专业知识运用到工作当中,下班休息之余扩充自己的专业知识和岗位安全知识,使自己在工作中更有竞争力。
时间过得很快,眼看我们六个月的实习期就要满了, 我觉得实习是对一个应届毕业生来说非常重要的经历,实习是我们离开学校接触社会的一个平台,最真实地感受社会的一个窗口。这次在海南海药有限公司为期六个月的实习生活让我学到了很多东西,对我而言有着十分重要的意义。它让我提高沟通及人际关系处理能力,提前体验上班族生活。在实习过程中,丰富了自己的专业知识,积累了工作经验,为以后走上工作岗位打基础,还找到自身的不足之处,早日弥补,增强了自己适应社会的能力。让我更深刻的了解社会,更便捷的融入社会,它不仅使我在理论上对制药技术这个领域有了全新的熟悉,而且在实践能力上也得到了提高,真正地做到了学以致用,让我学到了许多书本上学不到的东西,有效的锻炼了自己,长了见识,开拓了视野,实习是我们把学校学到的'理论知识应用在实际中的一次尝试,是我们迈向社会的第一步,通过这次实习,我发现了不少问题,自己的缺点、不足,早该摒弃陋习。让我知道自己所学的知识太肤浅,专业知识在实际运用中的匮乏。让我更加明白我需要学习的太多,使我了解到必须让自己懂得更多才能在当今竞争激烈的社会中拥有一席之地.
为认真贯彻学习党的十八大、省十一次党代会、十一届二、三次全会精神,全面推进省直机关工会工作,提高基层工会干部服务职工、维护职工的能力和水平,省直工会工委于20**年6月26日—28日在省水利厅松柏山生态保护基地举办了一期新任工会干部上岗培训班,省直各基层工会选派了188名工会干部参加了培训。总的来说,举办这次培训班,工作准备充分,培训内容丰富,理论联系实际,使工会干部增长了知识,开阔了视野,取得了明显的效果。
一、认真安排,精心准备。
根据年初的工作安排,为加强对省直机关工会干部培训,确保新任工会干部持证上岗,省直工会工委把新任工会干部培训工作,作为今年的一项重要工作来抓,专门召开会议对培训时间、培训地点、培训内容、聘请培训老师、安全保障等有关问题进行了认真研究,明确专人负责。6月18日,省直工会工委下发了《关于举办新任工会干部培训班的通知》,各单位工会根据通知要求,及时安排未参加过工会干部上岗培训的同志参加培训学习,同时省直工会及时与书店联系购买了《地方工会干部岗位培训辅导教材》、《劳动合同法》、《工会法》等3本培训资料共188套,发给参加培训的工会干部,确保了培训工作的顺利进行。
二、培训内容丰富,讲解通俗易懂。
这次培训共3天时间,结合当前的形势及工会职责,安排了“党的十八大报告宣讲、工会工作实务、工会法、劳动合同法、职代会制度建设、工会财务管理与经费审查、女职工工作等7个方面的内容课程。为确保培训质量,使参加培训的工会学到实在管用的知识,我们专门请到了省总工会原副巡视员王跃西、宣传部部长俞南平、女工部副部长安静、省直工会工委主任朱敏等有关工会领导、专家和经验丰富的老师进行授课。他们结合实际,进行了认真的准备,撰写讲课提纲,从工会的发展变化、法律法规的建立、当前劳动关系的变化、国际国内形势对工会发展的要求,工会维权职责等有关知识作了认真的讲解,深入浅出,通俗易懂,使大家对工会工作有了一个全新的认识,增强了做好工会工作的责任心和使命感。
三、领导重视、参加培训积极性高。
这次培训班原先计划培训120人左右,由于各单位党政工高度重视,要求没有参加过上岗培训的一次性全部进行培训,在人员安排上进行认真的研究,落实到个人,在工作上及时进行调整,保证参加学习的同志集中时间、集中精力参加培训学习,在经费上给予充分保证的情况下,主动报名参加培训的人员源源不断,直到培训班开班前还有同志直接到培训班报名要求参加培训。特别值得一提的是省广电网络公司工会在工作任务十分繁重的情况下抽调9个地州市分公司16名工会干部、省中八劳教所抽调13名工会干部和工会小组长全员参加了培训。尽管这次培训人数突破以往的记录,给培训工作带来一定的难度,但是负责培训的工作人员克服困难及时从北京组织教材,认真安排好学员食宿,保证了培训工作的顺利进行。
四、学习氛围浓厚,自觉遵守学习纪律。
参加培训的同志来自省直机关各基层单位,单位多、人数多,虽然培训班只有1名同志在负责管理,但是大家能够自觉地遵守学习纪律,不迟到,不早退,按时到课,专心听讲,认真做好读书笔记,课中大家对不懂和不了解的问题,能够主动提出来,与老师进行交流,课后大家相互交流学习心得体会,晚上还能够坚持自学,认真消化当天所学的课程,没有外出喝酒、打麻将或下河游泳等现象的发生,充分显示省直机关转变作风教育的成果。为检验学习成果,培训班利用学习结束后的1个小时对学员进行了测试,大家非常认真答好每道题,为这次培训交上了一份满意的答卷。
五、认真学习借鉴省外经验,推动我省机关工会工作。
培训班结束后,省直工会工委于7月2日又组织部分工会干部赴江西省直机关工会工委考察学习,通过与江西省直机关工会工委的对口交流,他们两项工作比较有特色,是值得我们学习和借鉴的。一是职工体育赛事活动。每年举办一次“百场篮球友谊赛”、“百场乒乓球友谊赛”活动,在赛制上革新以往按球队比赛胜负排列名次的老办法,改由按相互之间打的场次多少进行积分排列的新赛制。这种活动的开展凝聚了职工,调动了职工的积极性,促进了的和谐建设。二是建立“职工重大疾病医疗互助基金”。互助基金由参加医疗互助活动的在职职工缴纳,每人每年限交2份,每份标准为30元,凡在参加医疗互助期间首次确诊患有恶性肿瘤、再生障碍性贫血贫血、人体重要器官移植、冠状动脉搭桥、慢性肾功能衰竭尿毒症期、慢性肝功能衰竭失代偿期、瘫痪等7种重大疾病之一的,都将按照所交纳的互助金份数获得一次性补助1.5万或3万元。医疗互助金单独建账专人管理,专门用于重病救助,不另设开支项目,确保资金安全。这是以职工为本,关心职工、维护职工,为职工办实事,解难事的具体举措。
从贵州省直机关近几年来的情况看,在职职工发生重大疾病的情况有明显的上升趋势。由于没有建立职工重大疾病医疗互助基金,每次都是从工会工作经费中拿出3000—5000元对生病职工给予微不足道的补助,确实有些相形见拙。江西的做法和经验值得学习和借鉴,这项工作有待于从关心职工健康,为职工排忧解难,增强工会组织的凝聚力、向心力等方面进行不断探索和研究,进一步建立和完善省直机关困难职工帮扶机制。
为认真贯彻落实党的十八届三中全会精神,做好群众路线教育实践活动准备工作,健全完善党员轮训工作制度,提高党员队伍的整体素质,按照《关于开展冬季党员轮训工作的通知》(平党组发2013106号)文件精神,我局党员轮训工作从12月15日开始至2014年1月31日结束,为期1个半月,局机关及局属单位共68名党员及入党积极分子参加了轮训,参训率达96%以上。现将我局开展冬季党员轮训工作总结如下:
一、加强领导,提高认识,轮训工作有条不紊
一是组织到位。为确保党员轮训工作有条不紊的开展,我局总支印发了《人社局关于开展冬季党员轮训工作的安排意见》,明确了党员轮训工作的指导思想、学习内容、日程安排及工作要求,成立以总支书记为组长,各支部书记为成员的工作领导小组,确保了党员轮训工作的顺利进行。二是认真动员。轮训工作开始后,我局党总支于12月17日召开了全体党员大会,进行安排动员,要求局系统全体党员干部职工要强化认识,增强学习自觉性,结合各自思想、工作实际,认真抓好党员党性定性分析及评星定格工作,认真开展批评与自我批评,不断提高党员的思想、能力及作风建设,真正发挥***员的先锋模范作用。三是狠抓责任落实。局党总支将开展冬季党员轮训工作作为对各单位党建工作的一项重要考核内容,要求各支部书记为冬季轮训工作的第一责任人,形成一级抓一级层层抓落实,认真组织,精心安排,做到轮训工作与日常工作“两不误、两促进”。四是率先垂范,带头学习。在轮训过程中,局总支班子成员和各支部负责人自始至终带头参加学习,认真做好学习笔记,主动开展党员讲党课和批评与自我批评,起到了模范带头作用,党员干部职工树立了榜样。
二、重点突出,内容丰富,轮训学习氛围浓厚
此次轮训工作坚持以“三个代表”重要思想和落实科学发展观为统领,以学习党的十八大和十八届三中全会以及县委十三届七次全体扩大会议精神为重点,以加强政风行风和作风建设为目标,发挥党员先进性、提高党组织的战斗力和凝聚力。教育形式多样,内容丰富,教育面广,把党员轮训与反腐倡廉工作结合起来,同加强基层党组织的先进性建设结合起来,采取学习文件、专题辅导、观看录像、分组讨论等灵活多样的形式,深化学习效果。轮训中,一是邀请了县党校老师进行了十八届三中全会专题辅导。二是集中学习。利用党员大会,周一例会由总支书记及班子成员带领党员认真学习《关于深化改革若干重大问题的决定》、《关于深入落实“八项规定”反对“四风”务实节俭有关工作的通知》以及《厉行节约、反对浪费——重要论述摘编》等党的群众路线重要文献。三是开展专题讨论。组织班子成员和党员结合实际,开展专题讨论,交流学习心得,谈体会;开展普通党员和领导讲党课,使广大党员达到了相互学习,相互促进的作用。四是召开人社局廉政教育大会,传达学习了县委廉政教育大会相关文件精神,组织观看了党风廉政警示教育片,提高了广大党员反腐倡廉意识,筑牢思想道德防线。
全系统共开展集中培训14次,开展党员讲党课6次,参加党员人数68人,召开讨论会5场次,撰写心得体会60篇,撰写调研文章6篇,此次轮训,提高了党员的政治理论水平和思想觉悟,凝聚了党员的战斗力和向心力,加强了基层党的建设。
;关于化学原料药GMP厂房的问题
目录 1 拼音 2 英文参考 3 概述 4 GMP的历史 5 《药品生产质量管理规范》的最新版本 6 《药品生产质量管理规范(2010年修订)》实施对企业的影响 7 《药品生产质量管理规范(2010年修订)》产生的背景 8 参考资料 1 拼音
yào pǐn shēng chǎn zhì liàng guǎn lǐ guī fàn
2 英文参考Good Manufacture Practices,GMP [2010年版药典三部]
good practices in the manufacture and quality control of drugs
GMP
3 概述药品生产质量管理规范(Good Manufacture Practices,GMP)?是保证药品依照质量标准稳定地生产并进行质量控制的体系,实施GMP旨在降低药品生产过程中通过成品检验不可能去除的风险,这些风险主要包括:产品意外污染,危害人体健康或导致亡;药物容器标签错误,使得病人可能拿到错药;活性成分不足或过量,导致治疗无效或副反应。GMP涵盖生产的各个方面,从起始材料、厂房、设备到员工的培训和个人卫生。详细的书面操作细则对于可能影响成品质量的每个生产环节都是必要的。必须具有文件体系,证明在任何时间生产的制品,其每一步生产过程始终符合正确的操作细则。[1]
“GMP”是英文Good ManufacturingPractice的缩写,即“优良制造标准”之意。GMP是一种特别注重在生产过程中实施对产品质量与卫生安全的自主性管理制度,也是一套适用于制药、食品等行业的强制性标准。作为药品生产和质量管理的基本准则,GMP适用于药品制剂生产的全过程和原料药生产中影响成品质量的关键工序。
《药品生产质量管理规范》即中国版的GMP,是为规范药品生产质量管理,根据《中华人民共和国药品管理法》、《中华人民共和国药品管理法实施条例》制定的药品质量管理体系的一部分。涵盖影响药品质量的所有因素,包括确保药品质量符合预定用途的有组织、有计划的全部活动,是药品生产管理和质量控制的基本要求,旨在最大限度地降低药品生产过程中污染、交叉污染以及混淆、差错等风险,确保持续稳定地生产出符合预定用途和注册要求的药品。企业应当严格执行本规范,坚持诚实守信,禁止任何虚假、欺骗行为。
4 GMP的历史世界卫生组织上世纪60年代中开始组织制订药品GMP,1974年联合国将GMP分发给全体会员国,1975年11月提出了修订后的GMP,并在世界卫生组织技术报告第569号中正式发布。
中国则从上世纪80年代开始推行。我国于1985年由中国医药工业公司下发了《药品生产管理规范》。中国药材公司于1986年11月颁布了《中成药生产管理规范》,作为我国中药行业的GMP。
1988年,中国颁布了自己的药品GMP,并于1992年作了第一次修订。
1998年8月19日国家药品监督管理局成立后,以第9号局长令形式发布了《药品生产质量管理规范》(1998年修订),于1999年8月1日起正式施行并在2004年第一次在全国强制性推行GMP。
5 《药品生产质量管理规范》的最新版本《药品生产质量管理规范》(GMP)的最新版本《药品生产质量管理规范(2010年修订)》历经5年修订、两次公开征求意见,已经于2011年1月17日中华人民共和国卫生部令第79号发布,自2011年3月1日起实施。按照《中华人民共和国药品管理法》第九条规定,具体实施办法和实施步骤由国家食品药品监督管理局规定。
6 《药品生产质量管理规范(2010年修订)》实施对企业的影响自2011年3月1日起,新建药品生产企业、药品生产企业新建(改、扩建)车间应符合《药品生产质量管理规范(2010年修订)》的要求。现有药品生产企业将给予不超过5年的过渡期,并依据产品风险程度,按类别分阶段达到新版药品GMP的要求。2010年修订版GMP偏重于生产企业软件设施的改善,包括一套完善、成熟的管理系统,以用于检测生产流程中出现的人为疏忽等漏洞,包括原材料、工艺流程、消毒、技术、配方制剂、库房和物流等环节。
参照欧盟标准制定的新版GMP也被称作史上最严格的GMP。此轮升级改造很有可能牵扯到全国大小药企13000余家。业内人士估计,一旦新版GMP实施,预计药企平均需要投入500万元—1000万元,相当于一家药企1—2年的利润,而基础差些的投入或许更高达数千万至上亿,甚至数亿元。
虽然该政策对医药行业的长期发展来说是重大利好,但短期阵痛难免。新版GMP将快速拉高制药行业门槛,行业集中步伐加快,不合规的小型药厂将直接停产,或由大型药企收购改造,预计在新版GMP实施不久后甚至实施之前就会出现一大批被新版GMP淘汰出局的药企。
据不完全统计显示,1998年版的GMP规范,截至2005年3月有1112家医药企业在这一门槛之外,全国共有3959家生产企业通过,但也为此付出了1500多亿元的门槛费。
国家药监局药品安全监管司相关负责人也曾在公开场合表示,预计新规范的实施将使全国至少500家经营乏力的中小企业关停,而其他企业要符合新规定仅硬件投入合计需要2000亿—3000亿元。而中国医药企业管理协会副会长于明德则表示,新版GMP虽然给予中小企业3年的缓冲期,但上千家中小企业可能终将被淘汰。
有专家表示,从整体来看,新版GMP主要冲击的是地方型中小企业,新GMP反而为上市公司、龙头企业提供了并购和扩张机会。
7 《药品生产质量管理规范(2010年修订)》产生的背景目前,国内的药企70%—80%都是在5000万规模以下的小企业,医药行业“小、散、乱、差”,在资金投入上难以保证药品质量。“部分企业只看到眼前的利益,只想跟人家拼价钱,不断地降价,最后把质量都放弃了。”
麦肯锡的研究报告显示,目前中国仿制药价格只有全球市场仿制药价格的20%—30%。与国际市场相比,在我国仿制药品价格水平明显偏低,产业集中度极低,仿制品过度竞争,生产企业过多,造成同一药品之间质量价格差异奇大。比如部分仿制药品虽然出厂价和市场价都很低,但企业可能没有严格按规定工艺生产标准执行,或质量标准不高。
医药市场研究者李泊霆认为,发布新版GMP背后其中一个重要原因就是近几年国内不断出现的药品质量风波。主管部门不得不尽快出手整顿市场,使得药品生产市场“不是任何人都能进来参与的派对和狂欢”。
中国的医药企业及其产品在国际上整体处于弱势,药品出去的少,药企出去的更少。一个重要的原因就是标准和工艺不被认可,包括《药品生产质量管理规范》不被认可。中投顾问研究员郭凡礼直言,国内医药企业真正想要走出国门,和国际通用的标准接轨,那么必须实施新版GMP规范为其保驾护航。
这个并不是你封闭就可以的,关键是你的封闭要有文件支持,也就是验证,验证过你的干燥工段前的工序没有任何的交叉污染。
另外 你所说的GMP的厂房是洁净室还是什么?如果你所说的是洁净室 那就可以明确告诉你 没有必要,如果是无菌要求,经过验证这个进入最终干燥工段前可以达到无菌的要求就可以了。
但是如果你说的不是洁净室,比如指南规定中的要求:
0801 企业的生产环境应整洁;厂区地面、路面及运输等不应对药品生产造成污染;生产、行政、生活和辅助区总体布局应合理,不得互相妨碍。
1. 厂房周边环境情况,生产、行政、生活和辅助区的布局是否合理。
2. 化学合成、脏器组织处理及危险品库、试验动物房等的设置不得对原料药的生产造成污染。
3. 锅炉房的位置煤堆、煤渣的放置,垃圾存放,明沟处理,闲置物资堆放等不得影响原料药生产。
4. 兼有原料药及制剂生产企业,原料药生产不得对制剂生产造成污染或妨碍。
0901 厂房应按生产工艺流程及所要求的空气洁净度级别进行合理布局。
1. 工艺布局:化学合成及其他形式的前处理工序,与精、烘、包工序不得互相妨碍。
2. 厂房空气净化洁净度级别、布局应符合药品GMP中相应条款的规定。
3. 药品法定标准中列有无菌检查项目的原料药,其暴露环境应为10,000级背景下的局部100级;其他原料药的生产暴露环境不低于300,000级。
4. 无菌原料药内包装材料(直接接触药品)的最终处理环境应为10,000级;对于非最终灭菌的无菌原料药,内包装材料最终处理后的暴露环境应为100级或无菌10,000级背景下的局部100级。
这些都是必须的,无论你的生产是什么样子的,这些都是必须的。
你干燥的工段应该不是最后的吧?最后应该是包装啊。所以 把干燥和包装放置于洁净区域 其他工序符合上面的规定就可以了
还有一个问题,你的管道符合要求么?按照你的说法,你的管道在最终进入洁净区之前 内容物就已经达到最终成品了,对吧,你的设备已经直接接触产品了,你应该用到卫生级的材质做的管道,还有一个想不通的问题就是,那个你精制是在外面,既然要干燥,说明你干燥前就已经是湿品了,你湿品怎么通过管道输送?传送带?传送带肯定不行,其他的 我想不明白,如果你的产品在液体里进去,那就好说了,那你进去以后还有一个过滤或者离心的过程,这个就可以说是精制了。前面的不过是合成。
看不到工艺,不知道产品,也就只能这么分析下。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。