创新药,仿制药,原料药-原料药和创新药的区别
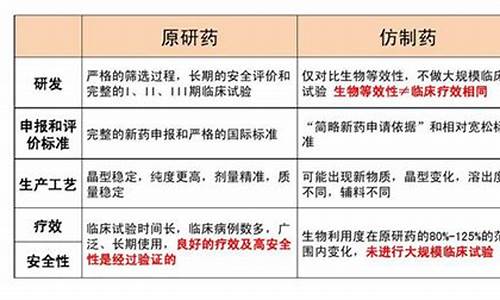
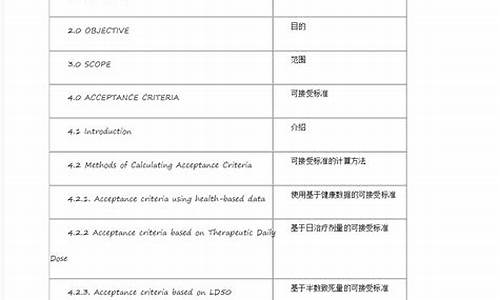
根据《化学药品注册分类改革工作方案》规定,药品3类和5.1类区别,在于申请主体是否属于境内和境外
3类是指:境内申请人仿制境外上市但境内未上市原研药品的药品。该类药品应与原研药品的质量和疗效一致。原研药品指境内外首个获准上市,且具有完整和充分的安全性、有效性数据作为上市依据的药品。
5.1类是指:境外上市的原研药品(包括原料药及其制剂)申请在境内上市。
扩展资料:
其他类别药品
1类:境内外均未上市的创新药。指含有新的结构明确的、具有药理作用的化合物,且具有临床价值的药品。
2类:境内外均未上市的改良型新药。指在已知活性成份的基础上,对其结构、剂型、处方工艺、给药途径、适应症等进行优化,且具有明显临床优势的药品。
4类:境内申请人仿制已在境内上市原研药品的药品。该类药品应与原研药品的质量和疗效一致。
参考资料:百度百科——化学药品注册分类改革工作方案
题主应该根据自己的专业和工作经历来决定哪个工作更适合。
紧跟企业主业发展制药厂的主业,一般有研发和生产两条主线,另外重要的还有销售。研发决定了药厂产品的竞争力和今后的发展方向;生产是药厂的最重要工作,生产质量是命脉所在,生产的产品一旦出了问题,对药厂的发展往往是致命的;销售是药厂参与市场竞争,增加收入,回笼资金的重要工作。
当然,这是一般而论,药企的发展模式不同,侧重面也不同。做原料药的更关注生产,做创新药的更重视研发,做仿制药的更注重销售。
在药企中要有一个更好的发展,必须结合企业的实际情况,紧跟主业发展。
对于题主的问题,一般来说药企的商标注册有多个渠道可以完成,可以自己独立去做,也可以合作完成,也可以外包出去。商标注册不能说不重要,但是并不是决定性的工作。
药企的质量管理是系统化、科学化的综合管理,相对复杂,不是一朝一夕就能建立的,也不是建立后走个过场应付检查的。一个好的制药企业,质量管理工作必然是和企业的发展息息相关、密不可分的,也必然会重视质量管理工作。
建议题主有机会更多的从事质量管理工作。
祝好运。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。