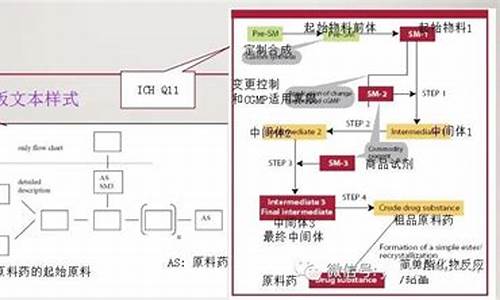
原料药生产日期-原料药生产日期 GMP

1、发运中药材的包装必须注明:品名、产地、日期、调出单位,并附有质量合格的标志。(药品管理法,P56,53条)
2、中药饮片的标签:品名、规格、产地、生产企业、产品批号、生产日期、实施批准文号管理的中药饮片必须注明药品批准文号。(注意没有:有效期)(药品管理法实施条例,P67,45条)
3、标签或说明书
药品管理法规定:通用名、成分、规格、生产企业、批准文号、产品批号、生产日期、有效期、适应症或功能主治、用法、用量、禁忌、不良反应和注意事项。(药品管理法,P56,54条)
4、药品内标签:药品通用名称、适应症或功能主治、规格、用法用量、生产日期、产品批号、有效期、生产企业等。内标签因包装尺寸过小至少应当标注的有:药品通用名称、规格、产品批号、有效期等P220,17条
药品外标签:药品通用名称、成份、性状、适应症或功能主治、规格、用法用量、不良反应、禁忌、注意事项、贮藏、生产日期、产品批号、有效期、批准文号、生产企业等。P220,18条
5、运输、储藏的'包装标签:药品通用名称、规格、贮藏、生产日期、产品批号、有效期、批准文号、生产企业,可根据需要注明:包装数量、运输注意事项或者其他标记等。P220,19条
运输、储藏包装和原料药标签标示的内容比较(P220,19、20条)
①?规格?标示在运输、储藏包装的标签中,而没有标示在原料药标签中。
②?执业标准? 没有标示在运输、储藏包装的标签中,而标示在原料药标签中。
③运输、储藏包装标示的是?药品通用名称?;原料药标签标示的是?药品名称?。
6、原料药的标签:药品名称、贮藏、生产日期、产品批号、有效期、执行标准、批准文号、生产企业,同时还需要注明包装数量、运输注意事项等。
“货架期”跟有效期由什么区别?
第一个问题:肯定是假药。首先,目前还没有一个正规厂家是把药品专门放在网上卖的,因为国家药品监督管理局绝不容许。其次,药品生产批号一般是指生产投料的日期,比如080201的批号,080222生产是可以理解的,如果投料将近一年了再生产,那就匪夷所思了。
第二个问题:药品生产批号与生产日期不一定必须一致,但不会相差太远,一般都只相差几天,最多也就当月。其原因在第一个问题里已经回答了。
兽药标签和说明书管理办法
保质期:产品的保质期是指产品的最佳食用期。产品的保质期由生产者提供,标注在限时使用的产品上。在保质期内,产品的生产企业对该产品质量符合有关标准或明示担保的质量条件负责,销售者可以放心销售这些产品,消费者可以安全使用。
保存期: 可以理解为有效期,也就是指在正常条件下,食品的最终食用期。 如果某一食品超过了保质期,但其不一定就超过了保存期。换句话说,保质期保证的是在标注时间内产品的质量是最佳的,超过保质期的食品,如果色、香、味没有改变,仍然可以食用。但超过了保存期的食品,质量会发生变化,因此不能再食用,更不能用以出售。根据《食品标签通用标准》规定,在任何情况下,食品的生产Lt期都不能省略,而保质期、保存期可以任选或同时标出。
货架期 :货架期指食品被贮藏在推荐的条件下,能够保持安全;确保理想的感官、理化和微生物特性;保留标签声明的任何营养值的一段时间。
保质期<货架期<保存期
龙虎人丹生产日期在哪
第一章 总则第一条 为加强兽药监督管理,规范兽药标签和说明书的内容、印制、使用活动,保障兽药使用的安全有效,根据《兽药管理条例》,制定本办法。第二条 农业部主管全国的兽药标签和说明书的管理工作,县级以上地方人民政府畜牧兽医行政管理部门主管所辖地区的兽药标签和说明书的管理工作。第三条 凡在中国境内生产、经营、使用的兽药的标签和说明书必须符合本办法的规定。第二章 兽药标签的基本要求第四条 兽药产品(原料药除外)必须同时使用内包装标签和外包装标签。第五条 内包装标签必须注明兽用标识、兽药名称、适应症(或功能与主治)、含量/包装规格、批准文号或《进口兽药登记许可证》证号、生产日期、生产批号、有效期、生产企业信息等内容。
安瓿、西林瓶等注射或内服产品由于包装尺寸的限制而无法注明上述全部内容的,可适当减少项目,但至少须标明兽药名称、含量规格、生产批号。第六条 外包装标签必须注明兽用标识、兽药名称、主要成分、适应症(或功能与主治)、用法与用量、含量/包装规格、批准文号或《进口兽药登记许可证》证号、生产日期、生产批号、有效期、停药期、贮藏、包装数量、生产企业信息等内容。第七条 兽用原料药的标签必须注明兽药名称、包装规格、生产批号、生产日期、有效期、贮藏、批准文号、运输注意事项或其它标记、生产企业信息等内容。第八条 对贮藏有特殊要求的必须在标签的醒目位置标明。第九条 兽药有效期按年月顺序标注。年份用四位数表示,月份用两位数表示,如“有效期至2002年09月”,或“有效期至2002.09”。第三章 兽药说明书的基本要求第十条 兽用化学药品、抗生素产品的单方、复方及中西复方制剂的说明书必须注明以下内容:兽用标识、兽药名称、主要成分、性状、药理作用、适应症(或功能与主治)、用法与用量、不良反应、注意事项、停药期、外用杀虫药及其他对人体或环境有毒有害的废弃包装的处理措施、有效期、含量/包装规格、贮藏、批准文号、生产企业信息等。第十一条 中兽药说明书必须注明以下内容:兽用标识、兽药名称、主要成分、性状、功能与主治、用法与用量、不良反应、注意事项、有效期、规格、贮藏、批准文号、生产企业信息等。第十二条 兽用生物制品说明书必须注明以下内容:兽用标识、兽药名称、主要成分及含量(型、株及活疫苗的最低活菌数或病毒滴度)、性状、接种对象、用法与用量(冻干疫苗须标明稀释方法)、注意事项(包括不良反应与急救措施)、有效期、规格(容量和头份)、包装、贮藏、废弃包装处理措施、批准文号、生产企业信息等。第四章 兽药标签和说明书的管理第十三条 兽药标签和说明书必须按照兽药批准权限,经农业部或省级畜牧兽医行政管理部门审核批准后方可使用。内容变更时须按原申报程序履行审批手续。第十四条 兽药标签和说明书必须按照本规定的统一要求印制,其文字及图案不得擅自加入任何未经批准的内容。第十五条 兽药标签和说明书的内容必须真实、准确,不得虚假和夸大,也不得印有任何带有宣传、广告色彩的文字和标识。第十六条 兽药标签和说明书的内容不得超出或删减规定的项目内容;不得印有未获批准的专利、兽药GMP、商标等标识。第十七条 兽药标签和说明书所用文字必须是中文,并使用国家语言文字工作委员会公布的现行规范化汉字。根据需要可有外文对照。第十八条 根据需要,兽药标签上可使用条形码;已获批准的专利产品,可标注专利标记和专利号,并标明专利许可种类;注册商标应印制在标签和说明书的左上角或右上角;已获兽药GMP合格证的,必须按照兽药GMP标识使用有关规定正确地使用兽药GMP标识。第十九条 兽药标签和说明书的字迹必须清晰易辨,兽用标识及外用药标识应清楚醒目,不得有印字脱落或粘贴不牢等现象,并不得用粘贴、剪切的方式进行修改或补充。第二十条 兽药标签和说明书内容对产品作用与用途项目的表述不得违反法定兽药标准的规定,并不得有扩大疗效和应用范围的内容;其用法与用量、停药期、有效期等项目内容必须与法定兽药标准一致,并使用符合兽药国家标准要求的规范性用语。第二十一条 兽药标签和说明书上必须标识兽药通用名称,可同时标识商品名称。商品名称不得与通用名称连写,两者之间应有一定空隙并分行。通用名称与商品名称用字的比例不得小于1:2(指面积),并不得小于注册商标用字。
执业药师《法规》每日一练-2019天津医考(2019.9.16)
在包装盒上。
龙虎人丹生产日期在包装盒上,保质期一般都在说明书或者盒子后侧的说明简介边上,可以仔细找一下。
龙虎人丹是由上海中华制药厂生产的中成药,上海中华制药厂创建于1911年,是近代中国第一家民族制药工业企业。是生产抗生素原料药、中西成药制剂和营养滋补品的综合型制药企业,历史悠久,质量稳定,具有先进的生产工艺和测试仪器,产品大部分出口。近几年不断开发新产品,生产规模逐年扩大,综合管理水平、质量保证体系日趋健全和完善。现已被评为上海市“高新技术企业。
中药材购销的管理行业规定有哪些
2019执业药师《药事管理与法规》每日冲刺
1. 关于药品说明书内容的说法,错误的是
A.药品说明书应当列出全部活性成分或者组方中的全部中药药味
B.非处方药说明书应当列出所用的全部辅料名称
C.注射剂的说明书应当列出所用的全部辅料名称
D.口服缓释制剂的说明书应当列出所用的全部辅料名称
2. 说明书用法用量项下要求的内容不包括
A.用药的剂量 B.用药次数
C.疗程期限 D.药品的装量
3. 说明书用法用量项中的内容不包括
A.用药的剂量 B.中毒剂量
C.计量方法 D.疗程期限
4. 下列药品有效期标注格式,错误的是
A.有效期至?/?/ B.有效期至年?月?日
C.有效期至.?. D.有效期至/?/?
5. 以下有关药品商品名称规定的表述,正确的是
A.药品商品名称的字体颜色应当使用黑色或者白色
B.药品商品名称的字体以单字面积计不得大于通用名称所用字体的四分之一
C.药品通用名称的字体和颜色不得比药品商品名称更突出和显著
D.药品商品名称不得与通用名称同行书写
6 根据《药品说明书和标签管理规定》,在药品说明书中应列出全部辅料名称的是
A.处方药 B.品和第一类精神药品
C.获得中药一级保护的中药品种 D.注射剂
7. 说明书药品名称项中所列顺序正确的是
A.通用名称、汉语拼音、商品名称、英文名称
B.通用名称、商品名称、英文名称、汉语拼音
C.通用名称、商品名称、汉语拼音、英文名称
D.通用名称、英文名称、商品名称、汉语拼音
8. 一般不在说明书注意事项项中说明的是
A.需要慎重的情况 B.影响药物疗效的因素
C.禁止应用该药品的疾病情况 D.用药过程中需观察的情况
配伍选择题
[9-10]
A.药品说明书 B.药品外标签
C.运输包装的标签 D.原料药标签
9. 应当列出全部活性成分或者组方中的全部中药药味的是
10. 应当注明药品名称、贮藏、生产日期、产品批号、有效期、执行标准、批准文号、生产企业等内容的是
[11-12]
A.有效期 B.规格
C.产品批号 D.执行标准
11. 原料药标签的内容不包括
12. 药品内标签的内容不包括
[13-14]
A.药品的外标签 B.药品的内标签
C.用于运输、储藏的药品的包装标签 D.原料药的标签
13. 至少应当标注药品通用名称、规格、产品批号、有效期等内容的标签是
14. 至少应当注明药品名称、贮藏、生产日期、产品批号、有效期、执行标准、批准文号、生产企业等内容的标签是
参考答案及解析
1答案D。解析:本题主要考查药品说明书管理规定。关于药品说明书中所列内容的要求为:①列出全部活性成分或者组方中的全部中药药味;②注射剂和非处方药列出所用的全部辅料名称;③处方中含有可能引起严重不良反应的成份或者辅料的,应当在注意事项予以说明。故本题选D。
2答案D。解析:本题主要考查药品说明书管理规定。用法用量应当包括用法和用量两部分。需按疗程用药或者规定用药期限的,必须注明疗程、期限。应当详细列出该药品的用药方法,准确列出用药的剂量、计量方法、用药次数以及疗程期限,并应当特别注意与规格的关系。故选D。
3答案B。解析:本题主要考查药品说明书管理规定。药品说明书用法用量项中的内容不包括中毒剂量,故选B。
4答案A。解析:本题主要考查药品标签管理规定。药品标签上药品有效期格式:(1)"有效期至年?月""有效期至.?.";(2)"有效期至年?月?日""有效期至/?/?"。故B、C、D正确,A错误。
5答案D。解析:本题主要考查药品名称使用要求。(1)药品通用名称应当显著、突出,其字体、字号和颜色必须一致,并符合以下要求:①对于横版标签,必须在上三分之一范围内显著位置标出;对于竖版标签,必须在右三分之一范围内显著位置标出;②不得选用草书、篆书等不易识别的字体,不得使用斜体、中空、阴影等形式对字体进行修饰;③字体颜色应当使用黑色或者白色,与相应的浅色或者深色背景形成强烈反差;④除因包装尺寸的限制而无法同行书写的,不得分行书写。(2)药品商品名称不得与通用名称同行书写,其字体和颜色不得比通用名称更突出和显著,其字体以单字面积计不得大于通用名称所用字体的二分之一。故选D。
6答案D。解析:本题主要考查药品说明书和标签管理规定。关于药品说明书中所列内容的要求为:①列出全部活性成分或者组方中的全部中药药味;②注射剂和非处方药列出所用的全部辅料名称;③处方中含有可能引起严重不良反应的成份或者辅料的,应当在注意事项予以说明。答案选D。
7答案B。解析:本题主要考查药品说明书管理规定。化学药品和治疗用生物制品的药品名称按下列顺序列出:通用名称、商品名称、英文名称、汉语拼音。故选B。
8答案C。解析:本题主要考查药品说明书管理规定。注意事项列出使用时必须注意的问题,包括:①需要慎用的情况(如肝、肾功能的问题);②影响药物疗效的因素(如食物、烟、酒);③用药过程中需观察的情况(如过敏反应,定期检查血象、肝功、肾功);④用药对于临床检验的影响等。禁忌中应当列出禁止应用该药品的人群或者疾病情况。故选C。
[9-10]答案AD。解析:本题主要考查药品说明书管理规定。(1)关于药品说明书中所列内容的要求为:①列出全部活性成分或者组方中的全部中药药味;②注射剂和非处方药列出所用的全部辅料名称;③处方中含有可能引起严重不良反应的成份或者辅料的,应当在注意事项予以说明。(2)原料药的标签应当注明药品名称、贮藏、生产日期、产品批号、有效期、执行标准、批准文号、生产企业,同时还需注明包装数量以及运输注意事项。故选A、D。
[11-12]答案BD。解析:本题主要考查药品标签管理规定。(1)原料药标签标示的内容包括:药品名称、贮藏、生产日期、产品批号、有效期、执行标准、批准文号、生产企业,同时还需注明包装数量以及运输注意事项。(2)药品的内标签标示的内容包括:药品通用名称、适应症或者功能主治、规格、用法用量、生产日期、产品批号、有效期、生产企业。(3)药品外标签标示的内容包括:药品通用名称、成分、性状、适应症或者功能主治、规格、用法用量、不良反应、禁忌、注意事项、贮藏、生产日期、产品批号、有效期、批准文号、生产企业。(4)运输、储藏包装标签标示的内容包括:药品通用名称、规格、贮藏、生产日期、产品批号、有效期、批准文号、生产企业,也可以根据需要注明包装数量、运输注意事项或者其他标记。故选B、D。
[13-14]答案BD。解析:本题主要考查药品标签管理规定。(1)内标签包装尺寸过小无法全部标明的,至少应当标注药品通用名称、规格、产品批号、有效期。(2)原料药的标签应当注明药品名称、贮藏、生产日期、产品批号、有效期、执行标准、批准文号、生产企业,同时还需注明包装数量以及运输注意事项。故选B、D。
?
药品有效期与批号有哪些区别?
《中华人民共和国药品管理法》及《中华人民共和国药品管理法实施条例》以及相关规章、规范性文件对中药管理做出了一些明文规定。
1.《药品管理法》的规定
“国家保护野生药材资源,鼓励培育中药材。”(第3条)
“除中药饮片的炮制外,药品必须按照国家药品标准和药品监督管理部门批准的生产工艺进行生产,生产记录必须准确无误。……”
“中药饮片必须按照国家药品标准炮制,国家药品标准没有规定的,必须按照省、自治区、直辖市人民政府药品监督管理部门制定的炮制规范炮制。省、自治区、直辖市人民政府药品监督管理部门制定的炮制规范应当报药品监督管理部门备案。”(第10条第二款)
“药品经营企业销售中药材,必须标明产地。”(第l9条)
“城乡集市贸易市场可以出售中药材医学|教育网搜集整理,另有规定的除外。”“城乡集市贸易市场不得出售中药材以外的药品,……”(第21条)
“生产新药或者已有国家药品标准的药品的,须经药品监督管理部门批准,并发给药品批准文号;但是生产没有实施批准文号管理的中药材、中药饮片除外。实施批准文号管理的中药材、中药饮片品种目录由药品监督管理部门会同中医药管理部门制定。”(第31条)
“药品必须符合国家药品标准。中药饮片依照本法第十条第二款规定执行。”(第32条)
“药品生产企业、药品经营企业、医疗机构必须从具有药品生产、经营资格的企业购进药品,但是购进没有实施批准文号管理的中药材除外。”(第34条)
“国家实行中药品种保护制度。具体办法由制定。”(第36条)
“新发现和从国外引种的药材,经药品监督管理部门审核批准后,方可销售。(第46条)”
“地区性民间习用药材的管理办法,由药品监督管理部门会同中医药管理部门制定。”(第47条)
“发运中药材必须有包装。每件包装上,必须注明品名、产地、日期、调出单位。并附有质量合格的标志。”(第53条)
“中药材的种植、采集和饲养的管理办法,由另行规定。”(第103条)
2.《药品管理法实施条例》的规定
“药品生产企业生产药品所使用的原料药,必须具有药品监督管理部门核发的药品批准文号或者进口药品注册证书、医药产品注册证书;但是未实施批准文号管理的中药材、中药饮片除外。”(第9条)
“国家鼓励培育中药材。对集中规模化栽培养殖、质量可以控制并符合药品监督管理部门规定条件的中药材品种医学|教育网搜集整理,实行批准文号管理。”(第40条)
“生产中药饮片,应当选用与药品性质相适应的包装材料和容器;包装不符合规定的中药饮片,不得销售。中药饮片包装必须印有或者贴有标签。”“中药饮片的标签必须注明品名、规格、产地、生产企业、产品批号、生产日期,实施批准文号管理的中药饮片还必须注明批准文号。”(第45条)
3.中药管理的其他规定
(1)国家对部分重点中药材购销实行严格管理
在购销活动中实行国家管理的重点中药材有以下两类:
第一类:野生、名贵品种,麝香、杜仲、厚朴、甘草。
第二类:产地集中、调剂面大的品种,黄连、当归、川芎、生地、白术、白芍、茯苓、麦冬、黄芪、贝母、银花、牛膝、元胡、桔梗、菊花、连翘、山萸肉、三七、人参、牛黄,共20种。
(2)国家实行进出口管理的中药材品种
①实行部分中药材出口管理的规定
出口按照先国内、后国外的原则,国内中药材生产供应严重不足时应停止或减少出口,国内供应有余品种应鼓励出口。出口中药材必须经对外经济贸易部门审批,办理《出口中药材许可证》后,方可办理出口手续,目前国家对35种中药材出口实行审批管理,具体品种如下:人参、鹿茸、当归、蜂王浆(包括粉)、三七、麝香、甘草及其制品、杜仲、厚朴、黄芪、党参、黄连、半夏、茯苓、菊花、枸杞、山药、川芎、生地、贝母、银花、白芍、白术、麦冬、天麻、大黄、冬虫夏草、丹皮、桔梗、元胡、牛膝、连翘、罗汉果、牛黄。
②实行部分中药材进口审批管理
根据1986年1月15日国发(1986)8号文件的规定,国家对以下l3种中药材实行进口审批制度:首先取得《进口许可证》后,方可进口,具体品种是:豆蔻、血竭、羚羊角、广角、豹骨、沉香、牛黄、麝香、砂仁、西红花、胖大海、西洋参、海马。为进一步加强进口药材监督管理,保证进口药材质量,2005年3月2日召开的全国药品注册工作会讨论制定了《进口药材管理办法》。
批号是该产品原料批次编号,药品有效期是相对与生产日期。生产日期是该药品制作成型并包装好预备销售的日期。产品可以有同批号不同生产日期。也可以有同生产日期不同批号。如果一个药品出现质量问题一般是以批次为单位,(例如召回某批次药品)而不是以生产日期为单位。
《药品生产质量管理规范》对确定批号的原则作了这样的规定:
无菌药品:(1)大、小容量注射剂以同一配液罐一次所配制的药液所生产的均质产品为一批。(2)粉针剂以同一批原料药在同一连续生产周期内生产的均质产品为一批。 (3) 冻干粉针剂以同一批药液使用同一台冻于设备在同一生产周期内生产的均质产品为一批。
非无菌药品:(1)固体、半固体制剂在成型或分装前使用同一台混合设备一次混合量所生产的均质产品为一批。(2)液体制剂以灌装(封)前经最后混合的药液所生产的均质产品为一批。
原料药:(1)连续生产的原料药,在一定时间间隔内生产的在规定限度内的均质产品为一批。(2)间歇生产的原料药,可由一定数量的产品经最后混合所得的在规定限度内的均质产品为一批。混合前的产品必须按同一工艺生产并符合质量标准,且有可追踪的记录。
生物制品:应按照《中国生物制品规程》中的“生物制品的分批规程”分批和编写批号。
中药制剂: (1)固体制剂在成型或分装前使用同一台混合设备一次混合量所生产的均质产品为一批。如采用分次混合,经验证,在规定限度内所生产一定数量的均质产品为一批。(2)液体制剂、膏滋、浸膏、流浸膏等以灌装(封)前经同一台混合设备最后一次混合的药液所生产的均质产品为一批。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。