细菌内毒素工作标准品效价标定-原料药细菌内毒素限度
题主是否想询问“湖北天门5%阿维菌素是什么,生产标准的介绍”阿维菌素是一种广谱抗生素,主要用于治疗细菌感染。湖北天门地区生产的5%阿维菌素主要是指阿维菌素钠盐注射液。以下是生产标准的介绍:
1、原料药:阿维菌素钠盐符合《中华人民共和国药典》规定的质量标准。
2、辅料:注射用水符合《中华人民共和国药典》规定的质量标准。
3、生产工艺:生产过程符合药品生产质量管理规范的要求,包括原料药的检测、制剂生产、灭菌、包装等环节,确保产品质量符合国家标准和相关规定。
4、质量标准:产品符合《中华人民共和国药典》和国家药品监督管理局制定的相关标准和规定,包括外观、溶解度、PH值、有效成分含量、细菌内毒素、微生物限度等指标。
5、包装和储存:产品采用符合卫生要求的包装材料进行包装,并在干燥、阴凉、通风、无异味的环境中储存,避免受潮、受热和日光照射。
新药开发中药物分析一般程序
《中华人民共和国药典)2015年版:
分四部出版,一部为中药;二部为化学药;三部为生物制品;四部为总则。
扩展资料
《中华人民共和国药典》(简称《中国药典》)2015年版,药典包括凡例、正文及附录,是药品研制、生产、经营、使用和监督管理等均应遵循的法定依据。所有国家药品标准应当符合中国药典凡例及附录的相关要求。
新版药典进一步扩大药品品种的收载和修订,共收载品种5608种。一部收载品种2598种,其中新增品种440种。二部收载品种2603种,其中新增品种492种。三部收载品种137种,其中新增品种13种、修订品种105种。
首次将上版药典附录整合为通则,并与药用辅料单独成卷作为新版药典四部。四部收载通则总数317个,其中制剂通则38个、检测方法240个、指导原则30个、标准物质和对照品相关通则9个;药用辅料收载270种,其中新增137种、修订97种。
1949年10月1日中华人民共和国成立后,党和政府十分关怀人民的医药卫生保健工作,当年11月卫生部召集在京有关医药专家研讨编纂药典问题。1950年1月卫生部从上海调药学专家孟目的教授负责组建中国药典编纂委员会和处理日常工作的干事会,筹划编制新中国药典。
1950年4月在上海召开药典工作座谈会,讨论药典的收载品种原则和建议收载的品种,并根据卫生部指示,提出新中国药典要结合国情,编出一部具有民族化、科学化、大众化的药典。
随后,卫生部聘请药典委员49人,分设名词、化学药、制剂、植物药、生物制品、动物药、药理、剂量8个小组,另聘请通讯委员35人,成立了第一届中国药典编纂委员会。卫生部部长李德全任主任委员。
1951年4月24日至28日在北京召开第一届中国药典编纂委员会第一次全体会议,会议对药典的名称、收载品种、专用名词、度量衡问题以及格式排列等作出决定。干事会根据全会讨论的意见,对药典草案进行修订,草案于1952年底报卫生部核转政务院文教委员会批准后,第一部《中国药典》1953年版由卫生部编印发行。
1953年,版药典共收载药品 531种,其中化学药 215种,植物药与油脂类 65种,动物药13种,抗生素2种,生物制品25种,各类制剂211种。药典出版后,于1957年出版《中国药典》1953年版第一增补本。
1955年,卫生部成立第二届药典委员会,聘请委员49人,通讯委员68人,但这届委员会因故未能进行工作。1957年成立第三届药典委员会,聘请委员80人,药学专家汤腾汉教授为这届委员会主任委员(不设通讯委员),同年7月28日至8月5日在北京召开第一次全体委员会议,卫生部李德全部长作了药典工作报告,特别指出第一版中国药典没有收载广大人民习用的中药,是个很大的缺陷。
会议在总结工作的基础上,通过了制订药典的原则,讨论了药典的性质和作用,并修改了委员会章程,会议一致认为应把合乎条件的中药收载到药典中。8月27日卫生部批准委员会分设药理与医学、化学药品、药剂、生化药品、生药、生物制品六个专门委员会及名词小组,药典委员会设常务委员会,日常工作机构改称秘书室。
1958年,经常务委员会研究并经卫生部批准,增聘中医专家8人、中药专家3人组成中医药专门委员会,组织有关省市的中医药专家,根据传统中医药的理论和经验,起草中药材和中药成方(即中成药)的标准。
1959年6月25日至7月5日在北京召开这届委员会第二次全体会议,会议主要审议新版药典草稿,并确定收载品种。草稿经修订补充后,分别由各 专门委员会审定,于1962年完成送审稿,报请批准后付印,1965年1月26日卫生部公布《中国药典》1963年版,并发出通知和施行办法。
1963年版药典共收载药品1310种,分一、二两部,各有凡例和有关的附录。一部收载中医常用的中药材446种和中药成方制剂197种;二部收载化学药品667种。此外,一部记载药品的"功能与主治",二部增加了药品的"作用与用途"。
1966年,由于""影响,药典委员会工作陷于停顿。1972年4月28日批复卫生部"同意恢复药典委员会,四部(卫生部、燃料化 学工业部、商业部、解放军总后卫生部)参加,卫生部牵头"。
据此,同年5月31日至6月10日在北京召开了编制国家新药典工作会议,出席会议的有全国各省 (自治区、直辖市)的药品检验、药政管理以及有关单位代表共88人。这次会议着重讨论了编制药典的指导思想、方法、任务和要求,交流了工作经验,确定了编 制新药典的方案,并分工落实起草任务。
1973年4月,在北京召开第二次全国药典工作会议,讨论制订药典的一些原则要求,以及中西药品的标准样稿和起草说 明书,并根据药材主产地和药品生产情况,调整了起草任务。1979年10月4日卫生部颁布《中国药典》1977年版自1980年1月1日起执行。
1977 年版药典共收载药品1925种。一部收载中草药材(包括少数民族药材)、中草药提取物、植物油脂以及一些单味药材制剂等882种,成方制剂(包括少数民族 药成方)270种,共1152种;二部收载化学药品、生物制品等773种。
1979年,由卫生部聘请委员112人组建第四届药典委员会,卫生部部长钱信忠兼任主任委员。同年11月22日至 28日在北京召开这届第一次全体委员会议,会议讨论修改了委员会章程、药品标准工作管理办法及工作计划。
委员会分设:中医、中药、医学与药理、化学药、生化药、药剂、抗生素、生物制品、放射品及名词10个专业组。由有关专业组分别推荐新药典收载的品种,中医专业组负责审查拟定一部收载的品种范围;
医学与药理专业组负责审查拟定二部收载的品种范围;由主产地所在的省(自治区、直辖市)药品检验所和有关单位负责起草标准,药典委员会办公室组织交叉复核,有 些项目组成专题协作组通过实验研究后起草,标准草案经有关专业组委员并邀请有关药品检验所和药厂的代表讨论审议后报卫生部审批。《中国药典》1985年版 于1985年9月出版。
1986年4月1日起执行。该版药典共收载药品1489种。一部收载中药材、植物油脂及单味制剂506种,中药成方207种,共713种;二部收载化学药品、生物制品等776种。
1985年7月1日《中华人民共和国药品管理法》正式执行,该法规定"药品必须符合国家药品标准或者省、自治区、直辖市药品标准"。明确"国务 院卫生行政部门颁布的《中华人民共和国药典》和药品标准为国家药品标准"。"卫生行政部门的药典委员会,负责组织国家药品标准的制定和修订"。进一步确定了药品标准的法定性质和药典委员会的任务。
1986年,卫生部根据药典委员会章程聘请委员150人组建第五届药典委员会,由卫生部崔月犁部长兼任主任委员,常设办事机构改为秘书长制。
同年 5月5日至8日召开第五届第一次全体委员会议,讨论修订了委员会章程,通过了"七五"期间标准工作设想,确定编制《中国药典》1990年版的指导思想和原则要求。分别举行中药材、中药成方制剂、化学药、抗生素、生化药及药理等专业会议,安排起草和科研任务。
1987年11月出版《中国药典》1985年版增 补本,新增品种23种,修订品种172种,附录21项。1988年10月,第一部英文版《中国药典》1985年版正式出版。同年还出版了药典二部注释选 编。1989年3月,各地起草的1990年版药典标准初稿基本完成,药典委员会常设机构开始组织审稿和编辑加工。
同年12月在北京举行药典委员会主任委 员、副主任委员和各专业组长扩大会议进行审议,报卫生部批准后付印。1990年12月3日卫生部颁布《中国药典》1990年版自1991年7月1日起执行。
这版药典分一、二两部,共收载品种1751种。一部收载784种,其中中药材、植物油脂等509种,中药成方及单味制剂275种;二部收载化学 药品、生物制品等967种。与1985年版药典收载品种相比,一部新增80种,二部新增213种(含1985年版药典一部移入5种);删去25种(一部3种,二部22种);对药品名称,根据实际情况作了适当修订。
药典二部品种项下规定的"作用与用途"和"用法与用量",分别改为"类别"和"剂量",另组织编著《临床用药须知》一书,以指导临床用药。有关品种的红外光吸收图谱,收入《药品红外光谱集》另行出版,该版药典附录内不再刊印。
1991年,组建第六届药典委员会,由卫生部聘请委员共168人,卫生部陈敏章部长兼任主任委员。同年5月16日至18日召开第一次全体委员会议,讨论通过了委员会的章程和编制《中国药典》1995年版设计方案,并成立由主任委员、副主任委员和专家共11人组成的常务委员会。
分设13个专业组, 即:中医专业组、中药材专业组、中成药专业组、西医专业组、药理专业组、化学药专业一组、化学药专业二组、化学药专业三组、抗生素专业组、生化药品专业组、生物制品专业组、放射品专业组、药品名词专业组。会后,各专业组分别召开专业组委员扩大会议,安排落实全会提出的任务。
1993年,《中国药典》1995年版附录初稿发往各地作为起草、修订正文标准的依据。1994年7月各地基本完成了标准的起草任务,由药典委员会各专业委员会分别组织审稿工作。1994年11月29日提交常务委员会扩大会议讨论审议,获得原则通过,报请卫生部审批付印。卫生部批准颁布《中国药 典》1995年版自1996年4月1日起执行。
这版药典收载品种共计2375种。一部收载920种,其中中药材、植物油脂等522种,中药成方及单味制剂398种;二部收载1455种,包括 化学药、抗生素、生化药、放射品、生物制品及辅料等。一部新增品种142种,二部新增品种499种。
二部药品外文名称改用英文名,取消拉丁名;中文名 称只收载药品法定通用名称,不再列副名。编制出版《药品红外光谱集》第一卷(1995年版)。《临床用药须知》一书经修订,随《中国药典》1995年版同时出版,经卫生部批准,其中的"适应证"和"剂量"部分作为药政和生产部门宣传使用和管理药品的依据。
这届药典委员会除完成1995年版药典的编制外,还于1992年、1993年先后编制出版《中国药典》1990年版第一、第二增补本,二部注释 和一部注释选编,《中药彩色图集》和《中药薄层色谱彩色图集》以及《中国药品通用名称》等标准方面的配套丛书。《中国药典》1990年版英文版亦于1993年7月出版发行。
1996年5月,经卫生部批准,第七届药典委员会成立,由卫生部聘请204位委员组成,其中名誉委员18人,卫生部陈敏章部长兼任主任委员。
1998年9月,根据中编办(1998)32号文:卫生部药典委员会更名为国家药典委员会,并成建制划转国家药品监督管理局管理。因管理体制的变化及 1999年3月陈敏章部长逝世,在征得有关领导部门同意后,按照第七届药典委员会章程精神,经1999年12月第七届药典委员会常务委员会议一致同意调整 主任委员、副主任委员。
这届委员会设专业委员会共16个,分别为:中医专业委员会、中药第一专业委员会、中药第二专业委员会、中药第三专业委员会、中药第 四专业委员会、医学专业委员会、药品名词专业委员会、附录专业委员会、制剂专业委员会、药理专业委员会、化学药品第一专业委员会、化学药品第二专业委员会、抗生素专业委员会、生化药品专业委员会、放射品专业委员会、生物制品专业委员会。
1996年召开第七届药典委员会常务委员会第一次会议,通过了这届药典委员会提出的"《中国药典》2000年版设计方案",一部确立了"突出特 色,立足提高",二部确立了"赶超与国情相结合,先进与特色相结合"的指导思想。根据这届委员会提出的设计方案,1996年10月起,各专业委员会先后召 开会议,落实设计方案提出的任务并分工进行工作。?
1997年底,首先完成了附录与制剂通则的修改,并下发各起草单位征求意见。1998年底药典初稿完成,经进一步征求全国各有关方面的意见,至1999年10月底,先后召开了16个专业委员会审定稿会议。《中国药典》2000年版于 1999年12月经第七届药典委员会常务委员会议审议通过,报请国家药品监督管理局批准颁布,于 2000年 1月出版发行,2000年 7月 1日起正式执行。
2000年版药典共收载药品 2691种,其中一部收载 992种,二部收载1699种。一、二两部共新增品种399种,修订品种562种。这版药典的附录作了较大幅度的改进和提高,一部新增附录10个,修订附录31个;二部新增附录27个,修订附录32个。二部附录中首次收载了药品标准分析方法验证要求等六项指导原则,对统一、规范药品标准试验方法起指导作用。 现代分析技术在这版药典中得到进一步扩大应用。
第七届药典委员会还完成了《中国药典》1995年版一九九七年增补本、一九九八年增补本、《中国药品通用名称》(一九九八年增补本)及《药品红 外光谱集》(第二卷)、《临床用药须知》(第三版)。1997年完成了《中国药典》1995年版英文版。为加强国际合作与交流,第七届药典委员会还决定 《中国药典》2000年版英文版与中文版同步出版。
以往几版药典中的"剂量"、"注意"项内容,由于过于简单不能准确反映临床用药的实际情况,根据"《中国药典》2000年版设计方案"的提议,这版药典二部取消了这两项,其有关内容移至《中国药典》2000年版《临床用药须知》一书中。
2002年10月,经国家食品药品监督管理局批准,第八届药典委员会成立。由国家食品药品监督管理局聘请312位委员组成,不再设立名誉委员。原 常务委员会更名为执行委员会,由全体委员大会授权审定《中国药典》及国家药品标准的重大事项。
本届委员会设专业委员会共24个。在上一届委员会的基础上, 增设了民族药专业委员会(筹)、微生物专业委员会、药品包装材料与辅料专业委员会;原生物制品专业委员会扩增为血液制品专业委员会、病毒制品专业委员会、 细菌制品专业委员会、体细胞治疗与基因治疗专业委员会、重组制品专业委员会和体外诊断用生物试剂专业委员会。
2002年10月召开第八届药典委员会全体大会及执行委员会第一次会议,通过了本届药典委员会提出的"《中国药典》2005年版设计方案"。设 计方案明确了坚持继承与发展、理论与实际相结合的方针;确定了"科学、实用、规范"等药典编纂原则;决定将《中国生物制品规程》并入药典,设为药典三部; 并编制首部中成药《临床用药须知》。
2002年11月起,各专业委员会先后召开会议,安排设计方案提出的任务并分别进行工作。2003年7月,首先完成了附录草案,并发有关单位征 求意见。2004年初药典附录与品种初稿基本完成,增修订内容陆续在国家药典委员会网站上公示3个月,征求全国各有关方面的意见。
6月至8月,各专业委员 会相继召开了审定稿会议。9月,《中国药典》2005年版经过第八届药典委员会执行委员会议审议通过,12月报请国家食品药品监督管理局批准颁布,于 2005年1月出版发行,2005年7月1日起正式执行。
本版药典收载的品种有较大幅度的增加。共收载3212种,其中新增525种。药典一部收载品种1147种,其中新增154种、修订453种;药 典二部收载1964种,其中新增327种、修订522种;药典三部收载101种,其中新增44种、修订57种。《中国药典》2000年版收载而本版药典未 收载的品种共有9种;2000年版《中国生物制品规程》及2002年增补本收载而未收载入药典的品种共有123种。
本版药典收载的附录,药典一部为98个,其中新增12个、修订48个,删除1个;药典二部为137个,其中新增13个、修订65个、删除1个; 药典三部为140个,其中新增62个、修订78个,删除1个。一、二、三部共同采用的附录分别在各部中予以收载,并进行了协调统一。
本版药典在主任委员的积极倡导下,对药品的安全性问题更加重视。药典一部采用原子吸收和电感耦合等离子体质谱法增加了有害元素(铅、镉、砷、 汞、铜)测定法,并规定了有害元素的限度;药典一部还增加了中药注射剂安全性检查法应用指导原则。
药典二部有126个静脉注射剂增订了不溶性微粒检查,增修订细菌内毒素检查的品种达112种;残留溶剂测定法中引入国际间已协调统一的有关残留溶剂的限度要求,并有24种原料药增订了残留溶剂检查;药典二部还 增加了药品杂质分析指导原则、正电子类和锝[99mTc]放射品质量控制指导原则。
药典三部增订了逆转录酶活性检查法、人血白蛋白铝残留量测定法等, 牛血清白蛋白残留量及CHO细胞蛋白残留量等检测方法也得到改进。本版药典结合我国医药工业的现状和临床用药的实际情况,将由卫生部颁布的原《澄明度检查细则和判断标准》修订为"可见异物检查法",以加强注射剂等药品的用药安全。
本版药典坚持注重环保的一贯性原则,在品种中对苯等有害溶剂,尽可能采用其他溶剂替代。
本版药典根据中医辨证施治的理论,对收载的中成药标准项下的功能主治进行了科学规范,为准确理解中成药的功能主治及合理用药提供了保证,促进中医药在新时期的健康发展。
本版药典三部源于《中国生物制品规程》。自1951年以来,该规程已有六版颁布执行,分别为1951年及1952年修订版、1959年版、 1979年版、1990年版及1993年版(诊断制品类)、1995年版、2000年版及2002年增补版。2002年翻译出版了第一部英文版《中国生物 制品规程》(2000年版)。
第八届药典委员会还完成了《中国药典》2000年版2002年增补版、2004年增补版、《中国药品通用名称》(2005年版)及《药品红外光谱集》(第三卷)、《临床用药须知》(中成药第一版、化学药第四版)。
2005年,完成了《中国药典》2005年版英文版。为加强国际合作与交流,本届委员会期间,与美国药典委员会联合举办了首届中美药典论坛。
2010年版《药典》分一部、二部和三部,收载品种总计4567种,其中新增1386种。药典一部收载药材和饮片、植物油脂和提取物、成方制剂和单味制剂等,品种共计2165种;
其中新增1019种(包括439个饮片标准)、修订634种;药典二部收载化学药品、抗生素、生化药品、放射品以及药用辅料等,品种共计2271种,其中新增330种、修订1500种;药典三部收载生物制品,品种共计131种,其中新增37种、修订94种。
2010版药典收载的附录亦有变化,其中药典一部新增14个、修订47个;药典二部新增15个、修订69个;药典三部新增18个、修订39个。一、二、三部共同采用的附录分别在各部中予以收载,并尽可能做到统一协调、求同存异。
2015年版《药典》是新中国成立以来的第10版药典。2010年3月第十届药典委员会组建成立,历时5年完成新版药典编制工作。
2015年版《药典》收载品种总数达到5608个,比2010年版药典新增1082个。涵盖了基本药物、医疗保险目录品种和临床常用药品,更加适合于临床用药的需求。而且标准数量有了全面提升,特别是围绕安全性和有效性的控制项目,增加了检测项目。《药典》将于2015年12月1日起正式实施。
国家食品药品监督管理总局科技标准司司长于军介绍,《药典》是国家为保证药品质量可控、确保人民用药安全有效而依法制定的药品法典,是药品研制、生产、经营、使用和管理都必须严格遵守的法定依据,国家药品标准体系的核心。
于军表示,2015年版《药典》在历版药典的基础上,坚持保障公众用药安全的原则,在品种收载、检验方法完善、检测限度设定以及质量控制水平上都有了较大提升,重点加强药品安全性和有效性的控制要求,充分借鉴国际先进质量控制技术和经验,整体提升药典标准水平,全面反映我国当前医药发展和检测技术的水平,集中体现了当前我国药典标准的最新科研成果;
将在推动我国药品质量提高、加快企业技术进步和产品升级换代、促进我国医药产业结构调整、提升《药典》权威性和国际影响力等方面发挥重要作用。2015年版《药典》收载品种总数达到5608个,比2010年版药典新增1082个。本版《药典》的一个重要变化将一部、二部、三部的附录进行了整合,增设为药典第四部,使得《药典》分类更加清晰明确。
"新版《药典》发布后,总局将重点开展新版药典的宣传培训工作。培训工作计划已制定完成,药典委将有计划、有针对性地组织药典委员会专家,对新版《药典》在技术要求、质量控制理念等多个方面展开培训,使众多药品生产经营企业、药品检验机构以及其他药典使用单位和人员充分了解和掌握新版《药典》的主要变化和技术要求,确保新版《药典》顺利实施。" 于军强调。
主要作用
作为我国保证药品质量的法典,本版药典在保持科学性、先进性、规范性和权威性的基础上,着力解决制约药品质量与安全的突出问题,着力提高药品标准质量控制水平,充分借鉴了国际先进技术和经验,客观反映了中国当前医药工业、临床用药及检验技术的水平,必将在提高药品质量过程中起到积极而重要的作用,并将进一步扩大和提升我国药典在国际上的积极影响。
凡中国药典收载的品种,自执行之日起,原收载于历版药典、卫生部颁布药品标准、国家食品药品监督管理局颁布新药转正标准和地方标准上升国家标准的同品种药品标准同时废止。
药品注册标准不符合中国药典有关要求的,药品生产企业应按《药品注册管理办法》的有关规定提出补充申请。对于药品注册标准中收载的检验项目多于中国药典规定的或质量指标高于中国药典要求的,在执行中国药典的基础上,应同时执行原标准的相应项目和指标。
中国药典品种项下未收载的制剂规格,其质量标准按中国药典同品种相关要求执行,规格项按原批准证明
药用辅料是不是用于药品GMP标准
1.原料药质量标准的确定
原料药的质量标准确定一般程序,这里将它分为三大阶段:合成工艺待确定期,合成工艺确定期,稳定性试验考察期。
1.1 合成工艺待确定期
一个原料药首先由药物合成部进行合成工艺的确定,在其进行工艺确定期间,就已经与药分部门有了密切的联系。
协助合成部门的工作:帮助确定反应步骤的终点控制、反应产物的纯度监控,所能提供的分析方法可能有薄层色谱、液相色谱或熔点等。
做好自己的准备工作:通过各种途径搜集查阅有关该药品的各方面信息,比如该药的理化性质(性状、溶解度、熔点、旋光性质、紫外光谱、鉴别方法等)、检查项(一般杂质检查、有关物质检查)、含量测定方法和该药物的稳定性等等。
1.2 合成工艺确定期
合成工艺路线打通后,合成部门将会提供试制的三批样品(已确定该药物结构)供分析部门质量研究及稳定性试验用,一般来说,所提供三批样品应该是成熟的工艺条件,以一定规模制备得到样品,此时我们的质量研究工作正式开始。
1.2.1 质量研究工作
理化常数:性状(外观、臭、味)、溶解度、熔点、比旋度、紫外吸收系数
鉴别:化学法、色谱法、光谱法
检查:酸碱度、溶液澄清度与颜色、干燥失重或水分、炽灼残渣、重金属、无机盐、无菌、热原或细菌内毒素、有机溶剂残留 、有关物质
含量测定:容量法、光谱法、色谱法
1.2.2 质量研究试验顺序安排
1.3 稳定性试验考察期
按照中国药典稳定性研究指导原则规定,我们的稳定性研究包括三大部分—影响因素试验、加速试验和长期留样试验。
考察项目:样品性状、有关物质和含量这三项必须考察(对于某些特殊药物可能无法考察有关物质),另外诸如:熔点(若质量标准中规定了熔点检查,或能测出准确熔点且熔点低于250℃的样品,稳定性研究中必须对其检查)、溶液颜色与澄清度(若为供注射用原料,稳定性研究中必须对其检查)、ph值(若为供注射用原料,稳定性研究中必须对其检查)等项目则根据各药物的性质而具体制定。
上面将原料药分析工作分三大块做了简单讨论,文中所讲的多是实际试验的简单思路和一些注意事项,但对于新药研究这样一个很严肃的工作有很多法定性的规定内容在文中并未详细说明,在《中国药典2000年版二部》和《新药质量研究与质量标准指导原则》中有详细的说明。
2.药物溶解度试验
1.试验溶剂的选择可参考有关文献制定,若无文献一般选择常用的水相溶剂(水、酸、碱溶液)和有机溶剂(甲醇、乙醇、乙腈、、丙酮、氯仿、冰醋酸、dmf、dmso)。
2.若按照中国药典要求的做法将用去大量的原料和溶剂一般我们都按倍数减量试验,但在做极易溶解或易溶时因溶剂量较小可适当放大原料量试验。
3.药物稳定性试验
药物的有关物质检查:它是药物质量的重要指标之一,包括未反应完全的化学原料、合成副产物和药品贮存过程中产生的降解物两部分,检查方法首选hplc检查,该方法亦是现在最常用的的有关物质检查方法,若该药物无紫外吸收则考虑用tlc检查。
细菌内毒素检查将处理好的样品应放置
药用辅料生产质量管理规范
目 录
第一章 总则
第二章 机构、人员和职责
第三章 厂房和设施
第四章 设备
第五章 物料
第六章 卫生
第七章 验证
第八章 文件
第九章 生产管理
第十章 质量保证和质量控制
第十一章 销售
第十二章 自检和改进
第十三章 附则
第一章 总 则
第一条 根据《中华人民共和国药品管理法》第十一条“生产药品所需的原料、辅料必须符合药用要求”的规定,制定本规范。
第二条 本规范旨在确定药用辅料(以下简称辅料)生产企业实施质量管理的基本范围和要点,以确保辅料具备应有的质量和安全性,并符合使用要求。
第三条 辅料生产的质量管理要求随工艺步骤的后移逐步提高,企业应根据辅料的生产工艺和产品的性质,确定执行规范的起始步骤。
第二章 机构、人员和职责
第四条 企业应设置与辅料生产相适应的组织机构,并以文件形式明确质量保证、质量控制、生产、物料、维修和工程等部门及人员的岗位职责。
第五条 质量管理部门应独立于生产管理部门,有权批准或拒收原料、包装材料、中间体和成品;有权审查生产记录,以确保没有发生差错或对发生的差错已作了必要的查处;有权参与审查批准生产工艺、偏差和投诉调查、质量标准、规程与检验方法的变更等。
第六条 质量管理负责人负责本规范的执行,定期向企业负责人报告质量体系运行情况、客户要求以及相关法规的变化情况等。企业负责人应定期评审质量体系以确保符合本规范的要求。
第七条 企业应配备一定数量的与辅料生产相适应的管理人员和技术人员。从事辅料生产的各级人员应具有与其职责相适应的受教育程度并经过培训考核,以满足辅料生产的需要。
第八条 企业应建立并执行培训规程。培训应包括相应的专业技术知识、岗位操作规程、卫生知识及本规范等内容。应由具备适当资质的人员进行足够频次的培训,以确保员工熟悉本规范的要求。培训应有相应的记录。
第三章 厂房和设施
第九条 企业应有整洁的生产环境,厂区的地面、路面及运输等不应对辅料的生产造成污染。
第十条 应根据辅料的用途和特点确定对生产厂房和设施的洁净控制要求。辅料生产、包装、检验和储存所用的厂房和设施应便于清洁、维修和保养,以保持良好的状态。
第十一条 生产区和贮存区应有与生产规模相适应的面积和空间,以合理放置设备、器具和物料,便于生产操作,并最大限度地减少差错和交叉污染。
第十二条 空气处理系统的设计应能防止交叉污染,对产尘量大、易产生交叉污染的区域不应利用回风。
第十三条 应根据产品的性质和工艺要求设定和控制温度和湿度。
第十四条 厂房应能防止鼠类、鸟类、昆虫和其它动物的侵扰。应采用必要的措施防止原料在厂区内发生污染或控制污染。厂房应根据工艺要求设必要的防尘及捕尘设施。
第十五条 所有的区域都应有适当的照明,并按规定设置应急照明。
第十六条 生产操作区地漏的设置应与生产要求相适应,并采用液封或其它装置防止倒吸和污染。
第十七条 生产人员和物料出入生产车间,应有防止交叉污染的措施。应配备适当的盥洗设施以方便生产区员工使用。
第四章 设 备
第十八条 辅料生产、包装、检验和储存的设备,其设计、安装应有利于操作、清洁、保养。设备的设计应能将操作人员直接接触所导致的污染降低到最低程度。封闭的设备和管道可安装在室外。
第十九条 生产用设备与物料接触的表面应光滑、平整,不与物料起化学反应、不发生吸附或吸着作用,易于清洗或灭菌 。
第二十条 对残留物难以清洗的辅料,应使用专用生产设备。
第二十一条 应采取措施避免设备运行所需的润滑剂或冷却剂与原料、包装材料、中间体或辅料成品直接接触,不可避免时,所用润滑剂或冷却剂至少应符合食用要求。
第二十二条 应标明与设备连接主要固定管道内物料的名称和流向。
第二十三条 企业应有定期校验关键仪器设备的计划和规程。应根据计划和规程对关键的计量、监测设备,包括实验室测试仪器以及中间控制仪器进行校验。达不到设定标准的仪器和设备不得使用。校验标准应能溯源至法定标准。
第二十四条 应建立并执行辅料生产、包装、检验、储存所用关键设备(包括工器具)的维修保养规程。维修保养记录至少应包括以下内容:
1.维修保养的详细说明及实施维修人员。
2.设备维修保养前后生产的品种和批号。
第二十五条 水处理及其配套系统的设计、安装和维护应能确保供水达到设定的标准。
第五章 物 料
第二十六条 应检查、评估供应商的综合能力,确保原料、包装材料以及服务满足合同的要求。
第二十七条 应制定辅料生产所用物料购入、储存、发放、使用等管理制度。物料应有质量标准,企业应按质量标准对物料进行检验,并审核供应商的检验报告,以确保物料的规格和质量满足辅料生产的质量要求。
第二十八条 成品和对成品质量有影响的关键物料应有明确的标识,以便通过文件系统对其进行追溯。质量体系应保证辅料产品的双向可追溯性。应能运用批/编号系统或其他途径,借助原料的标识(名称、编号)对辅料生产过程中所使用的原料追溯查询。对连续法生产所用的原料,应明确一定数量的原料作为一个批并给定具体批号。难以精确按批号分开的大批量、大容量原料、溶媒等物料入库时应编号, 其收、发、 存、用应有相应的管理制度。
第二十九条 应建立确定原料、包装材料、中间体和成品等检验状态的管理系统。待验、合格、不合格物料和成品等应合理存放于有明显标志的区域,并有明确标示状态的标记。不合格物料应有效隔离,批准放行前不得使用。
第三十条 成品标签必须符合有关法规的要求,标签应有名称、级别、批号、生产企业等内容。
第三十一条 成品、中间体和原料应在合适的温度、湿度和光线条件下处理和存放。易燃易爆和其它危险品的贮存应严格执行国家有关的规定。
第三十二条 生产药用明胶或其它辅料所用的动物组织或植物,应有文件或记录表明其没有受过有害化学物质的污染,如要求供应商提供卫生检疫部门的动物健康证明或其他检疫、检验证明材料。
第三十三条 使用菌种生产辅料的企业, 应建立菌种鉴定、保管、使用、储存、复壮、筛选等管理制度, 并有相应记录。
第六章 卫 生
第三十四条 应有防止污染的卫生措施, 并制定卫生管理制度。
第三十五条 生产、检验和仓储区域应保持清洁卫生。应按生产和空气洁净控制要求制定厂房、设备、容器具等的清洁规程, 内容包括清洁方法、程序、间隔时间、使用的清洁剂或消毒剂、清洁工具的清洁方法和存放地点等。
第三十六条 生产区不得存放非生产物品和个人杂物。生产中的废弃物应及时处理。
第三十七条 更衣室、浴室及厕所的设置不得对生产区域造成污染。
第三十八条 应建立有效的清洁制度以清除产品残留物和污染物,设备清洁的状态应有适当标识并有记录。
第三十九条 生产、检验、维修和仓储岗位的人员应穿着与其工作相适应的清洁工作服,不应佩戴首饰。工作服应不产生静电、不脱落异物。洁净区仅限于该区生产操作人员和经批准人员进入。
第四十条 应每年对生产人员进行体检, 并建立健康档案。当人员所患疾病或外部伤口可能对辅料的安全和质量带来不利影响时,应将其调离与原料、包装材料、中间体和成品直接接触的岗位。各级人员均应保持良好的卫生习惯,当自身健康状况有可能对产品造成不利影响时,应主动向主管人员报告。
第七章 验 证
第四十一条 应根据被验证对象制定验证方案,明确验证的项目、方法和合格标准,并按验证计划实施验证。验证完成后应写出验证报告,由验证负责人审核、批准。
第四十二条 应对生产厂房、设施及设备进行设计确认、安装确认、运行确认、性能确认。
第四十三条 工艺验证是实现质量保证目标的关键。应在工艺验证文件中阐明反应过程、工艺控制参数、取样以及中间测试要求,为工艺验证的顺利进行奠定基础。当影响产品质量的主要因素,如工艺、质量控制方法、主要原辅料、主要生产设备等发生改变时,应进行再验证。
第四十四条 清洁验证应能以数据资料证明主要设备、容器清洁消毒规程的有效性。如采用具有代表性产品的清洁模式制定清洁消毒规程,应保证清洁消毒满足产品和工艺的特定要求。
第四十五条 验证过程中获得的数据和资料应以文件形式归档保存。验证文件应包括验证总计划、验证方案、验证报告和验证总结。验证方案或报告中应清楚阐述被验证的对象/系统、需验证的项目、合格标准、结果评价、参考文献、建议、偏差和漏项、方案、结果审批等方面的内容。
第八章 文 件
第四十六条 应建立符合质量管理要求的文件管理系统,并制定、执行有关受控文件的标识、起草、复核、发放、归档、变更、过期文件收回处理的规程。
第四十七条 应建立并执行生产和质量控制的书面规程。规程的批准、修改和分发应加以控制,以确保生产全过程所使用的规程均为现行版本。所有文件的制订及修改须经指定人员审核、批准后按规定的范围发放。应有制度以确保文件正确发放并收回以前的版本。
第四十八条 受控文件应具有专一性的编号,注明发放日期,并标明版本号。应由指定的部门发放文件,所有文件的变更以及变更原因应有记录。
第四十九条 产品的所有记录应清晰易读。批相关的所有记录至少应保留至产品有效期后的一年。记录档案应便于追溯查询,其存档环境应符合有关规定。
第五十条 连续工艺生产或按批生产的产品均应有生产和质量控制记录,以记录每批产品生产和质量控制相关的所有信息。记录可存放在不同的场所,但应方便查询。记录通常包括以下二类:
1.指令性文件,即发至生产车间的批生产指令或控制文件原稿的复印件。
2.记录性文件,即完成批生产、包装或暂存等重要操作步骤获得的记录。文件的内容应包括:
(1)各操作步骤完成的日期/时间;
(2)所用主要设备和生产线的编号;
(3)每批原料或中间体的品名、编号或批号;
(4)生产过程中所用原料的数量(重量或其它计量单位);
(5)中间控制或实验室控制的结果;
(6)包装和贴签区使用前后的清场记录;
(7)某些加工步骤实际收率或产量的说明以及理论收率的百分数;
(8)标签控制记录,并尽可能附上所有使用标签的实样;
(9)包装材料、容器或密封件的详细说明;
(10)对取样过程的详细描述;
(11)生产重要步骤操作、复核、监督人员的签名;
(12)偏差查处记录;
(13)最终产品检验记录;
(14)以无菌操作方式生产药用辅料时,应有无菌操作区关键点环境监测的记录。
第五十一条 批生产记录应字迹清晰、内容真实、数据完整,并有操作人和复核人签名。记录应保持整洁,不得撕毁和任意涂改,如需更改,应在更改处签名,并保持原数据仍可辨认。
第九章 生产管理
第五十二条 企业应确保重要的生产过程能够连续稳定地运行。
第五十三条 每批产品生产应进行物料平衡检查。如有显著差异,必须查明原因。在得出合理解释、确认无潜在质量偏差后,方可按正常产品处理。
第五十四条 如在同一厂房或用同一台设备生产不同级别的同种产品,在不改变质量、安全的情况下,允许前一批的少量产品带至下一批中。
第五十五条 生产过程中需要暴露的产品应置于清洁的环境中,必要时应对生产环境进行监测,以避免微生物污染或因产品暴露在热、空气和光等条件下引起质量变化。直接接触产品的惰性气体应按原料要求管理。
第五十六条 无菌药品用辅料的生产环境应与制剂的生产环境相似,并制定相应的环境监测规程。无菌辅料灭菌后的操作必须使用无菌操作技术,无菌生产过程中有关灭菌及无菌操作区环境监控的结果,应纳入批生产记录中,并作为最终产品质量评估的重要依据。
第五十七条 生产过程中的工艺用水应符合产品工艺要求。一般情况下,工艺用水应符合饮用水质量标准。当产品工艺对水质有更高要求时,企业应建立包括理化特性、细菌总数、不可检出微生物等的标准。如由企业自行处理工艺用水使其达到标准,应对水处理工艺进行验证,并对系统的运行进行监控。如企业生产的非无菌辅料用于生产无菌药品,应对辅料最终分离和精制的工艺用水进行监测,同时应控制细菌总数及内毒素。
第五十八条 如企业采用加热或辐射的方式来减少非无菌辅料微生物污染时,辅料在灭菌前应达到规定的微生物限度标准,且灭菌工艺处于受控状态。应对采用的灭菌方法进行验证,以证明达到设定的要求。不应将辅料产品的最终灭菌替代工艺过程的微生物控制。
第五十九条 对储存条件有特殊要求(如避光和隔热等)的辅料,应在其包装上注明。
第六十条 回收溶剂在同一或不同的工艺步骤中使用时,必须符合回收使用或与其它溶剂混用的标准。
第六十一条 需反复使用的母液以及含有可回收辅料、反应物或中间体的滤液, 应符合投料的标准。批生产记录中应有符合回收规程的回收记录。
第六十二条 应根据工艺监控的需要进行中间检查和检测,或在指定操作点及规定的时间对实际样品进行检测,检测结果应符合设定的工艺参数或在规定限度以内。应根据中间体检测的结果来判断工艺过程是否正常运行。不合格的中间产品不得流入下道工序。
第六十三条 每批辅料都应编制生产批号。批的划分原则如下:
1.连续生产的辅料,指在一定时间间隔内生产的质量和特性符合规定限度的均质产品。
2.间歇生产的辅料,由一定数量的产品经最后的混合所得的质量和特性符合规定限度的均质产品。
第六十四条 为确保批的均一性或方便加工,可以进行中间混合,应对混合过程进行适当的控制并有记录。批与批之间应有重现性。不合格批号与合格批号的辅料不得相互混合。
第六十五条 更换品种时,必须对设备进行彻底的清洁。同品种生产中更换批次时,应清场并有记录。可允许批生产中物料零头的结转。在残留物影响产品质量情况下,应在更换批次时,对设备进行彻底的清洁。
第六十六条 应规定辅料生产各工艺步骤的完成时间和间隔时间。此外,还应规定直接接触产品的设备、容器、包装材料和其它物品的清洗、干燥、灭菌到使用的最长间隔时间。
第六十七条 包装过程应确保辅料的质量和纯度不受影响,并确保所有包装容器贴签正确无误。应有防止包装和贴签操作发生差错的措施。如辅料容器可回收并重复使用,原标签必须清除或涂销。同一辅料生产中使用的周转容器上所有以前的批号或标签也应清除或涂销。
第六十八条 辅料的包装系统应具备下列条件:
1.包装相关的规格/标准的文件、检查或测试方法以及清洁规程(如有此要求时)。
2.封签或其它识别包装是否被开启的安全措施。
3.容器封口性能作过评估,证明封口系统能保护辅料不变质、不受污染。
4.已建立储运和处理规程,能保护容器及封口,减少污染、减少损坏和变质、避免混批。
第六十九条 应制订并执行有关规程,以确保印制、发放的标签数量正确,标签内容准确无误。应有书面规程规定多余的标签及时得到销毁或退还专用标签储存区。已打印批号的多余标签应予销毁。包装和贴签设备在使用前应进行检查,以确保与下一批号无关的所有物料均已清除。无论是在辅料包装线上贴签,还是使用事先印制好的包装袋包装,或用槽车运送,均应建立完整的文件和记录系统,以满足上述有关要求。
第七十条 应对所有不合格批进行调查,查明原因并有调查记录。应采取措施防止类似问题再次发生。应建立不合格品的评估及处理规程,并按规程对不合格产品审查,并确定不合格品的最终处理方案。处理方案通常包括:
1.通过返工达到标准。
2.改变其使用级别。
3.销毁。
第七十一条 辅料产品可以进行返工或再加工,但须遵循返工和再加工的规程。不允许只依靠最终检验来判断返工产品是否符合标准,应对返工或再加工过程进行调查和评估。
为保证返工产品符合设定的标准、规格和特性,应对返工后物料的质量进行评估并有完整记录。应有充分的调查、评估及记录证明返工后产品的质量至少等同于其它合格产品,且造成返工辅料不合格的原因并非工艺缺陷。
返工或再加工过程不属正常生产过程,因此,未经质量部门审批准,不得进行返工。
第七十二条 使用自动化控制系统或其它复杂设备时,应符合下列要求:
1.系统与规程能证明设备及软件性能达到设定要求。
2.已建立并遵循定期检查、校验设备的规程。
3.有适当的保留程序和记录的备份系统。
4.确保只有被授权人员才能修改控制程序;程序的修改应通过验证并有记录。
第十章 质量保证和质量控制
第七十三条 质量管理部门应负责辅料生产全过程的质量管理和检验。质量管理部门应配备一定数量的质量管理人员和检验人员, 并有与辅料生产规模、品种、检验要求相适应的场所、仪器和设备。
第七十四条 质量管理部门应有为确保产品符合法定或企业内控质量标准所作检验的完整记录,具体包括:
1.对检品的详细描述,包括物料名称、批/编号或其它专一性的代号以及取样时间。
2.每一检验方法的索引号(或说明)。
3.物料和产品检测原始数据,包括图、表以及仪器检测图谱。
4.与检验相关的计算。
5.检验结果及与标准比较的结论。
6.检验人员的签字及测试日期。
第七十五条 应有试剂和试液采购、制备的书面规程。购进的试剂和试液应标明名称、浓度、有效期。试液制备的记录应予保存,包括产品名称、制备时间和所使用材料的数量等。容量分析用试液应按法定标准进行标定,标定的记录应予保留。
第七十六条 为确保原料、中间体、成品等符合有关标准要求,检验方案应包括质量标准、取样规程以及检验规程等。
第七十七条 成品应由质量管理部门检验并应符合标准。成品放行前,所有生产文件和记录,包括测试数据均应经质量管理部门审查并符合要求。不合格产品不得放行出厂。
第七十八条 检验结果如不符合标准要求,必须按照书面规程进行调查并有记录。除非查明原检验结果有误,否则不得对样品进行复检并只根据复检结果合格放行产品,而应采用所有检验数据的统计学结果,包括原检验结果和复检的数据,来确定该批产品能否放行。当怀疑检品不具备代表性时,可采用同样的原则处理。
第七十九条 留样应保存至使用期限后一年,留样量应不少于全检量的二倍。
第八十条 辅料留样的稳定性考察应有文件和记录。应按稳定性考察计划定期进行测试。计划通常包括以下内容:
1.每年考察的批数,样品的数量以及考察的间隔时间。
2.留样的储存条件。
3.稳定性考察所采用的测试方法。
4.如有可能,稳定性考察样品所用的容器及贮存时间应与销售产品相同。
第八十一条 应建立有关规程,以便对原料采购、质量标准/规格、设备以及生产工艺等方面的各种变更进行鉴别、分类、记录、审查和批准。应由质量管理部门和负责产品注册的部门一起负责最终批准变更。重要操作的变更应有验证结果支持。应在企业内部以及企业与用户之间就变更的影响进行必要的沟通。
第十一章 销 售
第八十二条 应保存辅料的销售记录。记录应包括辅料名称、批号、发送地点、收货人、发运量、发货日期等信息,以便必要时收回产品。
第八十三条 应有辅料退货的保管、处理、检验和再加工的书面规程并遵照执行。对退回辅料应作好退货标识并将其置于待处理状态。如产品暂存、贮存、发运及退货过程中的各种条件影响了产品的安全性、质量或纯度,应将产品作报废处理。应作好退货记录并予保存,记录内容应包括产品名称、批号、退货原因、退货数量、处理结果和处置日期等信息。
第十二章 自检和改进
第八十四条 企业应定期组织自检,以检查质量活动是否按计划进行并确定质量管理体系的有效性。应按照自检规程进行自检并跟踪自检结果。应与被检查部门的负责人一起对自检结果进行讨论,被检查部门应针对存在的问题及时采取措施予以改进。
第八十五条 应通过客户投诉、产品质量回顾、工艺能力研究、自查和客户审计等方面的信息寻找质量体系的薄弱环节并制订相应的改进措施。
第八十六条 应定期对产品质量指标、客户投诉内容、工艺运行参数、工艺故障等进行回顾总结,确定质量体系改进的方向。
第八十七条 企业应建立并执行以下规程:
1.调查产品不合格、退货、用户投诉并有防止此类问题再次发生而采取必要措施的规程。
2.分析工艺、生产操作、偏差、质量记录和维修报告以查找并消除导致产品不合格潜在因素的规程。
3.采取预防措施,及时处理可能导致质量风险的各种问题的规程。
4.采用适当管理手段,确保纠偏计划有效实施的规程。
5.采取纠偏措施后及时对规程进行必要的修改和审批的规程。
第十三章 附 则
第八十八条 本规范下列用语的含义是:
批(Batch/lot): 采用一个或一系列加工过程生产出的一定数量的质量和特性符合规定限度的均质原料、中间体、包装材料或最终产品。在连续工艺条件下,一批可以是指生产中质量和特性符合规定限度的特定的一段。批量也可以是一个固定的数量或是在一个固定的时间段内的生产量。
批号(Batch Number, Lot number): 用以确定一个批次生产、加工、包装、编码和分发历史全过程的具有专一性的数字、字母/或符号的组合。
受控文件(Controlled documents): 质量体系的组成部分,即为保证质量体系的有效运行,由质量部门批准颁发需企业各部门遵照执行的文件。
批生产工艺 (Batch Process): 指从辅料的各种起始原料生产药用辅料的制造过程。
批记录(Batch records): 记述从原料阶段到该批完成的整个历史文件和记录。
预防性维修保养 (Preventive maintenance): 即计划性维修,指根据设备的特点和运行情况,为防止设备运行过程中出现故障而定期进行的维修保养活动。
混入(Commingling): 通常指批交替生产或连续工艺法中一个等级或一个批号剩余的少量物料与另一个等级或另一个批号的混合。
连续法工艺(Continuous Process): 一种连续供料生产物料的制造工艺。
关键工艺(Critical Process): 直接影响产品质量特征的生产工艺步骤。
交叉污染(Cross-Contamination): 生产过程中一种原料、中间产品或辅料产品对另一种原料、中间体或辅料产品的污染。
客户(customers): 包括用户、中间商、代理商和药用辅料供应链中的其他组织。
均一性物料(Homogeneous Material): 整个一批组份、密度/定量特性均匀一致的物料。
典型产品(Model Product): 在组份、功效或质量标准/规格上能代表某一组同类产品的产品。
返工(Reprocessing): 将以前加工过但不符合标准或规格的物料返回至原工艺过程,并重复常规生产的一步或几步必要的步骤。
再加工(Reworking): 将以前加工过但不符合标准或规格的物料用与原工艺不同的加工步骤进行加工处理。
标准操作规程(Standard Operating Procedures): 经过批准用于执行某一特定操作的书面规程。
验证(Validation): 一个能确保某项特定工艺、方法、或系统始终如一产生满足预定标准的书面计划和规程。
验证负责人(the person in charge of validation): 由企业指定负责验证工作的人员。验证负责人可以是项目中负责验证的人员,也可以是企业质量部门中主管验证的人员或质量部门的负责人。
供应商(Supplier): 按合同提供原料或提供一种或多种服务的组织。
中华人民共和国药典几年编一次
菌内毒素检查法作为控制药品质量的一种有效方法,已经广泛的被世界各国药典收载。经过30多年的不断改进,无论是凝胶法还是光度法均比较成熟和完善。但是,在为新化合物或新药建立细菌内毒素检查方法时,常常会遇到各种各样的困难,尤其是尚处于新药研发早期阶段的药物,由于药物制剂、赋形剂等还不稳定,经常会发生变化,这样就给方法的建立带来不同程度的影响。在建立细菌内毒素检查法之前,应尽可能多的收集有关该药品的基本信息,例如:有关样品的溶解性信息,推荐的稀释液,在水中的溶解度,以及最适溶剂;样品的pH范围;分子量大小;产品规格、体积或重量;拟用于临床的用法和用量等等。以便选择合适的样品处理方法和内毒素检查方法,对于早期研发阶段的药物,应选择合适的赋形剂,以有利于细菌内毒素检查中对样品的稀释处理。此外,在确定内毒素限值时还应尽可能采用最大人拟用剂量,为临床安全性和有效性研究中增加剂量留出空间。
一、细菌内毒素检查方法建立的主要步骤
对某一新化合物建立细菌内毒素检查方法时,首先应根据人体最大日给药剂量和给药途径,计算和确定样品的内毒素限值,选择合适的鲎试剂,根据临床规格,计算最大有效稀释倍数,稀释产品,并在低于最大稀释倍数的浓度下进行检查。可以采用凝胶法,也可以采用终点法或动态法。当测定结果有争议时,除另有规定外,以凝胶法为准。
1、细菌内毒素限值的确定
一个药品在投放市场前,它是否满足内毒素限值的要求?样品的内毒素含量具体是多少?这些问题不但关注用药安全,还应该最大限度的提供有关内毒素含量的准确信息,为药品生产过程中质量控制提供警戒信息。尽管细菌内毒素检查方法的建立是一个科学方法的研究过程,但其最终目的还是要为控制药品质量服务。因此,在方法建立时,不但要阐明限值的合理性,考虑技术可能达到的限值,同时还要满足相关药品管理法规的要求。
研究人员在建立方法的早期,一般会按照临床建议的最大人用剂量确定一个非正式的限值,这个限值可以根据实验室可以达到的最低检测水平,把限值订的相对比较严格,但往往由于早期的临床剂量会比最终上市的临床剂量高几倍,所以严格的限值,可能会使得正式生产时很多产品不能通过检查,从而造成不必要的浪费;因此参按照法规允许的最高水平,酌情确定样品的限值。
样品内毒素限值的确定一般与临床人体最大给药剂量有关,剂量越大,单位重量或体积的内毒素限值越低。一般按以下公式计算:内毒素限值L=K/M。式中内毒素限值L是以EU/ml、EU/mg或EU/u表示;K为按规定的给药途径,人体每公斤体重每小时最大可耐受的内毒素剂量,以EU/(kg.h)表示,注射剂K=5EU/(kg.h),其中放射品注射剂K=2.5EU/(kg.h),鞘内用注射剂K=0.2EU/(kg.h)。一般我国人群平均体重按60kg计算,人体对细菌内毒素的最大耐受量为300EU/h;另我国人体的平均体表面积按1.55m2计算,人体每平方米的最大耐受剂量为(300EU/h)/ 1.55m2 =(193EU/h)/ m2 。 M为人体每公斤体重每小时接受的最大给药剂量,以ml/(kg.h)、mg/(kg.h)或u/(kg.h)表示。
内毒素限值计算举例(一):A注射剂的人体最大用量为每小时1.5g,每公斤每小时体重的剂量为1.5g/60kg=0.025g/kg=25mg/kg,内毒素限值L=K/M=(5EU/kg)/( 25mg/kg ) = 0.2EU/mg。在细菌内毒素检查法中,细菌内毒素标准品和鲎试剂常常以EU/ml表示,所以在具体实验中样品的内毒素的限量可以转换为EU/ml的表示方法,可使实验操作计算更为方便。假定产品A的浓度为100mg/ml(或原料药经溶解后的浓度为100mg/ml), 那么,将产品A的限值从EU/mg转变为EU/ml时,内毒素限值L= 0.2 EU/mg 100 mg/ml = 20 EU/ml。
内毒素限值计算举例(二):B注射剂的临床最大用药剂量为1g/m2,规格为50mg/ml,内毒素限值L=(193 EU/ m2)/(1g/m2)=193 EU/g=0.193 EU/mg,转换为EU/ml 表示时,L = 0.193 EU/mg50 mg/ml=9.65EU/ml
细菌内毒素不同实验条件对结果的影响
1949 年10 月1 日中华人民共和国成立后,党和政府十分关怀人民的医药卫生保健工作,当年11 月卫生部召集在京有关医药专家研讨编纂药典问题。1950 年1 月卫生部从上海调药学专家孟目的教授负责组建中国药典编纂委员会和处理日常工作的干事会,筹划编制新中国药典。
1950 年4 月在上海召开药典工作座谈会,讨论药典的收载品种原则和建议收载的品种,并根据卫生部指示,提出新中国药典要结合国情,编出一部具有民族化、科学化、大众化的药典。随后,卫生部聘请药典委员49 人,分设名词、化学药、制剂、植物药、生物制品、动物药、药理、剂量8 个小组,另聘请通讯委员35 人,成立了第一届中国药典编纂委员会。卫生部部长李德全任主任委员。
1951 年4 月24 日至28 日在北京召开第一届中国药典编纂委员会第一次全体会议,会议对药典的名称、收载品种、专用名词、度量衡问题以及格式排列等作出决定。干事会根据全会讨论的意见,对药典草案进行修订,草案于1952 年底报卫生部核转政务院文教委员会批准后,第一部《中国药典》 1953 年版由卫生部编印发行。
1953 年版药典共收载药品531 种,其中化学药215 种,植物药与油脂类65 种,动物药13 种,抗生素2 种,生物制品25 种,各类制剂211 种。药典出版后,于1957 年出版《中国药典》 1953 年版第一增补本。1955 年卫生部成立第二届药典委员会,聘请委员49 人,通讯委员68 人,但这届委员会因故未能进行工作。1957 年成立第三届药典委员会,聘请委员80 人,药学专家汤腾汉教授为这届委员会主任委员(不设通讯委员),同年7 月28 日至8 月5日在北京召开第一次全体委员会议,卫生部李德全部长作了药典工作报告,特别指出第一版中国药典没有收载广大人民习用的中药,是个很大的缺陷。会议在总结工作的基础上,通过了制订药典的原则,讨论了药典的性质和作用,并修改了委员会章程,会议一致认为应把合乎条件的中药收载到药典中。8 月27日卫生部批准委员会分设药理与医学、化学药品、药剂、生化药品、生药、生物制品六个专门委员会及名词小组,药典委员会设常务委员会,日常工作机构改称秘书室。1958 年经常务委员会研究并经卫生部批准,增聘中医专家8 人、中药专家3 人组成中医药专门委员会,组织有关省市的中医药专家,根据传统中医药的理论和经验,起草中药材和中药成方(即中成药)的标准。
1959 年6 月25 日至7 月5日在北京召开这届委员会第二次全体会议,会议主要审议新版药典草稿,并确定收载品种。草稿经修订补充后,分别由各专门委员会审定,于1962 年完成送审稿,报请批准后付印,1965 年1 月26 日卫生部公布《中国药典》 1963 年版,并发出通知和施行办法。
1963 年版药典共收载药品1310种,分一、二两部,各有凡例和有关的附录。一部收载中医常用的中药材446 种和中药成方制剂197 种;二部收载化学药品667 种。此外,一部记载药品的“功能与主治”,二部增加了药品的“作用与用途”。
1966 年由于“”影响,药典委员会工作陷于停顿。1972 年4 月28 日批复卫生部“同意恢复药典委员会,四部(卫生部、燃料化学工业部、商业部、解放军总后卫生部)参加,胜生部牵头”。据此,同年5 月31 日至6 月10日在北京召开了编制国家新药典工作会议,出席会议的有全国各省(自治区、直辖市)的药品检验、药政管理以及有关.单位代表共88 人。这次会议着重讨论了编制药典的指导思想、方法、任务和要求,交流了工作经验,确定了编制新药典的方案,并分工落实起草任务。1973 年4 月,在北京召开第二次全国药典工作会议,讨论制订药典的一些原则要求,以及中西药品的标准样稿和起草说明书,并根据药材主产地和药品生产情况,调整了起草任务。1979 年10 月4 日卫生部颁布《中国药典》 1977 年版自1980 年1 月1 日起执行。1977 年版药典共收载药品1925 种。一部收载中草药材(包括少数民族药材)、中草药提取物、植物油脂以及一些单味药材制剂等882 种,成方制剂(包括少数民族药成方)270 种,共1 152 种;二部收载化学药品、生物制品等773 种。
1979 年,由卫生部聘请委员112 人组建第四届药典委员会,卫生部部长钱信忠兼任主任委员。同年11月22 日至28 日在北京召开这届第一次全体委员会议,会议讨论修改了委员会章程、药品标准工作管理办法及工作计划。委员会分设:中医、中药、医学与药理、化学药、生化药、药剂、抗生素、生物制品、放射品及名词10 个专业组。由有关专业组分别推荐新药典收载的品种,中医专业组负责审查拟定一部收载的品种范围;医学与药理专业组负责审查拟定二部收载的品种范围;由主产地所在的省(自治区、直辖市)药品检验所和有关单位负责起草标准,药典委员会办公室组织交叉复核,有些项目组成专题协作组通过实验研究后起草,标准草案经有关专业组委员并邀请有关药品检验所和药厂的代表讨论审议后报卫生部审批。《中国药典》 1985 年版于1985 年9 月出版。1986 年4 月1 日起执行。该版药典共收载药品1489 种。一部收载中药材、植物油脂及单味制剂506 种,中药成方207 种,共713 种;二部收载化学药品、生物制品等776 种。
1985 年7 月1 日《中华人民共和国药品管理法》正式执行,该法规定“药品必须符合国家药品标准或者省、自治区、直辖市药品标准”。明确“卫生行政部门颁布的《中华人民共和国药典》和药品标准为国家药品标准”。“卫生行政部门的药典委员会,负责组织国家药品标准的制定和修订”。进一步确定了药品标准的法定性质和药典委员会的任务。
1986 年卫生部根据药典委员会章程聘请委员150 人组建第五届药典委员会,由卫生部崔月犁部长兼任主任委员,常设办事机构改为秘书长制。同年5 月5 日至8 日召开第五届第一次全体委员会议,讨论修订了委员会章程,通过了“七五”期间标准工作设想,确定编制《中国药典》 1990 年版的指导思想和原则要求。分别举行中药材、中药成方制剂、化学药、抗生素、生化药及药理等专业会议,安排起草和科研任务。1987 年11 月出版《中国药典》 1985 年版增补本,新增品种23 种,修订品种172 种,附录21 项。1988 年10 月,第一部英文版《中国药典》 1985 年版正式出版。同年还出版了药典二部注释选编。1989 年3 月,各地起草的1990 年版药典标准初稿基本完成,药典委员会常设机构开始组织审稿和编辑加工。同年12 月在北京举行药典委员会主任委员、副主任委员和各专业组长扩大会议进行审议,报卫生部批准后付印。1990 年12 月3 日卫生部颁布《中国药典》 1990 年版自1991 年7 月1日起执行。
这版药典分一、二两部,共收载品种1751 种。一部收载784 种,其中中药材、植物油脂等509 种,中药成方及单味制剂275 种;二部收载化学药品、生物制品等967 种。与1985 年版药典收载品种相比,一部新增80 种,二部新增213 种(含1985 年版药典一部移人5 种);删去25 种(一部3 种,二部22 种);对药品名称,根据实际情况作了适当修订。药典二部品种项下规定的“作用与用途”和“用法与用量”,分别改为“类别”和“剂量”,另组织编著《临床用药须知》一书,以指导临床用药。有关品种的红外光吸收图谱,收人《药品红外光谱集》另行出版,该版药典附录内不再刊印。
1991 年组建第六届药典委员会,由卫生部聘请委员共168 人,卫生部陈敏章部长兼任主任委员。同年5 月16 日至18 日召开第一次全体委员会议,讨论通过了委员会的章程和编制《中国药典》 1995 年版设计方案,并成立由主任委员、副主任委员和专家共11 人组成的常务委员会。分设13 个专业组,即:中医专业组、中药材专业组、中成药专业组、西医专业组、药理专业组、化学药专业一组、化学药专业二组、化学药专业三组、抗生素专业组、生化药品专业组、生物制品专业组、放射品专业组、药品名词专业组。会后,各专业组分别召开专业组委员扩大会议,安排落实全会提出的任务。
1993 年《中国药典》 1995 年版、附录初稿发往各地作为起草、修订正文标准的依据。1994 年7 月各地基本完成了标准的起草任务,由药典委员会各专业委员会分别组织审稿工作。1994 年11 月29 日提交常务委员会扩大会议讨论审议,获得原则通过,报请卫生部审批付印。卫生部批准颁布《中国药典》 1995 年版自1996 年4 月l 日起执行。
这版药典收载品种共计2375 种。一部收载920 种,其中中药材、植物油脂等522 种,中药成方及单味制剂398 种;二部收载1 455 种,包括化学药、抗生素、生化药、放射品、生物制品及辅料等。一部新增品种142 种,二部新增品种4 ”种。二部药品外文名称改用英文名,取消拉丁名;中文名称只收载药品法定通用名称,不再列副名。编制出版《药品红外光谱集》第一卷(1995 年版)。《临床用药须知》一书经修订,随《中国药典》 1995 年版同时出版,经卫生部批准,其中的“适应证”和“剂量”部分作为药政和生产部门宣传使用和管理药品的依据。
这届药典委员会除完成1995 年版药典的编制外,还于1992 年、1993 年先后编制出版《中国药典》1990 年版第一、第二增补本,二部注释和一部注释选编,《中药彩色图集》和《中药薄层色谱彩色图集》以及《中国药品通用名称》等标准方面的配套丛书。《中国药典》 1990 年版英文版亦于1993 年7 月出版发行。
为加强国家药品标准工作,1993 年5 月21 日卫生部决定将药典委员会常设机构从中国药品生物制品检定所分离出来,作为卫生部的直属单位,这是药典委员会机构史上一次重大的改革。
1996 年5 月经卫生部批准,第七届药典委员会成立,由卫生部聘请204 位委员组成,其中名誉委员18 人,卫生部陈敏章部长兼任主任委员.1998 年9 月,根据中编办(1998 ) 32 号文:卫生部药典委员会更名为国家药典委员会,并成建制划转国家药品监督管理局管理。因管理体制的变化及1999 年3 月陈敏章部长逝世,在征得有关领导部门同意后,按照第七届药典委员会章程精神,经1999 年12 月第七届药典委员会常务委员会议一致同意调整主任委员、副主任委员。这届委员会设专业委员会共16 个,分别为:中医专业委员会、中药第一专业委员会、中药第二专业委员会、中药第三专业委员会、中药第四专业委员会、医学专业委员会、药品名词专业委员会、附录专业委员会、制剂专业委员会、药理专业委员会、化学药品第一专业委员会、化学药品第二专业委员会、抗生素专业委员会、生化药品专业委员会、放射品专业委员会、生物制品专业委员会。
1996 年召开第七届药典委员会常务委员会第一次会议,通过了这届药典委员会提出的“《中国药典》 2000年版设计方案”,一部确立了“突出特色,立足提高”,二部确立了“赶超与国情相结合,先进与特色相结合”的指导思想。根据这届委员会提出的设计方案,1996 年10 月起,各专业委员会先后召开会议,落实设计方案提出的任务并分工进行工作。1997 年底,首先完成了附录与制剂通则的修改,并下发各起草单位征求意见。1998 年底药典初稿完成,经进一步征求全国各有关方面的意见,至1999 年10 月底,先后召开了16 个专业委员会审定稿会议。《中国药典》 2000 年版于1 999 年12 月经第七届药典委员会常务委员会议审议通过,报请国家药品监督管理局批准颁布,于2000 年1月出版发行,2000 年7 月1 日起正式执行。
2000 年版药典共收载药品2691 种,其中一部收载992 种,二部收载1699 种。一、二两部共新增品种399 种,修订品种562 种。这版药典的附录作了较大幅度的改进和提高,一部新增附录10 个,修订附录31 个;二部新增附录27 个,修订附录32 个。二部附录中首次收载了药品标准分析方法验证要求等六项指导原则,对统一、规范药品标准试验方法起指导作用。现代分析技术在这版药典中得到进一步扩大应用。第七届药典委员会还完成了《中国药典》 1995 年版一九九七年增补本、一九九八年增补本、《中国药品通用名称》(一九九八年增补本)及《药品红外光谱集》(第二卷)、《临床用药须知》(第三版)。1997 年完成了《中国药典》 1995 年版英文版。为加强国际合作与交流,第七届药典委员会还决定《中国药典》 2000 年版英文版与中文版同步出版。
以往几版药典中的“剂量”、“注意”项内容,由于过于简单不能准确反映临床用药的实际情况,根据“《中国药典》 2000 年版设计方案”的提议,这版药典二部取消了这两项,其有关内容移至《中国药典》 2000 年版《临床用药须知》一书中。
2002 年10 月经国家药品监督管理局(2003 年9 月更名为国家食品药品监督管理局)批准,第八届药典委员会成立。由国家药品监督管理局聘请312 位委员组成,不再设立名誉委员。国家药品监督管理局局长郑筱英兼任主任委员。原常务委员会更名为执行委员会,由全体委员大会授权审定《中国药典》及国家药品标准的重大事项。本届委员会设专业委员会共24 个。在上一届委员会的基础上,增设了民族药专业委员会(筹)、微生物专业委员会、药品包装材料与辅料专业委员会;原生物制品专业委员会扩增为血液制品专业委员会、病毒制品专业委员会、细菌制品专业委员会、体细胞治疗与基因治疗专业委员会、重组制品专业委员会和体外诊断用生物试剂专业委员会。
2002 年10 月召开第八届药典委员会全体大会及执行委员会第一次会议,通过了本届药典委员会提出的“《中国药典》 2005 年版设计方案”。设计方案明确了坚持继承与发展、理论与实际相结合的方针;确定了“科学、实用、规范”等药典编纂原则;决定将《中国生物制品规程》并人药典,设为药典三部;并编制首部中成药《临床用药须知》。
2002 年11 月起,各专业委员会先后召开会议,安排设计方案提出的任务并分别进行工作。2003 年7月,首先完成了附录草案,并发有关单位征求意见。2004 年初药典附录与品种初稿基本完成,增修订内容陆续在国家药典委员会网站上公示3 个月,征求全国各有关方面的意见。6 月至8 月,各专业委员会相继召开了审定稿会议。9 月,《中国药典》 2005 年版经过第八届药典委员会执行委员会议审议通过,12 月报请国家食品药品监督管理局批准颁布,于2005 年1 月出版发行,2005 年7 月1 日起正式执行。本版药典收载的品种有较大幅度的增加。共收载3214 种,其中新增525 种。药典一部收载品种1 146 种,其中新增154 种、修订453 种;药典二部收载1967 种,其中新增327 种、修订522 种;药典三部收载101 种,其中新增44 种、修订57 种。《中国药典》 2000 年版收载而本版药典未收载的品种共有9 种。2000 年版《中国生物制品规程》及2002 年增补本收载而未收载人药典的品种共有123 种。
本版药典收载的附录,药典一部为98 个,其中新增12 个、修订48 个,删除1 个;药典二部为137 个,其中新增13 个、修订65个、删除1 个;药典三部为140 个,其中新增62 个、修订78 个,删除1 个。一、二、三部共同采用的附录分别在各部中予以收载,并进行了协调统一。
本版药典在主任委员的积极倡导下,对药品的安全性问题更加重视。药典一部采用原子吸收和电感耦合等离子体质谱法增加了有害元素(铅、镉、砷、汞、铜)测定法,并规定了有害元素的限度;药典一部还增加了中药注射剂安全性检查法应用指导原则。药典二部有126 个静脉注射剂增订了不溶性微粒检查,增修订细菌内毒素检查的品种达112 种;残留溶剂测定法中引入国际间已协调统一的有关残留溶剂的限度要求,并有24 种原料药增订了残留溶剂检查;药典二部还增加了药品杂质分析指导原则、正电子类和锝[ 99mm Tc 〕放射品质量控制指导原则。药典三部增订了逆转录酶活性检查法、人血白蛋白铝残留量测定法等,牛血清白蛋白残留量及CHO 细胞蛋白残留量等检测方法也得到改进。本版药典结合我国医药工业的现状和临床用药的实际情况,将由卫生部颁布的原《澄明度检查细则和判断标准》修订为“可见异物检查法”,以加强注射剂等药品的用药安全。
本版药典坚持注重环保的一贯性原则,在品种中对苯等有害溶剂,尽可能采用其他溶剂替代。本版药典根据中医辨证施治的理论,对收载的中成药标准项下的功能与主治进行了科学规范,为准确理解中成药的功能主治及合理用药提供了保证,促进中医药在新时期的健康发展。
本版药典三部源于《中国生物制品规程》。自1951 年以来,该规程已有六版颁布执行,分别为1951 年及1952 年修订版、1959 年版、1979 年版、1990 年版及1993 年版(诊断制品类)、1995 年版、2000 年版及2002 年增补本。2002 年翻译出版了第一部英文版《中国生物制品规程》(2000 年版)。
第八届药典委员会还完成了《中国药典》 2000 年版2002 年增补本、2004 年增补本、《中国药品通用名称》(2005 年版)及《药品红外光谱集》(第三卷)、《临床用药须知》(中成药第一版、化学药第四版)。2005 年,完成了《中国药典》 2005 年版英文版.为加强国际合作与交流,本届委员会期间,与美国药典委员会联合举办了首届中美药典论坛。
参考资料:
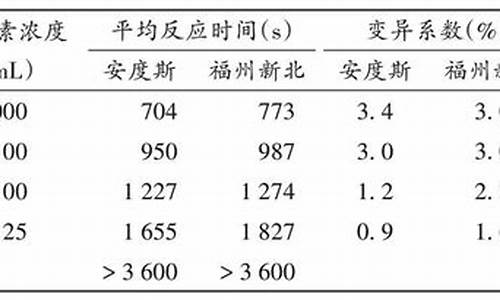
细菌内毒素检查是一复杂的酶促反应过程,检查条件的任何变化都会对实验结果产生影响。中国药典附录”细菌内毒素检验法“项下明确规定:
1、反应温度37℃±1℃,时间60min±2min。反应时间与温度一定要严格控制好,否则会得出错误结论。如果反应温度或反应时间不足都会-----出现假阳性;同时反应温度或反应时间超出药典规定会-----出现假阴性。
2、药典规定该试验应在1万级环境内的100级区域下进行。然而对试验室温度要求在检查项下未做明确规定,但从中国药典凡例三十条4项下:除另有规定外应以25℃±2℃为准。
我本人认为试验环境没有必要控制在1万级环境内局部100级区域下进行,因这种环境反而易污染内毒素(原因:以前试验时污染的内毒素溶液挥发后易从风口吹出)。但实验室温度最好控制在20℃以下,这是一个酶促反应,温度对其影响比较大。
3、供试品溶液的pH值、离子浓度、鲎试剂的灵敏度及操作人员的操作水平等因素都会影响到试验结果。
因此,中国药典2015年版开始对“细菌内毒素检查”做了较大修改:
① 做“鲎试剂灵敏度复核”试验。该试验的目的不仅是考察鲎试剂的灵敏度是否准确,也是考察检验人员操作方法是否正确及实验条件是否符合规定的一次考核;
② “干扰试验”,当一个新的药品制订“质量标准”时或生产企业的原料来源、配方和生产工艺发生变化时都应做“干扰试验”;消除干扰的方法一般采用BET水稀释或加酸碱调节pH的方法消除干扰。其目的是确证供试品在该试验浓度及试验条件下对鲎试剂与细菌内毒素的反应无干扰作用。
③ 平时做“细菌内毒素检查”试验时,分别做:供试品2管;PPC2管;阳性对照2管;阴性对照2管。并且规定当阳性对照管、PPC管都为阳性且阴性对照管都为阴性时实验才可认为有效。否则,实验结果无效。
原因:如果阳性对照管不是阳性,=====出现该问题的原因最大可能性是出在“细菌内毒素标准溶液的制备”第一步,内毒素标准品或工作标准品加BET水复溶是很关键的一步,一定要按药典操作,既加BET水后在振荡器上振荡,15min,否则内毒素混合不均匀会出现这种清况;其次是更换不同批号或不同厂家的鲎试剂或BET水后,一定要做鲎试剂灵敏度复核试验,否则不知该批鲎试剂灵敏度及检查用水是否符合要求。-
--------阴性对照管不是阴性说明BET水有污染。
---------PPC管应显阳性,而未显阳性说明供试品或供试品稀释液在该试验条件下对试验有干扰。
如对细菌内毒素检查法感兴趣,你可以用“百度”搜索下近年来我在《中国药师》、《中国药业》、〈海峡药学〉等专业杂志上发表的有关细菌内毒素检查内容的文章,“得力生注射液细菌内毒素检查法的探讨”、“吡拉西坦细菌内毒素检查方法的建立”、“长春西汀葡萄糖注射液细菌内毒素检查法的研究”、“地塞米松磷酸钠原料药细菌内毒素检查法的建立”、“利巴韦林细菌内毒素检查法的建立”、“维生素C注射液细菌内毒素检查中干扰问题的探讨”等论文,以加深对该问题的理解。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。