药品原料进口流程-进口原料药管理办法最新

去药监局办理药品经营许可证的时候需要有三名以上具有药师资格的人员,也就是需要三本证书。
注册程序:由全体股东指定的代表或者共同委托的代理人向公司登记机关申请名称预先核准,凭名称预先核准通知书、药师资格证书到药监局办理药品经营许可证,凭名称预先核准通知书到银行开户,然后到会计师事务所进行验资,由会计师事务所出具验资报告后,带上全体股东指定代表或者共同委托代理人的证明、企业名称预先核准通知书、验资报告、股东会决议(选举法宝代表人的决议)、股东身份证、公司章程、许可证、营业场所证明材料、房屋租赁协议到工商局办理注册登记。然后到税务局办理税务登记证,到质监局办理机构代码证。
药品注册,是指国家食品药品监督管理局根据药品注册申请人的申请,依照法定程序,对拟上市销售的药品的安全性、有效性、质量可控性等进行系统评价,并决定是否同意其申请的审批过程。
注册申请:
药品注册申请包括新药申请、已有国家标准的药品申请、进口药品申请和补充申请。
新药申请,是指未曾在中国境内上市销售的药品的注册申请。已上市药品改变剂型、改变给药途径、增加新适应症的,按照新药申请管理。
已有国家标准的药品申请,是指生产国家食品药品监督管理局已经颁布正式标准的药品的注册申请。
进口药品申请,是指境外生产的药品在中国境内上市销售的注册申请。
补充申请,是指新药申请、已有国家标准的药品申请或者进口药品申请经批准后,改变、增加或取消原批准事项或者内容的注册申请。
进口药品注册,如果境外生产企业在中国没有合法办事机构,必须委托中国的专业机构代理注册。
再注册申请,指药品批准证明文件有效期满后,申请人拟继续生产或进口该类药品的注册申请。 [1]?
新药注册:
新药定义
按照《药品注册管理办法》的规定,新药是指未曾在中国境内外上市销售的药品,已上市药品改变剂型、改变给药途径的,按照新药管理。
申请人
药品注册申请人 (以下简称申请人 ),是指提出药品注册申请,承担相应法律责任,并在该申请获得批准后持有药品批准证明文件的机构。境内申请人应当是在中国境内合法登记的法人机构,境外申请人应当是境外合法制药厂商。办理药品注册申请事务的人员应当是相应的专业技术人员,并熟悉药品注册管理法律、法规和技术要求。
公民以个人名义不能注册新药。
申请详细
国家药品监督管理局主管全国药品注册管理工作,负责对药物临床研究、药品生产和进口的审批。省、自治区、直辖市药品监督管理局受国家药品监督管理局的委托,对药品注册申报资料的完整性、规范性和真实性进行审核。
申请药品注册,申请人应当向所在地省、自治区、直辖市药品监督管理局提出,并报送有关资料和药物实样;申请新药注册所报送的资料应当完整、规范,数据必须真实、可靠 ;引用文献资料应当注明著作名称、刊物名称及卷、期、页等 ;未公开发表的文献资料应当提供资料所有者许可使用的证明文件。外文资料应当按照要求提供中文译本。国家药品监督管理局对下列新药申请可以实行快速审批: (一 )未在国内上市销售的来源于植物、动物、矿物等药用物质制成的制剂和从中药、天然药物中提取的有效成份及其制剂; (二 )未在国内外获准上市的化学原料药及其制剂、生物制品; (三 )抗艾滋病病毒及用于诊断、预防艾滋病的新药,治疗恶性肿瘤、罕见病等的新药; (四 )治疗尚无有效治疗手段的疾病的新药。
申请人在提出药品注册申请时,应当承诺所有试验数据均为自行取得并保证其真实性。
申请人委托其他机构进行药物研究或者进行单项试验、检测、样品的试制、生产等,应当与被委托方签订合同。申请人应当对申报资料中的药物研究数据的真实性负责。
为申请药品注册而进行的药物临床前研究,包括药物的合成工艺、提取方法、理化性质及纯度、剂型选择、处方筛选、制备工艺、检验方法、质量指标、稳定性,药理、毒理、动物药代动力学等。中药制剂还包括原药材的来源、加工及炮制等;生物制品还包括菌毒种、细胞株、生物组织等起始材料的质量标准、保存条件、遗传稳定性及免疫学的研究等。
申请人应当对所申请注册的药物或者使用的处方、工艺等,提供在中国的专利及其权属状态说明,并提交对他人的专利不构成侵权的保证书,承诺对可能的侵权后果负责。药品注册申请批准后发生专利权纠纷的,当事人应当自行协商解决,或者依照有关法律、法规的规定,通过司法机关或者专利行政机关解决。
生物制品原料药在国外可以单独申报吗
第一条 为规范蛋白同化制剂、肽类激素的进出口管理,根据《中华人民共和国药品管理法》、《中华人民共和国海关法》、《反兴奋剂条例》等法律、行政法规,制定本办法。第二条 国家对蛋白同化制剂、肽类激素实行进出口准许证管理。第三条 进口蛋白同化制剂、肽类激素,进口单位应当向所在地省、自治区、直辖市食品药品监督管理部门提出申请。第四条 进口供医疗使用的蛋白同化制剂、肽类激素,进口单位应当报送以下资料:
(一)药品进口申请表。
(二)购货合同或者订单复印件。
(三)《进口药品注册证》(或者《医药产品注册证》)(正本或者副本)复印件。
(四)进口单位的《药品经营许可证》、《企业法人营业执照》、《进出口企业资格证书》(或者《对外贸易经营者备案登记表》)、《组织代码证书》复印件;药品生产企业进口本企业所需原料药和制剂中间体(包括境内分包装用制剂),应当报送《药品生产许可证》、《企业法人营业执照》、《组织代码证书》复印件。
(五)《进口药品注册证》(或者《医药产品注册证》)持有者如委托其他公司代理出口其药品的,需提供委托出口函。
上述各类复印件应当加盖进口单位公章。第五条 因教学、科研需要而进口蛋白同化制剂、肽类激素的,进口单位应当报送以下资料:
(一)药品进口申请表;
(二)购货合同或者订单复印件;
(三)国内使用单位合法资质的证明文件、药品使用数量的测算依据以及使用单位出具的合法使用和管理该药品保证函;
(四)相应科研项目的批准文件或者相应主管部门的批准文件;
(五)接受使用单位委托代理进口的,还需提供委托代理协议复印件和进口单位的《企业法人营业执照》、《进出口企业资格证书》(或者《对外贸易经营者备案登记表》)、《组织代码证书》复印件。
上述各类复印件应当加盖进口单位公章。第六条 境内企业因接受境外企业委托生产而需要进口蛋白同化制剂、肽类激素的,报送本办法第五条第一款第(一)项、第(三)项、第(五)项规定的资料。
上述各类复印件应当加盖进口单位公章。第七条 省、自治区、直辖市食品药品监督管理部门收到进口申请及有关资料后,应当于15个工作日内作出是否同意进口的决定;对同意进口的,发给药品《进口准许证》;对不同意进口的,应当书面说明理由。第八条 进口蛋白同化制剂、肽类激素必须经由批准的允许药品进口的口岸进口。进口单位持省、自治区、直辖市食品药品监督管理部门核发的药品《进口准许证》向海关办理报关手续。进口蛋白同化制剂、肽类激素无需办理《进口药品通关单》。第九条 进口供医疗使用的蛋白同化制剂、肽类激素(包括首次在中国销售的),进口单位应当于进口手续完成后,及时填写《进口药品报验单》,持《进口药品注册证》(或者《医药产品注册证》)原件(正本或者副本)、药品《进口准许证》原件,向进口口岸食品药品监督管理部门报送下列资料一式两份,申请办理《进口药品口岸检验通知书》:
(一)《进口药品注册证》(或者《医药产品注册证》)(正本或者副本)和药品《进口准许证》复印件;
(二)进口单位的《药品生产许可证》或者《药品经营许可证》复印件,《企业法人营业执照》复印件;
(三)原产地证明复印件;
(四)购货合同复印件;
(五)装箱单、提运单和货运发票复印件;
(六)出厂检验报告书复印件;
(七)药品说明书及包装、标签的式样(原料药和制剂中间体除外)。
上述各类复印件应当加盖进口单位公章。第十条 口岸食品药品监督管理部门接到《进口药品报验单》及相关资料,审查无误后,将《进口药品注册证》(或者《医药产品注册证》)(正本或者副本)原件、药品《进口准许证》原件交还进口单位,并应当于当日向负责检验的口岸药品检验所发出《进口药品口岸检验通知书》,附本办法第九条规定的资料1份。
口岸药品检验所接到《进口药品口岸检验通知书》后,应当在2个工作日内与进口单位联系,到存货地点进行抽样,抽样完成后,应当在药品《进口准许证》原件第一联背面注明“已抽样”字样,并加盖抽样单位的公章。
进口医药商品价格平衡细则(试行)
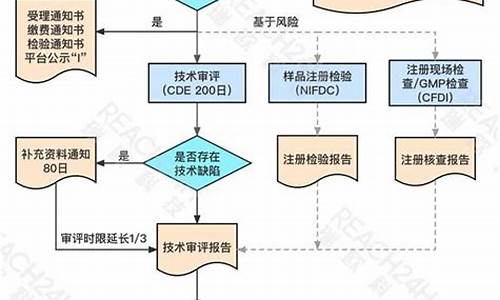
进口药品注册管理办法及所需时间 1、申请进口药品注册,应当填写《药品注册申请表》,报送有关资料和样品,提供相关证明文件,(证明性文件需向进口国的大使馆进行公证)向国家食品药品监督管理局提出申请。 2、国家食品药品监督管理局对申报资料进行形式审查需30日,符合要求的,出具药品注册申请受理通知书并通知中国药品生物制品检定所组织对3个生产批号的样品进行注册检验。 3、中国药品生物制品检定所收到资料和样品后,应当在5日内组织进行注册检验。 4、承担进口药品注册检验的药品检验所在收到资料、样品和有关标准物质后,应当在60日内完成注册检验并将药品注册检验报告报送中国药品生物制品检定所。特殊药品和疫苗类制品的样品检验和药品标准复核应当在90日内完成。 5、中国药品生物制品检定所接到药品注册检验报告和已经复核的进口药品标准后,应当在20日内组织专家进行技术审查,必要时可以根据审查意见进行再复核。 6、国家食品药品监督管理局药品审评中心应当在120日内组织药学、医学及其他技术人员对申报资料进行审评,如需补充资料,审评中心发布补充资料通知,根据通知内容,需在4个月内一次性将资料补充完毕。药品审评中心对补充资料进行审评需40日。 7、国家食品药品监督管理局应当在20日内作出审批决定;20日内不能作出决定的,经主管局领导批准,可以延长10日,并应当将延长时限的理由告知申请人。 8、国家食品药品监督管理局应当自作出药品注册审批决定之日起10日内颁发、送达有关行政许可证件。 9、申请人拿到临床批件需向国家食品药品监督管理局提交临床方案等资料进行备案,然后进行临床试验6-8个月。 10、将临床报告递交国家食品药品监督管理局。国家食品药品监督管理局药品审评中心应当在120日内组织药学、医学及其他技术人员对报送的临床试验等资料进行全面审评。如需补充资料,审评中心发布补充资料通知,根据通知内容,需在4个月内一次性将资料补充完毕。药品审评中心对补充资料进行审评需40日。 11、国家食品药品监督管理局依据综合意见,在20日内做出审批决定。符合规定的,发给《进口药品注册证》。 综上所有手续,共需受理时间为:23-38个月
国外进口的药物在国内要不要做临床试验呢?有什么相关法律法规
第一条 根据国家物价局、国家医药管理局国药联经字[90]第79号“关于加强进口医药商品价格管理的通知”精神,为做好进口医药商品价格平衡工作,特制定本细则。第二条 国家医药管理局负责组织进口医药商品价格的衔接、平衡工作。暂定:北京、天津、上海、广州、广东、大连、辽宁、湖北、福建、山东、江苏省、直辖市医药管理局和中国医药公司为参加价格平衡单位。第三条 国药联经字[90]第79号文件进口医药商品中的药品类不包括进口药材和中成药。进口原料药的作价办法另行下达。第四条 同一品种、有几种外汇同时进口的。其外汇价格应综合平衡,平衡基价以不超过国家外汇管理局外汇调剂中心颁布的外汇牌价为准。第五条 进口医药商品价格衔接、平衡应遵循的原则:进口医药商品价格的制订,必须符合经济规律的要求,有利于国内医药工业的发展和符合市场的实际需要,合理使用外汇,发挥价格调节供求的作用。
1.国内不能生产,医疗急需,必须组织进口的品种,进销差率可高于规定差率安排。
2.国内已有生产,但疗效尚不稳定,需要部分进口的品种,进销差率原则上按18%掌握。
3.国内已有生产,基本上能满足需要,应减少或控制进口的品种,进口成本高于国内价格的按国内价格执行,低于国内价格的,进销差率可低于规定差率安排。
4.因特殊情况,临时组织进口的急救,特需品种的国内销售价格,可在进口成本的基础上加适当的手续费制定。具体价格由各省、自治区、直辖市医药管理局审定。第六条 衔接、平衡的进口医药商品国内销售价格,由国家医药管理局下达。药品实行全国统一价;尚未平衡价格的品种,暂由各省、自治区、直辖市医药管理局参照以上原则制定口岸销售价格,报国家医药管理局备案。药品销地执行进货口岸地价格。医疗器械销地价格按国产作价即:销地价格在产地进货口岸价格基础上,加实际运杂费后,再加综合差率5%左右。第七条 进口医药商品价格平衡工作每年进行两次,时间一般在广交会后一个半月左右。各省、自治区、直辖市医药管理局应在广交会后一个月之内将进口的品种、数量,国外底价等数字按附表的要求报国家医药管理局经济协调司物价处。第八条 进口医药商品的商业内部调拨作价仍按现行规定执行。进口医疗器械的商业内部调整拨作价仍按国药联财字[84]第271号和药财字[84]第56号文件规定即:“商业内部调拨作价,在现行调拨扣率的基础上,由购、销双方协商确定”。第九条 本细则自通知之日起执行。
药材进口批文是什么
根据《进口药品管理办法》
第十一条 申请注册的进口药品,必须按照国家药品监督管理局规定的程序和要求在中国进行临床研究(包括生物等效性试验)。其中申请注册的原料药若中国尚未生产,则应用该原料药制成的制剂在中国进行临床研究。临床研究须按照中国《新药审批办法》及《药品临床试验管理规范》(GCP)的规定执行。特殊病种或其它情况需减免临床研究的,需经国家药品监督管理局审查批准。
第十六条 《进口药品注册证》是国家药品监督管理局核发的允许国外生产的药品在中国注册、进口和销售使用的批准文件。国家药品监督管理局各口岸药品检验所凭《进口药品注册证》接受报验。
进口兽药管理办法
问题一:进口中药材需提供什么手续 你好。先要办理进口药材批件。
进口药材的申报资料项目及要求
申请人需报送下述资料一式一份。
(一)《进口药材申请表》。
(二)申请人《药品经营许可证》或者《药品生产许可证》、《营业执照》(复印件)。
(三)供货方合法登记证明文件(如《营业执照》等)(复印件)。
(四)购货合同(复印件)。
(五)药材质量标准及其来源。
现已成功注册韩国红参、朝鲜穿山龙、印度决明子、加拿大西洋参、伊朗西红花等非首次进口药材;
现已成功注册朝鲜*羊藿、苍术、威灵仙、杏仁、赤芍等首次进口药材。
联系人:王晓锋经理
邮件:[email protected]
问题二:进口中药材,中药饮片、原料药应具有哪些证书和批件? 进口原料药、中药材、中药饮片应具有《进口药品注册证》(或《医药产品注册证》)或《进口药品批件》,应符合药品进口手续,应有口岸药品检验所的药品检验报告。进口药品注册证》或《医药产品注册证》、《进口药品检验报告书》或《进口药品通关单》和首次进口的《进口药品检验报告单》。
2.进口药材:《进口药材批件》。
3.《注册证》、《批件》的有效期、生产国、进口包装的标签上应注明药品的名称、注册证号,并有中文标识。
4.复印件应有供货单位质量管理机构的原印章。
5.所规定的范围内,需批批进口检验的,应按规定索要批《进口药品检验报告
6.相关的管理文件。
问题三:添加有中药材成分产品能否进口,参考哪些相关文件 具体就是要看你的是一般食品,还是药品,还是保健品。理论上,全部都是可以进的。但是后两个是需要批文的。前一个是比较简单的。如果想进一步了解,可以联系我。多谢
问题四:中药材出口需要什么资格和手续 35分 国家税务总局转发对外贸易经济合作部
《关于进出口经营资格管理的有关规定》的通知
各省、自治区、直辖市和计划单列市国家税务局:
为加快外贸经营体制改革,促进和规范各类企业从事进出口业务,对外贸易经济合作部制定了《关于进出口经营资格管理的有关规定》。《规定》对进出口经营资格实行分类管理,采用登记和核准制;核准或登记企业进出口经营范围时,不再单列贸易方式,企业可以按国家规定以各种贸易方式从事进出口业务;进出口企业资格证书的年审期限由每年3月31日前改为每年4月30日之前。
为适应管理体制的变化,对外贸易经济合作部从2002年1月1日起,启用进出口经营资格新的批文格式。
现将《对外贸易经济合作部关于印发的通知》(外经贸贸发[2001]370号)和2002年新启用的批文格式转发你们,请在办理出口企业退(免)税登记及日常管理时,参照执行。
附件:2002年起启用的新批文格式(略)
对外贸易经济合作部关于印发《关于进出口经营资格管理的有关规定》的通知
2001年7月10日 外经贸贸发[2001]370号各省、自治区、直辖市及计划单列市外经贸委(厅、局),新疆建设兵团外经贸局: 为加快外贸经营体制改革,促进和规范各类企业从事进出口业务,我部制定了《关于进出口经营资格管理的有关规定》,现将该文印发给你们,请遵照执行。
特此通知
附件:关于进出口经营资格管理的有关规定附件
关于进出口经营资格管理的有关规定
为加快外贸经营体制改革,促进和规范各类企业从事进出口业务,现对企业进出口经营资格管理的有关问题规定如下:
一、进出口经营资格实行登记和核准制,遵循自主申请、公开透明、统一规范、依法监督的原则,各类所有制企业(外商投资企业、商业物资、供销社企业、边境小额贸易企业,经济特区、浦东新区企业除外,下同)进出口经营资格实行统一的标准和管理办法。
外经贸部授权各省、自治区、直辖市、计划单列市及哈尔滨、长春、沈阳、西安、成都、南京、武汉、广州、珠海、汕头市外经贸委(厅、局),新疆建设兵团外经贸局(以下统称授权发证机关)负责办理进出口经营资格登记并核发《中华人民共和国进出口企业资格证书》。
二、对企业的进出口经营资格,按登记或核准的经营范围实行如下分类管理:
(一)外贸流通经营权(经营各类商品和技术的进出口,但国家限定公司经营或禁止进出口的商品及技术除外)。
(二)生产企业自营进出口权(经营本企业自产产品的出口业务和本企业所需的机械设备、零配件、原辅材料的进口业务,但国家限定公司经营或禁止进出口的商品及技术除外)。
外经贸部和授权发证机关在核准或登记企业进出口经营范围时,不再单列贸易方式,企业可以按国家规定以各种贸易方式从事进出口业务。
三、申请进出口经营权的企业资格条件和要求提交的材料
(一)申请外贸流通经营权的企业资格条件和要求提交的材料
1.资格条件
(1)企业应具备企业法人资格,成立一年以上,经工商行政管理部门登记注册领取《企业法人营业执照》,按国家规定办理工商年检并通过年检。
(2)注册资本(金)不低于500万元人民币(中西部地区不低于300万元人民币,币别下同)。
(3)已办理税务登记,依法纳税。
(4)该企业法定代表人或负责人,在3年内未曾担任过被撤销对外贸易经营许可的企业的法定代表人或负责人(指在其担任法定代表人或负责人期间,企业违法违规被撤销对外贸易经营许可)。
2.要求提交的材料:
(1)企业书面申......>>
问题五:怎么从批准文号区别中药和西药 药品的批准文号格式是:国药准字+1位字母+8位数字
化学药品的1位数字是H,中药是Z,生物制品是S,体外叮学诊断试剂是T,进口分包装药品是J,通过SFDA整顿的原保健药品是S。
问题六:报关中药品属于哪种货物 重要属于药品,需要北京食药监局批文才能正规进口的。希望能够帮到您。
问题七:进口干海马是否需要进口药材批件 当然需要,还需要办理进口药材批件,备案。
兽药进口通关单怎么办理
第一章 总则第一条 为了加强进口兽药的管理,保证兽药的质量,根据《兽药管理条例》的规定,制定本办法。第二条 中华人民共和国农业部负责进口兽药的注册、审批工作,省、自治区、直辖市畜牧(农牧)厅(局)负责本辖区进口国家已注册兽药的审批工作。
中国兽药监察所负责进口兽药的质量复核试验工作,农业部指定的口岸兽药监察所负责进口兽药的检验和质量监督工作。
各级农牧行政管理机关、兽药监察所对已进口的兽药实施监督管理。第三条 国家对进口兽药实行注册登记、质量许可制度。未经注册并取得《进口兽药登记许可证》的兽药,不准进口。
凡需进口兽药者,均必须向所在省、自治区、直辖市畜牧(农牧)厅(局)或农业部申报,办理《进口兽药许可证》。第四条 凡进口兽药者,都应遵守《兽药管理条例》、《兽药管理条例实施细则》和本办法的规定。第二章 进口兽药的注册管理第五条 农业部公布的《进口兽药注册目录》收载的兽药,系已按照国家或国外兽药质量标准进行了质量复核试验,并准予在我国注册的兽药品种。第六条 进口兽药注册的要求、程序按农业部发布的《外国企业在中华人民共和国注册兽药管理办法》的规定办理。第七条 农业部在接到外国企业申请注册兽药的全部材料后的三个月内做出是否受理的决定。第八条 注册兽药的动物药效试验结束后,由承担试验单位将试验报告报农业部。第九条 经质量复核试验合格的,由试验单位起草质量标准草案,连同试验报告一起送交农业部。试验不合格的,由农业部通知申请注册企业。
注册《外国企业在中华人民共和国注册兽药管理办法》第六条规定的第一类兽药,不再制定质量标准。
承担质量复核试验的单位在收到试验用全部材料后的六个月内向农业部报送结果。第十条 农业部在收到动物试验报告和质量复核试验报告后的四个月内做出是否批准发给《进口兽药登记许可证》的决定。第十一条 为科学研究试验或为积累临床资料试验而进口的兽药不需注册,但需报农业部批准。未经批准,不得私自进行试验。第三章 申请进口兽药的审批程序第十二条 需要进口兽药的单位,到所在省(自治区、直辖市)畜牧(农牧)厅(局)领取“进口兽药申请表”,按表中所列要求和《进口兽药注册目录》收载的品种填写。“进口兽药申请表”经单位主管部门签署同意意见后,报所在省(自治区 、直辖市)畜牧(农牧)厅(局)。第十三条 省(自治区 、直辖市)畜牧(农牧)厅(局)接到“进口兽药申请表”后,对进口单位、兽药品种、进口数量等逐一审核。经审核批准后,发给《进口兽药许可证》。审批机关应在一个月内做出是否批准的决定。
《进口兽药许可证》有效期限为一年,逾期未进口应重新申请。
《进口兽药许可证》副本应抄送农业部和进口口岸兽药监察所。第十四条 进口生产紧急需要并且是自用的和用于科学研究试验所需要的少量未注册的兽药,由进口单位填写“进口兽药申请表”,经单位主管部门签署意见后报农业部。地方所属单位须经所在省(自治区、直辖市)畜牧(农牧)厅(局)同意。
农业部应在收到“进口兽药申请表”后的一个月内做出是否发给《进口兽药许可证》的决定。所进口的兽药只限自用,不准销售或转让。第十五条 进口兽药单位取得《进口兽药许可证》后,方可签订进口合同。合同必须按照《进口兽药许可证》规定的兽药名称、规格、数量、生产厂家、质量标准签订。第十六条 需要常年进口兽药的畜禽饲养场、饲料加工企业、兽药生产企业,可以申报全年度进口计划,一次办理《进口兽药许可证》。如需变更进口计划,必须向原审批机关申报。第十七条 从事兽药或饲料添加剂生产的中外合资经营企业、中外合作经营企业、外资企业(以下简称三资企业)以及来料加工、补偿贸易方式的企业,其产品不在中国销售的,所进口的原料药可不注册。用货单位凭《兽药生产许可证》、营业执照和出口或加工合同,到所在省(自治区、直辖市)畜牧(农牧)厅(局)办理《进口兽药许可证》,并报农业部备案。进口的原料只限自用,不准销售或转让。产品在中国销售的,应申请注册并按本办法第十二条、第十三条的规定办理。第四章 进口兽药质量检验与监督
法律分析:根据农业部、海关总署令第2号 公布《 兽药进口管理办法 》,兽药进口应当办理《进口兽药通关单》。《进口兽药通关单》由中国境内代理商向兽药进口口岸所在地省级人民政府兽医行政管理部门申请。申请时,应当提交下列材料(普通兽药进口《进口兽药通关单》申请应提交的材料):
(一)兽药进口申请表;
(二)代理合同(授权书)和购货合同复印件;
(三)《兽药经营许可证》、工商营业执照复印件;兽药生产企业申请进口本企业生产所需原料药的,提交《兽药生产许可证》、工商营业执照及其所生产产品的批准文号证明文件复印件;
(四)《进口兽药注册证书》复印件
法律依据:《中华人民共和国兽药管理条例》
第三条 兽医行政管理部门负责全国的兽药监督管理工作。县级以上地方人民政府兽医行政管理部门负责本行政区域内的兽药监督管理工作。
第四条 国家实行兽用处方药和非处方药分类管理制度。兽用处方药和非处方药分类管理的办法和具体实施步骤,由兽医行政管理部门规定。
第五条 国家实行兽药储备制度。发生重大动物疫情、灾情或者其他突发事件时,兽医行政管理部门可以紧急调用国家储备的兽药;必要时,也可以调用国家储备以外的兽药。
第六条 国家鼓励研制新兽药,依法保护研制者的合法权益。
第七条 研制新兽药,应当具有与研制相适应的场所、仪器设备、专业技术人员、安全管理规范和措施。研制新兽药,应当进行安全性评价。从事兽药安全性评价的单位应当遵守兽医行政管理部门制定的兽药非临床研究质量管理规范和兽药临床试验质量管理规范。省级以上人民政府兽医行政管理部门应当对兽药安全性评价单位是否符合兽药非临床研究质量管理规范和兽药临床试验质量管理规范的要求进行监督检查,并公布监督检查结果。
第八条 研制新兽药,应当在临床试验前向临床试验场所所在地省、自治区、直辖市人民政府兽医行政管理部门备案,并附具该新兽药实验室阶段安全性评价报告及其他临床前研究资料。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。