欧盟原料药注册条件-欧盟原料药注册条件最新
什么是欧盟「REACH制度」?
REACH制度,中译名《关于化学品注册、评估、授权与限制制度》,是欧盟基于保护人类健康和环境安全的长远考虑,同时也为提高欧盟化学工业竞争力,追求社会可持续发展,即将建立的一个统一的化学品监控管理体系。
REACH法规主要对3万多种化学品及其下游的纺织、轻工、制药等产品的注册、评估、许可和限制等进行管理。它将取代欧盟现有的40多项有关化学品的指令和法规,涉及面相当广。法规中对企业影响最大的是注册,对于1吨以上的新物质,新法规生效后60天,生产商、进口商要完成注册。
[REACH制度实施时间表]
按欧盟委员会提出新的规章制度登记、评估和批准的化学品(实现)2003年10月29日( 委员会(03)644(01) . 是为了更好地保护人类健康和环境的改善,尽早发现化学物质的特性. 同时创新能力和竞争力的提高欧盟化学工业. 福利制度的实现将逐渐,越来越成为物质逐步实现.
提案责任范围更加危险化学品行业管理和提供物质安全资料. 制造商和进口商必须了解有关药物的特性,使他们安全管理和登记资料中心数据库. 一种化学机构担任中心的系统实现:将从数据库需要操作系统,配合深入评估可疑化学物质管理、公共数据库中,消费者人才可以威胁信息。
"在两年的谈判 委员会原先建议 之后,在2006年6月27日, 欧洲议会,安理会共同达成立场。委员会欢迎并全力支持 共同立场 并认为,根据平衡 里斯本目标和创新能力显着提高,实现欧洲公民健康和环境的好处。实现支持进行二读时达成最后协议,将尽全力协助协议预计2006年底内实现。"
据了解,REACH法规已于2005年11月通过欧盟议会全体投票第一次正式宣读,今年10月将进行第二次正式宣读。如果能产生第二次公开宣读协议,REACH将从2007年4月1日起正式生效;如果不能达成协议,REACH仍将在2007年中期开始生效。
[REACH制度的理据原则]
“一种化学物质,在尚未证明其安全之前,它就是不安全的。”这是欧盟酝酿多年、并将正式实施的REACH制度的重要理论依据。这一原则将推翻先前的假定原则:“一种化学物质,只要没有证据表明它是危险的,它就是安全的。”
[REACH制度对中国的影响]
预定于2006年开始实施的REACH法规将对世界石油化工、轻工、纺织、制药、农药等相关行业产生重大影响。据估计,将有500万种现今在欧盟市场上销售的商品受到影响。
欧盟提出的化学品注册、评估和批准(REACH)政策,将对中国检验检疫工作人员在执法监管中带来新课题。
REACH法规是一个空前的绿色贸易壁垒,众多中国企业在欧盟市场将面临严峻考验。对中国来说,制药、农药以及广泛应用化学品的纺织、服装、鞋、玩具、家具等行业都将受到REACH的“牵连”。
法规中对企业影响最大的是注册,注册不仅抬高了欧盟的市场门槛,巨额的注册费用也是大多数中小企业无力承担的。另外,REACH法规所涉及的不仅仅是化学品的生产商,还囊括了进口商、下游产业等多个领域。一旦REACH法规正式生效,欧盟化学品生产商或出口企业无疑会将巨额检测费用转嫁给下游企业,这对中国化工进口企业来说将增加成本。
REACH法规的影响将是双向的,由于欧盟本土企业所生产的产品同样需要遵照该法规进行注册、评估等,所以待其实施后,欧盟的化学品生产商或出口企业成本亦将同步提高,这将可能引起由欧盟进口的产品价格上涨,这对于生产依赖于该地区中高端原料药供应的企业来说,同样是个坏消息。
中国由商务部世贸司牵头,中国石油化工协会、中国五矿化工进出口商会、国家质检总局、商务部公平贸易局、国际商报等有关部门联合组成了“评估欧盟REACH法规对企业影响工作小组”,将尽快就REACH法规可能对我国产生的实质影响以及我国企业、政府应如何应对等问题与行业内专家对话,并开展化工企业的行业调查,以便了解REACH法规对企业的实质影响。
[企业应积极做好应对REACH法规准备]
作为一个全新的体系,欧盟REACH法规(《关于化学品注册、评估、许可和限制制度》)将欧盟市场上约3万种化工产品及其下游的纺织、轻工、制药等产品分别纳入注册、评估、许可三个管理监控系统。
按照欧盟拟订的时间表,REACH法规实施后,产量在1000吨以上的化学物质,应于3年内完成注册;产量在100~1000吨的化学物质,于6年内完成注册;产量在1~100吨的化学物质于11年内完成注册,未能按期纳入该管理系统的产品不能在欧盟市场上销售。
同时,该法规还规定了严格的检测标准,需要高昂的检测费用,而这些费用将全部由企业承担。据欧盟估算,每一种化学物质的基本检测费用约需8.5万欧元,每一新物质的检测费用约需57万欧元。据中国石油和化学工业协会估计,由此而增加的费用,将使我国对欧盟石油和化工产品的出口成本普遍提高5%以上,一些医药类的产品包括原料药、中间体、植物提取物也被涵盖于此范围内。
[国际对REACH制度的反应]
由REACH所引起的连锁反应将导致国际贸易环境恶化同样让人担心。据了解,受欧盟的影响,美国已在2003年启动了立法提案,初期目标是在2004年底完成2800种大量生产的化学品的检测。出于同样的原因,日本在2003年5月28日宣布未来将要建立商品检验注册制度,其做法与REACH法规非常相似。可以预见,随着由REACH法规所引发的“绿色壁垒”大战的一步步激化,包括原料药在内的化工产品将在短期内遭受巨大挑战。
每一个已经和准备开展出口欧洲业务的企业,现在都应该进一步了解REACH体系的细节,审核产品业务以确定适合REACH规定的产品和REACH对公司的影响,采取战略和行为计划以应对REACH的挑战,准备与上下游供应链进行沟通,寻找足够的资料以应对REACH。
REACH法规对纺织企业的影响
REACH法规主要对3万多种化学品及其下游的纺织、轻工、制药等产品的注册、评估、许可和限制等进行管理,涉及面相当广。
意大利纺织企业表明,对于Reach法规的实施,企业持有不同的态度:准备相应措施的少数派和持观望态度的多数派。
而世界著名的Marioboselli控股公司总裁兼意大利时尚协会主席Mario Boselli则认为,Reach法规立法实施后,将对意大利纺织产业带来很大的影响。
Mario先生谈到:“我们以集团方式进行纺织品生产,已对染色加工企业提出了尽早采取应对Reach法规措施的指示”。不愧为行业的龙头企业,措施落实也快。
Reach法规(Registration, Evaluation, Authorization and Restriction of Chemicals)是欧盟《关于化学品注册、评估、许可和限制制度》的简称。是完善现行欧盟指令(危险品安全指令(DPD)、危险品调剂指令(DPD)、现存物质规则以及销售和使用限制等)框架的一部法规。
Reach法规是为了更好地保护人类健康和环境的改善? 是绿色贸易壁垒? 企业持有不同的态度。
原料药在欧盟是不是按照药品管理的?
出口到欧盟药品需要在国内批准。2011年6月欧盟发布了原料药新指令2011/62/EU,要求对进口到欧盟成员国的原料药,自2013年7月2日起,其生产企业必须取得出口国药品监管机构签发的证明文件。出口欧盟原料药证明文件由原料药生产企业所在地省级食品药品监督管理部门负责出具。
出口欧盟原料药证明文件办理大概要多久
是。随着世界经济一体化进程的加快,国内药企也逐步走出国门,接受国际竞争和技术壁垒挑战,在欧洲市场,由欧洲药品质量管理局(EDQM)颁发的CEP证书是国内原料药成功进入欧洲的首选注册程序,所以原料药在欧盟是按照药品管理的。
什么是COS认证和EDMF注册
可在6个月之内办完。
CEP的有效期为5年,CEP持有者应在过期前6个月申请更新,如若企业能坚持不断更新档案资料,CEP将具有无限期的有效期。CEP持有者须及时通知客户有关变更内容,且将对应已修订的CEP提供给客户。CEP的修订类型主要包括通知、小变更、重大变更、更新(5年之后)、专论修订或条例变更后更新等。
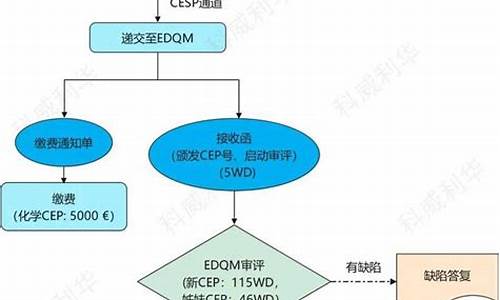
目前,我国原料药出口至欧盟市场须通过欧洲药品质量管理局(简称EDQM)现场检查,获取CEP证书。据EDQM官方数据显示,截至2011年12月7日,我国原料药企业共获取367个CEP证书,其中,有效CEP证书335个,被取消、暂停及已过期的CEP证书32个,企业被暂停和吊销CEP证书的情况时有发生。2010年期间,EDQM在全球范围内对34家生产企业进行了现场核查,暂停了16个CEP证书,撤销了8个,检查中的不合格率非常高。
COS
认证和
EDMF
注册的比较
EDMF
和
COS
证书都是原料药进入欧洲市场有效而必需的支持性材料,
二者都是用于证明
制剂产品中所使用的原料药质量的文件以便支持使用该原料药的制剂产品在欧洲的上市申
请(
MAA
);它们之间究竟有什么不同呢?
首先,是评审方式上的不同。
EDMF
是由单个国家的机构评审的,是作为制剂上市许
可申请文件的一部分而与整个制剂的上市许可的申请文件一起进行评审的。针对不同的制
剂,不同的评审机构有不同的侧重,
因而会对文件有不同的要求,
提出不同的问题。无论原
料药物用于哪个制剂的生产,也无论该
EDMF
是否已进行过登记,都要进行重新评审,因
而对我们这些原料药的生产厂家来说是多次申请登记,要花费更多的时间和精力。而
COS
申请文件是由有关当局组成的专家委员会集中评审的,
评审结果将决定是否发给
COS
证书。
一个原料药一旦取得
COS
证书,就可以用于欧洲药典委员会的三十一个成员国内的所有制
剂生产厂家的制剂生产。
其次,针对的情况不同。
EDMF
与使用该原料药的制剂药物的上市许可申请(
MAA
)
不可分离,必须由使用该原料药的欧洲终端用户申请;而
COS
证书则是直接将证书颁发给
原料药的生产厂家,
因此可由原料药生产厂家独立申请
,
并不需要现成的中间商和终端用户,
因而生产厂家在申请过程中更加主动。
第三,适用的范围不同。
EDMF
程序适用于所有的原料药品,只要是原料药,无论是
否已收载入欧洲药典,
都可以通过
EDMF
文件的方式进入欧洲市场,
而
COS
证书只能处理
欧洲药典已收载的物质,
当然不仅是原料药,
也包括生产制剂所用的辅料,
我国的药用辅料
也可以申请
COS
证书。
第四,所要求提供的资料不同。比如
EDMF
文件必须包括药物的稳定性研究资料,而
COS
证书的申请文件并不强求这些资料。
第五,申请的结果不同。申请
COS
证书的结果是直接颁发给原料药的生产厂家一个证
书,
只要将这个证书的复印件提供给欧洲方面的中间商或终端用户,
对方就可以购买我们的
原料药,而
EDMF
文件登记的结果是只告诉制剂生产厂家一个
EDMF
文件的登记号,欧洲
评审机构不会将这个登记号告诉原料药的生产厂家,
原料药的生产厂家只能从负责申请登记
的欧洲药品制剂的生产厂家那儿查询这个登记号。
CoS
(
Certificate
of
Suitability
)指的是欧洲药典适用性认证,目的是考察欧洲药典是否能
够有效地控制进口药品的质量,
这是中国的原料药合法地被欧盟的最终用户使用的另一种注
册方式。
这种注册途径的优点是不依赖于最终用户,
可以由原料药生产厂商独立地提出申请。
中国的原料药生产厂商可以向欧盟药品质量指导委员会(
EDQM
)提交产品的
CoS
认证文
件(
CoS
Dossier
),申请
CoS
证书,同时生产厂商必须要承诺产品生产的质量管理严格
遵循
GMP
标准,
在文件审查和可能的现场考察通过之后,
EDQM
会向原料药品的生产厂商
颁发
CoS
证书。
如果作为最终用户的欧盟成员国制剂生产企业准备采用中国生产的原料时,
只要在注册文件或变更文件中附上该产品的
CoS
证书复印件即可非常容易地获得批准。
欧洲药典适应性认证证书(
CEP
)不仅被所有欧盟成员国所承认,而且被很多承认欧
洲药典地位的国家所认可,如很多欧盟以外的欧洲国家、澳大利亚和中国。
CEP
证书能够
替代
EDMF
文件用于药品上市申请和原料药来源的变更申请。
要求
随着美国、
欧盟和日本三方在药品注册程序和法规上的相互协调,
欧盟在进口的原料药
注册中逐步接近美国
FDA
的偏重现场
GMP
检查的办法,
今后有可能对每一家提出
COS
认
证的生产厂家进行现场的
GMP
检查。
自
1999
年开始,原料药生产企业在申请
COS
认证的技术文件后面必须要附加两封承
诺信,
一封信承诺说产品是按照
GMP
规范进行生产的,
另一封信要承诺同意欧盟的相关审
查机构进行现场检查。如果欧盟
EDQM
的
GMP
审查越来越频繁,甚至最终变成为一种必
要的审查手段,
生产厂家就应当对此做出充分的准备,以使自身的
GMP
管理状况能够适应
欧盟的检查。
欧盟的
GMP
检查与国内的
GMP
认证有以下差别:首先,欧盟的
GMP
检查依据的
IC
H
Q7A
的指导纲要,厂家要参照此指导进行自身检查;其次,所有的质量管理文件、操作
规范(
SOP
)和各种生产管理表格、标牌、标签和生产记录都应当具备中英文对照,能够
让国外的审查官员看懂;其三,要对员工进行
GMP
的全员培训,了解并适应国外检查的特
点。
COS
认证过程对企业是有积极意义的,会使企业的
GMP
管理达到国际水平,而且随
着美、欧、日三方协调的进一步发展,通过欧盟的
GMP
检查和
COS
认证最终有可能直接
进入美国和日本市场,
至少会使美国
FDA
的注册变得更为容易。
因此,
尽管目前
EDQM
还
没有对
COS
认证的申请人全部进行
GMP
检查,但中国的原料药生产厂家在提出
COS
认
证申请的同时为欧盟
GMP
检查做充分的准备是值得的。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。