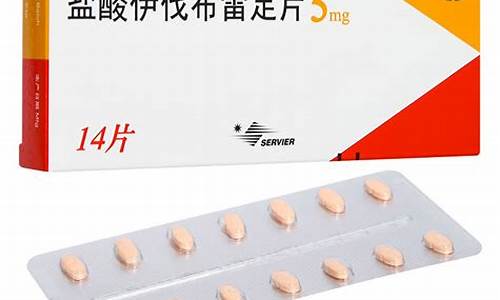
原料药备案登记平台-原料药备案查询
食品生产配料表需要备案吗?
需要,因为食品生产许可发证检验过程标签中的配料是必检项。配料表中各种配料应按要求进行标注,不得隐瞒或虚报。否则一旦发现后果严重。特别是食品添加剂或特殊原辅料,例如防腐剂,糖,营养强化剂等不得出现实际添加隐瞒不标,也不得未添加而虚假标注。所以必须备案。
什么是主料?
主料是指对产品的生产起主要作用的材料,辅料是指对产品生产起辅助作用的材料。
在生活中,常见的主料和辅料有许多类别:
在烹饪行业,主料是想要加工的菜品的主要原材料。
在服装行业,主料是制作衣服的主要材料。
在制药行业,主料是制作药品的原料药。
餐厅菜品配方需要备案吗?
不需要备案,餐厅菜品配方属于商业秘密,不能进行备案,以免造成泄露。
材料备案需要哪些材料?
材料起草说明,起草的法律依据及领导批示,相关部门单位会审资料,本单位内审相关资料。
原料药通用名的命名依据是什么?在药品注册中要如何进行描述?
作用不同。
药品登记号是生产或者已有国家标准的东西的,须经监督管理部门批准,并在批准文件上规定该产品的专有编号,此编号称为批准文号,而药品备案号,针对补充申请而言,如改变说明书、包材、原料产地,生产地址等很多需要重新完善的工作,前者是登记申请注册的,后者是补充申请,两者的区别就是其作用不同。
药品是用来预防、治疗、诊断疾病,有目的地调整人体生理机能,并规定有适应症或功能主治、用法、用量的物质。药品包括中药材、中成药、化学原料药及其制剂、抗生素、生化药品、放射品、血清、疫苗、血液制品及诊断药品等。
原料药DMF是什么
由药典委员会按照《药品通用名称命名原则》组织制定并报卫生部备案的药品的法定名称,是同一种成分或相同配方组成的药品在中国境内的通用名称,具有强制性和约束性。
药品在上市之前,都是要去药典会核名的。药典会给盖章。
一般大学做实验,原料药都是由哪些人买呢?
药物管理档案(Drug Master Files, DMF)是一份提交给美国FDA的保密文件,它提供了关于用于生产药物的原料、活性中间体及其设施、流程、包装及仓储等相关的信息。FDA目前接受书面递交和电子递交(eCTD)两种格式。点击免费了解FDA法规要求
DMF的主要的种类有:
I型,生产地点和厂房设施、人员(已取消);
II型,中间体、原料药和药品;
III型,包装物料;
IV型,辅料、着色剂、香料、香精及其它添加剂;
V型,非临床数据资料和临床数据资料。
虽然美国FDA没在正式文件中规定出口到美国的厂家必须上报DMF资料,但是若该产品被用做处方药时,美国FDA会派官员对生产厂家进行检查,以确定该厂的生产是否与上报资料所述相符,是否是按美国cGMP(现行GMP)要求进行生产。美国的DMF文件库是全世界制剂厂家广泛参照的一个供应商资源库,所以几乎所有想让产品推向国际的制药厂都进行DMF备案。DMF注册后有以下几个优势:
1 简化了制剂厂家申请的内容,直接以DMF备案号来代替制剂申请资料中有关单元的具体资料,减少了因向众多制剂客户提供资料而造成企业技术秘密外泄的风险;
2 取得DMF备案号的企业和其产品均会在FDA网站上公示,持有FDA给予的DMF备案号可以吸引更多的制剂客户共建合作发展关系,并在企业的竞争中被制剂客户优先考虑而获得竞争优势;
一般大学做实验,所需要的原材料包括药品等数量都是比较大的,是不能直接购买,否则就违反了相关纪律规定。
现在购买实验材料的流程基本上是:
1、使用单位(实验室)管理员在学期开学之前根据下学期教学计划安排,造出需要购买的实验材料清单,交到实验室主任。
2、实验室主任会同相关课程负责人、专业负责人对实验材料清单进行核查,适当进行修改完善,交到院系。
3、由各院系统一汇总后的实验材料清单上报到学校教务处及分管教学的校长(或院长),经校级领导审批后,转到学校招标办。
4、学校招标办报省市相关部门备案后,在学校网站或其它公开媒体上发布相关实验材料购买的招标信息,由各家公司进行公开招标。
5、中标公司按标书约定提供原材料后,由各实验室管理员,实验室主任进行签收。
6、院系所有原材料全部签收完成后,院系负责人签名。
7、中标公司及学校招标办再一次对原材料进行核查核对,中标公司准备相关发票等材料,报学校相关领导签字。
8、到学校财务部门结帐。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。