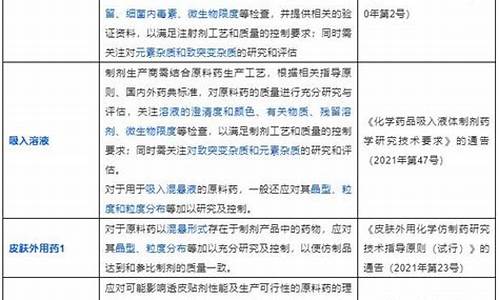
原料药注册指导原则-原料药注册国家

1、中牧CAHIC ( 国内最大的动物保健品生产企业之一,农业产业化重点龙头企业,北京市高新技术企业,中牧实业股份有限公司 )
2、Zoetis硕腾 ( 由辉瑞旗下动物保健更名而来,全球最大的动物保健品提供商之一,引领动保行业,硕腾(苏州)动物保健品有限公司 )
3、Merial梅里亚 ( 源于法国的世界著名动物保健品品牌,全球动物保健行业领导者,大型跨国企业,梅里亚动物保健有限公司 )
4、勃林格殷格翰 ( 世界领先的动物保健品企业,全球最大的猪疫苗供应商之一,大型制药企业,上海勃林格殷格翰药业有限公司 )
5、拜耳BAYER ( 全球制药巨头,世界领先的兽用医药专业产品供应商之一,世界500强企业,大型跨国企业,拜耳医药保健有限公司 )
6、宝灵BAOLING ( 内蒙古著名商标,农业部定点口蹄疫疫苗骨干企业,国家级兽用疫苗工程实验室,金宇保灵生物药品有限公司 )
7、瑞普ringpu ( 天津名牌,国内规模最大/产品种类最全的动物保健品生产基地之一,行业领先企业,津瑞普生物技术股份有限公司 )
8、易邦 ( 国家保护商标,山东省名牌产品,国家级高新技术企业,兽用生物制品行业领先品牌,青岛易邦生物工程有限公司 )
9、三仪SAM ( 国家保护商标,辽宁省著名商标,领先的高科技动物药品制造商,兽用制剂知名品牌,大连三仪动物药品有限公司 )
10、远征 ( 国家保护商标,国内规模最大的兽药制剂企业之一,国家高新技术企业,知名兽药品牌,河北远征药业有限公司 )
一个新研制的药品,国家分为一、二、三(还有吗)类药品,分别是什么含义,(即区分标准)
COS
认证和
EDMF
注册的比较
EDMF
和
COS
证书都是原料药进入欧洲市场有效而必需的支持性材料,
二者都是用于证明
制剂产品中所使用的原料药质量的文件以便支持使用该原料药的制剂产品在欧洲的上市申
请(
MAA
);它们之间究竟有什么不同呢?
首先,是评审方式上的不同。
EDMF
是由单个国家的机构评审的,是作为制剂上市许
可申请文件的一部分而与整个制剂的上市许可的申请文件一起进行评审的。针对不同的制
剂,不同的评审机构有不同的侧重,
因而会对文件有不同的要求,
提出不同的问题。无论原
料药物用于哪个制剂的生产,也无论该
EDMF
是否已进行过登记,都要进行重新评审,因
而对我们这些原料药的生产厂家来说是多次申请登记,要花费更多的时间和精力。而
COS
申请文件是由有关当局组成的专家委员会集中评审的,
评审结果将决定是否发给
COS
证书。
一个原料药一旦取得
COS
证书,就可以用于欧洲药典委员会的三十一个成员国内的所有制
剂生产厂家的制剂生产。
其次,针对的情况不同。
EDMF
与使用该原料药的制剂药物的上市许可申请(
MAA
)
不可分离,必须由使用该原料药的欧洲终端用户申请;而
COS
证书则是直接将证书颁发给
原料药的生产厂家,
因此可由原料药生产厂家独立申请
,
并不需要现成的中间商和终端用户,
因而生产厂家在申请过程中更加主动。
第三,适用的范围不同。
EDMF
程序适用于所有的原料药品,只要是原料药,无论是
否已收载入欧洲药典,
都可以通过
EDMF
文件的方式进入欧洲市场,
而
COS
证书只能处理
欧洲药典已收载的物质,
当然不仅是原料药,
也包括生产制剂所用的辅料,
我国的药用辅料
也可以申请
COS
证书。
第四,所要求提供的资料不同。比如
EDMF
文件必须包括药物的稳定性研究资料,而
COS
证书的申请文件并不强求这些资料。
第五,申请的结果不同。申请
COS
证书的结果是直接颁发给原料药的生产厂家一个证
书,
只要将这个证书的复印件提供给欧洲方面的中间商或终端用户,
对方就可以购买我们的
原料药,而
EDMF
文件登记的结果是只告诉制剂生产厂家一个
EDMF
文件的登记号,欧洲
评审机构不会将这个登记号告诉原料药的生产厂家,
原料药的生产厂家只能从负责申请登记
的欧洲药品制剂的生产厂家那儿查询这个登记号。
CoS
(
Certificate
of
Suitability
)指的是欧洲药典适用性认证,目的是考察欧洲药典是否能
够有效地控制进口药品的质量,
这是中国的原料药合法地被欧盟的最终用户使用的另一种注
册方式。
这种注册途径的优点是不依赖于最终用户,
可以由原料药生产厂商独立地提出申请。
中国的原料药生产厂商可以向欧盟药品质量指导委员会(
EDQM
)提交产品的
CoS
认证文
件(
CoS
Dossier
),申请
CoS
证书,同时生产厂商必须要承诺产品生产的质量管理严格
遵循
GMP
标准,
在文件审查和可能的现场考察通过之后,
EDQM
会向原料药品的生产厂商
颁发
CoS
证书。
如果作为最终用户的欧盟成员国制剂生产企业准备采用中国生产的原料时,
只要在注册文件或变更文件中附上该产品的
CoS
证书复印件即可非常容易地获得批准。
欧洲药典适应性认证证书(
CEP
)不仅被所有欧盟成员国所承认,而且被很多承认欧
洲药典地位的国家所认可,如很多欧盟以外的欧洲国家、澳大利亚和中国。
CEP
证书能够
替代
EDMF
文件用于药品上市申请和原料药来源的变更申请。
要求
随着美国、
欧盟和日本三方在药品注册程序和法规上的相互协调,
欧盟在进口的原料药
注册中逐步接近美国
FDA
的偏重现场
GMP
检查的办法,
今后有可能对每一家提出
COS
认
证的生产厂家进行现场的
GMP
检查。
自
1999
年开始,原料药生产企业在申请
COS
认证的技术文件后面必须要附加两封承
诺信,
一封信承诺说产品是按照
GMP
规范进行生产的,
另一封信要承诺同意欧盟的相关审
查机构进行现场检查。如果欧盟
EDQM
的
GMP
审查越来越频繁,甚至最终变成为一种必
要的审查手段,
生产厂家就应当对此做出充分的准备,以使自身的
GMP
管理状况能够适应
欧盟的检查。
欧盟的
GMP
检查与国内的
GMP
认证有以下差别:首先,欧盟的
GMP
检查依据的
IC
H
Q7A
的指导纲要,厂家要参照此指导进行自身检查;其次,所有的质量管理文件、操作
规范(
SOP
)和各种生产管理表格、标牌、标签和生产记录都应当具备中英文对照,能够
让国外的审查官员看懂;其三,要对员工进行
GMP
的全员培训,了解并适应国外检查的特
点。
COS
认证过程对企业是有积极意义的,会使企业的
GMP
管理达到国际水平,而且随
着美、欧、日三方协调的进一步发展,通过欧盟的
GMP
检查和
COS
认证最终有可能直接
进入美国和日本市场,
至少会使美国
FDA
的注册变得更为容易。
因此,
尽管目前
EDQM
还
没有对
COS
认证的申请人全部进行
GMP
检查,但中国的原料药生产厂家在提出
COS
认
证申请的同时为欧盟
GMP
检查做充分的准备是值得的。
国家药品监督管理局建立化学原料药、辅料及直接接触药品的包装材料和容器关联审评审批制度。这种制度是
新药的分类目前我国对于新药的分类,是将新药分成中药、天然药物和化学药品及生物制品三大部分,又按照各自不同的成熟程度再分类。现行《药品注册管理办法》将在化学药品注册各分为五类,具体如下:
(1)中药、天然药物分类
(一)注册分类
1、未在国内上市销售的中药、天然药物中提取的有效成分及其制剂。
2、未在国内上市销售的来源于植物、动物、矿物等药用物质制成的制剂。
3、中药材的代用品。
4、未在国内上市销售的中药材新的药用部位制成的制剂。
5、未在国内上市销售的中药、天然药物中提取的有效部位制成的制剂。
6、未在国内上市销售的中药、天然药物制成的复方制剂。
7、未在国内上市销售的中药、天然药物制成的注射剂。
8、改变国内已上市销售药品给药途径的制剂。
9、改变国内已上市销售药品剂型的制剂。
10、改变国内已上市销售药品工艺的制剂。
11、已有国家标准的中成药和天然药物制剂。
(二)说明
1、“未在国内上市销售的中药、天然药物中提取的有效成分及其制剂”是指国家药品标准中未收载的从中药、天然药物中得到的未经过化学修饰的单一成分及其制剂。
2、“未在国内上市销售的来源于植物、动物、矿物等药用物质制成的制剂”是指未被国家药品标准或省、自治区、直辖市地方药材规范(以下简称“法定标准”)收载的中药材及天然药物制成的制剂。
3、“中药材的代用品”是指用来代替中药材某些功能的药用物质,包括:(1)已被法定标准收载的中药材;(2)未被法定标准收载的药用物质。
4、“未在国内上市销售的中药材新的药用部位制成的制剂”是指具有法定标准的中药材原动、植物新的药用部位制成的制剂。
5、“未在国内上市销售的中药、天然药物中提取的有效部位制成的制剂”是指从中药、天然药物中提取的一类或数类成分制成的制剂。
6、“未在国内上市销售的中药、天然药物制成的复方制剂”包括:(1)传统中药复方制剂;(2)现代中药复方制剂;(3)天然药物复方制剂。
7、“未在国内上市销售的中药、天然药物制成的注射剂”,其中包括水针、粉针、大输液之间的相互改变及其他剂型改成的注射剂。
8、“改变国内已上市销售药品给药途径的制剂”包括:(1)不同给药途径之间相互改变的制剂;(2)局部给药改为全身给药的制剂。
9、“改变国内已上市销售药品剂型的制剂”是指在给药途径不变的情况下改变剂型的制剂。
10、“改变国内已上市销售药品工艺的制剂”包括:(1)工艺有质的改变的制剂;(2)工艺无质的改变的制剂。
工艺有质的改变主要是指在生产过程中改变提取溶媒、纯化工艺或其他制备工艺条件等,使提取物的成分发生较大变化。
11、“已有国家标准的中成药或天然药物制剂”是指我国已批准上市销售的中药或天然药物制剂的注册申请。
(2)化学药品注册分类
1、未在国内外上市销售的药品:
(1)通过合成或者半合成的方法制得的原料药及其制剂;
(2)天然物质中提取或者通过发酵提取的新的有效单体及其制剂;
(3)用拆分或者合成等方法制得的已知药物中的光学异构体及其制剂;
(4)由已上市销售的多组份药物制备为较少组份的药物。
(5)新的复方制剂;
2、改变给药途径且尚未在国内外上市销售的制剂 。
3、已在国外上市销售但尚未在国内上市销售的药品:
(1)已在国外上市销售的原料药及其制剂;
(2)已在国外上市销售的复方制剂 ;
(3)改变给药途径并已在国外上市销售的制剂 。
4、改变已上市销售盐类药物的酸根、碱基(或者金属元素),但不改变其药理作用的原料药及其制剂。
5、改变国内已上市销售药品的剂型,但不改变给药途径的制剂。
6、已有国家药品标准的原料药或者制剂。
(3)生物制品注册分类
1、未在国内外上市销售的生物制品。
2、单克隆抗体。
3、基因治疗、体细胞治疗及其制品。
4、变态反应原制品。
5、由人的、动物的组织或者体液提取的,或者通过发酵制备的具有生物活性的多组份制品。
6、由已上市销售生物制品组成新的复方制品。
7、已在国外上市销售但尚未在国内上市销售的生物制品。
8、含未经批准菌种制备的微生态制品。
9、与已上市销售制品结构不完全相同且国内外均未上市销售的制品(包括氨基酸位点突变、缺失,因表达系统不同而产生、消除或者改变翻译后修饰,对产物进行化学修饰等)。
10、与已上市销售制品制备方法不同的制品(例如采用不同表达体系、宿主细胞等)。
11、首次采用DNA重组技术制备的制品(例如以重组技术替代合成技术、生物组织提取或者发酵技术等)。
12、国内外尚未上市销售的由非注射途径改为注射途径给药,或者由局部用药改为全身给药的制品。
13、改变已上市销售制品的剂型但不改变给药途径的生物制品。
14、改变给药途径的生物制品(不包括上述12项)。
15、已有国家药品标准的生物制品。
请问原料药生产的批文怎么办理?
答案:A
考查药品注册管理的基本制度和要求。“审批”是审查批准决定,是比“审评”(审查评价过程)更为严格的行政许可程序,化学药品制剂、原料药既要审评,也要审批,但是相关辅料、直接接触药品的包装材料和容器要求相对宽松。选项A说法最精确。故答案为A。
新药注册中的化药3+3类;化药4+4类;化药3+6类;都是什么意思呢?
这个程序是很麻烦的,首先得研究,研究原料的合成,检验,进行详细的研究后组成申报资料,向国家药品监督管理局进行申报,国家药品监督管理局审评中心认为你的研究符合规定,生产的原料安全、有效、稳定后,会发给你一个生产批件。条件是必须由持有GMP认证证书的生产企业申报。相关的情况很多,可以查看一下《药品管理法》中的相关条款,也可以联系我。我现在做药品研发的。zhangyanhong1961@163.com
原料药数据分析系统怎么样?
化药3+3类中前一个3是指原料药按3类注册申报,后一个3是指制剂也按3类注册申报;化药4+4类是指原料药按4类注册申报,其制剂按4类注册申报;化药3+6是指原料药按3类注册申报,其制剂按6类注册申报.
几加几,就指原料药按几类注册申报,其制剂按几类注册申报。
扩展资料
化学药品具体的注册分类办法如下:
一、化学药品注册分类
1、未在国内外上市销售的药品:
(1)通过合成或者半合成的方法制得的原料药及其制剂;
(2)天然物质中提取或者通过发酵提取的新的有效单体及其制剂;
(3)用拆分或者合成等方法制得的已知药物中的光学异构体及其制剂;
(4)由已上市销售的多组份药物制备为较少组份的药物;(5)新的复方制剂。
2、改变给药途径且尚未在国内外上市销售的制剂。
3、已在国外上市销售但尚未在国内上市销售的药品:
(1)已在国外上市销售的原料药及其制剂;
(2)已在国外上市销售的复方制剂;
(3)改变给药途径并已在国外上市销售的制剂。
4、改变已上市销售盐类药物的酸根、碱基(或者金属元素),但不改变其药理作用的原料药及其制剂。
5、改变国内已上市销售药品的剂型,但不改变给药途径的制剂。
6、已有国家药品标准的原料药或者制剂。
百度百科-化学药品
api的原料药的发展
原料药对于医药产业链是上游的存在的属性,是保障药品供应、满足人民用药需求的基础,目前各国对于原料药产业的重视程度明显加大。
但是在原料药研发和使用的过程中,很多人都是“开头难、结尾也难”,为了检索药物合成路线,需要查询大量的刊期、论文、专利资料等等,耗时耗力,找到资料搞清一篇文献的合成细节,却找寻不到更多更优质的合成路线;想要购买却找寻不到合适的厂商,想要分析原料药进出口数据,分析市场动态,却没有数据来源。
对此,药融云重磅推出了原料药数据库,集成原料药生产厂商、原料药用量、海关进出口、合成路线,原料药注册信息、登记信息等,实现原料药综合查询的系统,提供全球API供需、市场规模、合成信息一站检索,帮助业内人士快速、高效的完成所需信息的查找与整理。
原料药行业数据分析系统适用于:原料药研发人员、调研人员、高校师生、医药中间体生产企业、有机化学销售员等。
一、查询合成路线,筛选最佳方案
任何一个化合物的合成路线通常都有多条,药物合成也是这样,原料药的合成,最终的目的是要走进工厂批量化的生产,选择一条适合自己生产情况的路线是至关重要。
原料药系统
药融云数据库整合了多条合成方法,包含对应的合成路线、反应条件、中间体、试剂信息。并提供了对应的参考文献,专利溯源。
1、查询合成路线
列如:在合成路线数据库中通过名称搜索“Ezetimibe”合成路线共一百多条。
药物合成路线
2、查询中间体和试剂
除了查询合成路线还可查看每条合成路线中涉及的中间体和试剂,还提供更为详细的原始资料,也可根据下方的参考文献,自行查看。
中间体试剂
二、调研市场需求、为立项/市场分析做参考
1、原料药用量推算
根据每年全球市场制剂用量推算,收载得到6000+原料药用量信息。不同品种、不同企业、不同国家市场下,各个年份中该原料药的详细用量、占比及排行;并包含全局分析模块,清晰展示各品种、区域中该产品的用量对比情况,便于探究某原料药在目标市场近年的大致用量,及分析潜在的客户、竞争企业。
调研市场需求,为立项/市场分做参考
2、查询海关进出口信息
包含了中国、美国、俄罗斯、印度等各国海关进出口货物的货物名称、时间、进口商、出口商、数量及价格等信息,可通过货物名称、海关编码、提单号检索,并支持进出口国家筛选,帮助您方便快捷地了解药物的进出口情况,进行全面市场调研、分析市场动态。
原料药海关进出口
三、生产厂商分布一键查,掌握企业供应竞争布局
在药融云原料药数据库中,可以查询目标产品的全球生产厂商分布,在中国、欧美日韩等五个国家地区的登记注册状态;掌握供应企业、竞争企业布局。
如检索「Ritonavir」,可看到该原料药在全球范围内有近50家企业可生产。中国、印度、意大利、美国等10个国家均有相应的生产企业,其中印度最多,有21家企业可生产;其次为中国,中国安徽、上海、石家庄等省市有十余家企业可生产。
掌握企业供应竞争布局
四、查询注册登记信息,满足更多需求
包含CDE原料药、药用辅料和药材包登记信息、美国DMF注册、欧盟CEP认证、日本MF注册、韩国DMF注册、FDA批准辅料等。
注册登记信息、分析更多需求
药融云原料药行业数据分析系统助力于,原料药市场分析、用量推算,查询合成路线、中间体、试剂等等,助力于业内人士快速查询相关数据。
新药注册特殊审批管理规定的管理规定
根据权威调查机构发布的国内化学药制品市场分析报告指出,2013年化学制药工业经济运行情况不容乐观,但增长情况仍值得期待。创新型企业将带动本产业转型升级。此外,随着化学制药工业电子务的发展,入驻交易平台成为创新型企业的必经之路。传统的原料药发展受限,转型升级需择路而行,随着深圳创新型企业入驻南方交易平台,越来越多的原料药供应商也开始了自己的电商之路。 中国是原料药生产大国,2012年原料药产量为136万吨,同比增长了9.05%,产量位居世界第一。规模效益的取得得益于中国生产的低成本和环境的污染,在目前我国物价普遍上涨,环保管理不断加强的情况下,行业发展的成本优势变的不明显。
在国际上,中国最大的竞争对手印度,虽然其在行业发展的规模上不如中国,但在成本优势和行业发展速度上都比中国有明显的优势。 我国现有医药企业8700多家,通过GMP的医药生产企业6000多家,在国家食品药品监督管理局注册的原料药生产企业共有3000多家,医药中间体的生产企业也占较大比例,
2008年,中国原料药进出口总额238.94亿美元,同比增长22.19%,占我医药进出口总额的49.07%。
从2008年至今,我国原料药出口年均复合增长率超过20%,2009出口额达到175.8亿美元,同比增长29.59%。出口对原料药工业的拉动作用越来越明显和重要,直接促进了行业利润水平的提高,2012年1-11月,原料药实现利润155.9亿元,增幅高达49.5%。 第一,受金融危机的影响,国际买家资金紧张,购买力下降或购买周期延长,不仅影响了中国原料药的销售量,而且增大了出口企业的经营风险。
第二,价格暴涨暴落加重了国际买家的担心和观望,影响了原料药行情的平稳发展。
第三,部分原料药价格增幅较大,造成企业扩大产能的冲动,加剧了市场供过于求的矛盾。
第四,主要出口目的国和竞争对手国的货币贬值,降低了中国原料药的价格竞争力,加大了出口难度。第五,金融危机促使国际贸易保护主义加剧,使中国部分出口市场环境进一步恶化。 首先,全球药品市场2014年将有望保持8%以上的增幅,新兴医药市场有可能保持更大的增幅,原料药的国际国内市场需求将继续呈增长态势。
其次,中国的许多原料药品种在国际市场占有较高的市场份额,规模优势明显,短期内其它国家无法替代。
第三,虽然因多重因素的影响,中国原料药的价格有较大上涨,但这些上涨因素是刚性的,2013年不可能大幅下降并影响到中国原料药的出口总额。从2012年原料药进口情况看,均价上涨了28.21%,在全球原料药价格普遍上涨的情况下,中国原料药价格的比较优势依然存在。
第四,中国企业避免同质化竞争,发展特色原料药的努力,和众多企业瞄准发达国家市场,积极通过高端市场认证,不断提高出口产品质量的做法,将拓展中国原料药的出口空间。
第五,国家鼓励出口政策的不断出台和落实,也将对原料药的出口增长起到重要的推动作用。
第一条 为鼓励研究创制新药,有效控制风险,根据《药品注册管理办法》,制定本规定。
第二条 根据《药品注册管理办法》第四十五条的规定,国家食品药品监督管理局对符合下列情形的新药注册申请实行特殊审批:
(一)未在国内上市销售的从植物、动物、矿物等物质中提取的有效成份及其制剂,新发现的药材及其制剂;
(二)未在国内外获准上市的化学原料药及其制剂、生物制品;
(三)治疗艾滋病、恶性肿瘤、罕见病等疾病且具有明显临床治疗优势的新药;
(四)治疗尚无有效治疗手段的疾病的新药。
主治病证未在国家批准的中成药功能主治中收载的新药,可以视为尚无有效治疗手段的疾病的新药。
属于(一)、(二)项情形的,药品注册申请人(以下简称申请人)可以在提交新药临床试验申请时提出特殊审批的申请。
属于(三)、(四)项情形的,申请人在申报生产时方可提出特殊审批的申请。
第三条 国家食品药品监督管理局根据申请人的申请,对经审查确定符合本规定第二条情形的注册申请,在注册过程中予以优先办理,并加强与申请人的沟通交流。
第四条 申请人申请特殊审批,应填写《新药注册特殊审批申请表》(附件1),并提交相关资料。
《新药注册特殊审批申请表》和相关资料应单独立卷,与《药品注册管理办法》规定的申报资料一并报送药品注册受理部门。
第五条 药品注册受理部门受理后,应将特殊审批申请的相关资料随注册申报资料一并送交国家食品药品监督管理局药品审评中心。
第六条 国家食品药品监督管理局药品审评中心负责对特殊审批申请组织审查确定,并将审查结果告知申请人,同时在国家食品药品监督管理局药品审评中心网站上予以公布。
(一)属于本规定第二条(一)、(二)项情形的,国家食品药品监督管理局药品审评中心应在收到特殊审批申请后5日内进行审查确定;
(二)属于本规定第二条(三)、(四)项情形的,国家食品药品监督管理局药品审评中心应在收到特殊审批申请后20日内组织专家会议进行审查确定。
特殊审批申请的审查确定时间包含在《药品注册管理办法》规定的技术审评工作时间内。
第七条 国家食品药品监督管理局药品审评中心对获准实行特殊审批的注册申请,按照相应的技术审评程序及要求开展工作。负责现场核查、检验的部门对获准实行特殊审批的注册申请予以优先办理。
第八条 获准实行特殊审批的注册申请,申请人除可以按照国家食品药品监督管理局药品审评中心的要求补充资料外,还可以对下列情形补充新的技术资料:
(一)新发现的重大安全性信息;
(二)根据审评会议要求准备的资料;
(三)沟通交流所需的资料。
属于(一)项情形的,若申请人在国家食品药品监督管理局药品审评中心形成技术审评意见后提交补充资料的,技术审评工作时间将适当延长,一般为20日。
第九条 申请人在收到国家食品药品监督管理局药品审评中心发出的补充资料通知后,如在4个月内无法提交补充资料,可延长至8个月。
第十条 已获准实行特殊审批的注册申请,国家食品药品监督管理局药品审评中心应建立与申请人沟通交流的工作机制,共同讨论相关技术问题。
第十一条 属于本规定第二条(一)、(二)项情形的注册申请,且同种药物尚未获准实行特殊审批的,申请人在已获得基本的临床前药学研究、安全性和有效性数据后,可以在申报临床试验前就特殊审批的申请、重要的技术问题向国家食品药品监督管理局药品审评中心提出沟通交流申请。
第十二条 属于本规定第二条情形的注册申请,申请人在完成某一阶段临床试验及总结评估后,可就下列问题向国家食品药品监督管理局药品审评中心提出沟通交流申请:
(一)重大安全性问题;
(二)临床试验方案;
(三)阶段性临床试验结果的总结与评价。
第十三条 已获准实行特殊审批的注册申请,若在临床试验过程中需作临床试验方案修订、适应症及规格调整等重大变更的,申请人可在完成变更对药品安全性、有效性和质量可控性影响的评估后,提出沟通交流申请。
第十四条 申请人提出沟通交流申请,应填写《新药注册特殊审批沟通交流申请表》(附件2),并提交相关资料。
第十五条 国家食品药品监督管理局药品审评中心对申请人提交的《新药注册特殊审批沟通交流申请表》及相关资料进行审查,并将审查结果告知申请人。
第十六条 国家食品药品监督管理局药品审评中心对同意进行沟通交流的,应明确告知申请人拟讨论的问题,与申请人商定沟通交流的形式、时间、地点、参加人员等,并在告知申请人后1个月内安排与申请人沟通。但对属于本规定第十一条情形的,应在3个月内安排与申请人沟通。
第十七条 沟通交流应形成记录。记录需经双方签字确认,对该新药的后续研究及审评工作具有参考作用。
第十八条 申请特殊审批的申请人,在申报临床试验、生产时,均应制定相应的风险控制计划和实施方案。
第十九条 对在申报临床试验时已获准实行特殊审批的注册申请,申请人在申报生产时仍需按照本规定提交相关资料,但不再进行审查确定,直接实行特殊审批。
第二十条 属于下列情形的,国家食品药品监督管理局可终止特殊审批,并在药品审评中心网站上予以公布。
(一)申请人主动要求终止的;
(二)申请人未按规定的时间及要求履行义务的;
(三)经专家会议讨论确定不宜再按照特殊审批管理的。
第二十一条 当存在发生突发公共卫生事件的威胁时,以及突发公共卫生事件发生后,对突发公共卫生事件应急处理所需药品的注册管理,按照《国家食品药品监督管理局药品特别审批程序》办理。
第二十二条 本规定自发布之日起施行。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。