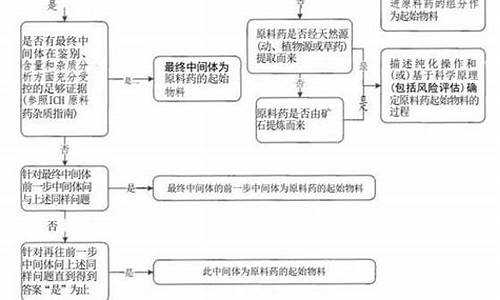
原料药起始物料的定义-原料药起始物料选择依据
例如,片剂在压片后进行内包装,压片结束后检测鉴别、含量均匀度等理化项目,而内包装之后仅取样检测微生物限度,最后成品放行的检验报告数据采用压片之后的理化项目数据和内包装之后的微生物限度数据,这样做是否可行? 答:放行,系指对一批物料或产品进行质量评价,作出批准使用或投放市场或其他决定的操作。一般情况下,如果企业对成品进行质量评价,能够确认中间产品的关键质量属性到成品时未发生变化,中间产品的检验结果能够代表成品放行前的检验结果,则可以引用中间产品的检验数据和结果。 企业如果采用这种方式,则必须对中间产品的关键质量属性到成品状态时的变化情形进行科学研究或评价,确保中间产品的检验数据能够代表最终包装完成的成品。应当注意,并非所有中间体的关键质量属性到最终放行时都不会产生变化。 2.问: 答:《药品生产质量管理规范(2010年修订)》明确要求制剂生产用每批原辅料和与药品直接接触的包装材料均应当有留样,并对留样作出了详细要求,而对于原料药则没有详细规定,但在第十二条(七)中明确规定:物料和最终包装的成品应当有足够的留样,以备必要的检查或检验。 原辅料留样的目的是为了能够有追溯性,一旦上市或未上市产品出现问题,企业能够从物料角度查找分析可能产生的原因。因此,企业还是应当根据其对成品质量影响的情形进行分析,从而决定是否留样、如何留样并形成操作规程。一般而言,原料药生产所用的起始物料、对原料药质量有直接或关键影响的那些关键物料均应当留样。 3.问:我们生产最终灭菌的大容量注射剂,从配制到灭菌的时限,工艺规程描述为不超过12小时,但实际工作中最多也超不过8小时,那么,12小时的时限是否必须要通过验证?8小时的时限也是否必须要通过验证? 答:《药品生产质量管理规范(2010年修订)》第五十七条规定:应当尽可能缩短药液从开始配制到灭菌(或除菌过滤)的间隔时间。应当根据产品的特性及贮存条件建立相应的间隔时间控制标准。 灭菌工艺的有效性不仅与灭菌参数有关,还与待灭菌物品的微生物负荷量有关。建立间隔时间控制标准的目的是为了控制待灭菌产品的微生物负荷量,使灭菌工艺能够达到相应的效果。 药液的微生物负荷量会随着时间的延长而增加。企业根据灭菌工艺能力确定可接受的最大微生物负荷量之后,应根据产品特性和贮存条件考察、建立并控制药液从配制至灭菌的时间,以控制微生物负荷量在可接受的最大范围之内。 问题中工艺规程规定的时限应当是经过验证的。如果最长的12小时时限已经过验证,根据实际工作情况,在其他条件不变的情形下,将时限缩短至8小时可不再验证。 4.问:检验人员须经过与所从事的检验操作相关的实践培训且通过考核。是不是药企的QC只要经过公司内部的岗位培训并考核合格就能上岗,不再需要经过药检或药品监管部门认可的机构培训后发证上岗? 答:《药品生产质量管理规范(2010年修订)》对检验人员提出了要求:质量控制实验室的检验人员至少应当具有相关专业中专或高中以上学历,并经过与所从事的检验操作相关的实践培训且通过考核。 该规范没有强制规定企业的检验人员需经过药检或药监部门认可的机构培训后发证上岗,其注重的是培训的有效性,企业应确保培训后检验人员检验的准确性。企业可采取理论培训、实践培训、或者师傅带徒弟等多种方式,也可以采取委托第三方机构进行培训的方式对检验人员进行培训,但必须注意,培训和考核仅仅是确保检验结果准确性的手段。
中间体与原料药有何区别?
8月26日,天宇股份(300702.SZ)公告称,公司收到美国食品药品监督管理局出具的警告信,认为公司两产品毒性杂质调查、评估系统存在缺陷等问题。
合计来看,三年来,天宇股份两类产品直接或间接出口美国市场的销售金额高达6.53亿元。
天宇股份一直是以出口为导向的企业,2021年,公司外销金额达18.5亿元,同比下滑1.35%,而且外销毛利率为37.69%,同比大幅下滑13.82%。
二级市场上,天宇股份股价也跌跌不休,截至8月29日,公司年内下滑超47%。
就在此时,天宇股份拟花最高1亿元进行回购。但截至2022年一季度,公司货币资金达6.22亿元,短期借款为6.08亿元,手上现金已不算充沛。
涉事两产品三年在美销售额达6.53亿
天宇股份是一家专业从事研发、生产和销售中间体、原料药及制剂业务的医药制造企业。公司由一对来自于浙江台州的夫妻屠勇军和林洁创立,两人合计持有上市公司57.67%股票。
资料显示,天宇股份产品主要涉及降血压、降血糖、抗病毒、抗哮喘、抗凝血等药物,按照业务模式的不同,分为CDMO原料药及中间体、仿制药原料药及中间体、制剂业务。
2021年年报显示,天宇股份产品销往欧盟、印度、韩国、日本、美国等国家和地区。公司与默沙东、诺华、赛诺菲、武田、第一三共、梯瓦、晖致、阿拉宾度等全球大型制剂厂商建立了长期、稳定的合作关系。
然而,8月26日,天宇股份公告称,公司于近日收到美国食品药品监督管理局(简称“FDA”)出具的警告信,该警告信是FDA针对2022年2月28日至3月4日在公司黄岩江口生产场地的现场检查,警告信的缺陷内容包括,2018年沙坦类亚硝胺杂质被发现后,公司未能及时发现后续市场出现的氯沙坦钾中MB-X和LADX两个基毒杂质,认为公司基因毒性杂质调查、评估系统存在缺陷;起始物料尿苷生产设备的清洗验证存在不足。
FDA在警告信中,针对天宇股份提交的整改报告中存在的不足提出整改要求,公司将根据FDA规定的时间及时递交回复报告,具体说明采取的各项整改措施和完成计划,FDA将重新进行现场检查以解除警示。
据了解,警告信涉及的两大产品氯沙坦钾原料药和起始物料尿苷,在近三年里,天宇股份直接或间接出口美国市场的销售金额高达6.53亿元。
天宇股份表示,该警告信目前对公司生产、经营没有造成实质性影响。除氯沙坦钾原料药外,公司暂无其他原料药销往美国市场。
2021年净利大降近70%
从2018年开始,天宇股份的营收增幅均超20%,但到了2021年,这一趋势发生逆转。
2021年,天宇股份实现营业收入25.45亿元,较上年同期下降1.62%;归属于上市公司股东的净利润2.05亿元,较上年同期下降69.32%;归属于上市公司股东的扣除非经常性损益的净利润1.61亿元,较上年同期下降72.85%。
天宇股份表示,2021年公司净利润下滑主要受主营业务毛利下降、研发费用增长、管理费用增长等因素影响。
其中,天宇股份的沙坦类原料药及中间体产品因市场竞争激烈导致产品降价;2021年平均记账汇率6.4477,去年同期平均记账汇率6.9338,同比升值7.01%,影响收入1.39亿元。
同时,天宇股份表示,公司生产规模建设扩大,新投入使用的生产基地产能利用率较低,完工产品分摊的固定成本较高。而且,随着化学基础原料价格持续上涨,公司环保费用支出增加、部分产品生产场地转移、限电限产造成的产能冲击,导致生产成本提高。
具体来看,天宇股份2021年仿制药原料药及中间体实现收入19.64亿元,较上年同期收入24.92亿元下降21.20%。公司表示,主要受沙坦类原料药及中间体市场价格下降、人民币汇率升值等影响。
不过,2021年,天宇股份CDMO业务呈快速增长,营业收入为5.57亿元,同比增长552.65%。公司表示,2021年公司出色完成了默沙东的抗疫新药紧急项目研发,在极短的时间内为客户提供了从研发至商业化的服务,进一步得到了客户的高度认可与信赖。
现金不足仍坚持最高花1亿回购
天宇股份一直是以出口为导向的企业,但2021年以来也出现了下滑。
2021年年报显示,天宇股份外销金额达18.5亿元,同比下滑1.35%,占总营收的72.69%。而且,公司外销毛利率为37.69%,较2020年大幅下滑13.82%。
2022年一季度,天宇股份实现营业收入7.50亿元,同比下滑1.19%;净利润8472.14万元,同比下滑36.52%。同期,公司毛利率进一步下滑至33.51%。
二级市场上,天宇股份股价也跌跌不休,截至8月26日,公司每股股价达25.55元,年内下滑约47%。
7月5日,天宇股份发布回购报告书显示,公司拟使用自有资金以集中竞价交易的方式回购公司部分社会公众股份,用于实施股权激励计划或员工持股计划。
公告显示,天宇股份本次回购总金额在5000万元至10000万元,回购价格不超过人民币49.16元/股。
而且,截至2022年一季度,天宇股份货币资金达6.22亿元,较上年同期9.87亿元减少约37%,但公司短期借款达6.08亿元,较上年同期2.46亿元,同比提高约147%,公司手上现金已不充沛。
8月2日,天宇股份公告称,公司首次通过回购专用证券账户以集中竞价交易方式实施股份回购,回购数量为8万股,占公司目前总股本的0.023%,最高成交价为25.60元/股,最低成交价为25.17元/股,成交总金额为202.84万元(不含交易费用)。
原料和制剂的细菌内毒素限度需要一致吗
中间体是生产某些产品中间的产物,比如要生产一种产品,可以从中间体进行生产,节约成本。与原料其实区别不大,只是需求需要而已,还有进出口问题
我国医药中间体发展迅猛
-------------------------------------------------------------------------------
药品生产需要大量的特殊化学品,这些化学品原来大多由医药行业自行生产,但随着社会分工的深入与生产技术的进步,医药行业将一些医药中间体转交化工企业生产。医药中间体属精细化工产品,生产医药中间体目前已成为国际化工界的一大产业。
有,需要继续控制。原料药是原料药,制剂是制剂。你知道这些杂质是原料药中带入的,只能证明了它的来源。现在对于杂质的要求非常严格,即便是原料药中的杂质也分为:起始物料、中间体或者降解产物等等。看这个吧,超过了报告限度的杂质,是需要出报告的。超过鉴定限度的杂质是需要知道它具体的化学结构的。尤其是你在制剂研究、生产过程中监控这些杂质的增长情况。有些杂质在原料药里增长不明显,做成了制剂就蹭蹭地长。到底是湿度影响,还是酸碱度影响,或者是温度影响。这关系到制剂工艺的问题,另外产品贮藏条件,包装条件都是跟主成分含量以及杂质有关系的。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。












