化学原料药审评审批-化学原料药受理审查指南

法律分析:如果医疗机构擅自配置自制药造成患者损害,应当承担相应的赔偿责任。根据《中华人民共和国药品管理法》的规定,医疗机构配制制剂,须经所在地省、自治区、直辖市人民政府卫生行政部门审核同意,由省、自治区、直辖市人民政府药品监督管理部门批准,发给《医疗机构制剂许可证》。没有《医疗机构制剂许可证》的,不得配制制剂。
法律依据:《中华人民共和国药品管理法》第二十三条对正在开展临床试验的用于治疗严重危及生命且尚无有效治疗手段的疾病的药物,经医学观察可能获益,并且符合伦理原则的,经审查、知情同意后可以在开展临床试验的机构内用于其他病情相同的患者。《中华人民共和国药品管理法》第二十五条对申请注册的药品,药品监督管理部门应当组织药学、医学和其他技术人员进行审评,对药品的安全性、有效性和质量可控性以及申请人的质量管理、风险防控和责任赔偿等能力进行审查;符合条件的,颁发药品注册证书。药品监督管理部门在审批药品时,对化学原料药一并审评审批,对相关辅料、直接接触药品的包装材料和容器一并审评,对药品的质量标准、生产工艺、标签和说明书一并核准。本法所称辅料,是指生产药品和调配处方时所用的赋形剂和附加剂。
四个专项整治内容是什么
开药店要具备这些条件:\x0d\1.营业场地不少于40平方米,仓库不少于20平方米.至少要有一个驻店药师、一个营业员(要高中以上或与药学相关毕业的或经过药监部门考核获得上岗证的人员).\x0d\2.要申办《药品经营许可证》,《医疗器械经营许可证》还要办营业执照,卫生许可证。药店工作人员还要有健康证。新开的药店要施行GSP认证,GSP就是指:药品经营质量管理,一切都要按GSP模式运作。附:按照以下程序办理《药品经营许可证》:\x0d\(一)申办人向拟办企业所在地设区的市级(食品)药品监督管理机构或省、自治区、直辖市(食品)药品监督管理部门直接设置的县级(食品)药品监督管理机构提出筹建申请,并提交以下材料:\x0d\1.拟办企业法定代表人、企业负责人、质量负责人的学历、执业资格或职称证明原件、复印件及个人简历及专业技术人员资格证书、聘书;\x0d\2.拟经营药品的范围;\x0d\3.拟设营业场所、仓储设施、设备情况。\x0d\(二)(食品)药品监督管理机构对申办人提出的申请,应当根据下列情况分别作出处理:\x0d\1.申请事项不属于本部门职权范围的,应当即时作出不予受理的决定,发给《不予受理通知书》,并告知申办人向有关(食品)药品监督管理部门申请;\x0d\2.申请材料存在可以当场更正的错误的,应当允许申办人当场更正;\x0d\3.申请材料不齐或者不符合法定形式的,应当当场或者在5日内发给申办人《补正材料通知书》,一次性告知需要补正的全部内容。逾期不告知的,自收到申请材料之日起即为受理;\x0d\4.申请事项属于本部门职权范围,材料齐全、符合法定形式,或者申办人按要求提交全部补正材料的,发给申办人《受理通知书》。《受理通知书》中注明的日期为受理日期。\x0d\(三)(食品)药品监督管理机构自受理申请之日起30个工作日内,依据本办法第五条规定对申报材料进行审查,作出是否同意筹建的决定,并书面通知申办人。不同意筹建的,应当\x0d\说明理由,并告知申办人依法享有申请行政复议或者提起行政诉讼的权利。\x0d\(四)申办人完成筹建后,向受理申请的(食品)药品监督管理机构提出验收申请,并提交以下材料:\x0d\1.药品经营许可证申请表;\x0d\2.工商行政管理部门出具的拟办企业核准证明文件;\x0d\3.营业场所、仓库平面布置图及房屋产权或使用权证明;\x0d\4.依法经过资格认定的药学专业技术人员资格证书及聘书;\x0d\5.拟办企业质量管理文件及主要设施、设备目录。\x0d\(五)受理申请的(食品)药品监督管理机构在收到验收申请之日起15个工作日内,依据开办药品零售企业验收实施标准组织验收,作出是否发给《药品经营许可证》的决定。不符合条件的,应当书面通知申办人并说明理由,同时,告知申办人享有依法申请行政复议或提起行政诉讼的权利。
根据《新药注册特殊审批管理规定》,可以加快审评审批的新药包括
法律分析:四项专项整治内容包括:一是企业是否严格按照《药品生产质量管理规范》组织中药注射剂生产,重点检查企业是否建立健全药品生产质量管理体系,药品生产过程是否持续符合法定要求;二是中药注射剂是否按国家标准或核准的生产工艺组织药品生产和检验,重点检查企业是否严格按处方成分投料,投料量与实际批量要求是否一致;是否存在擅自添加中药提取物或化学成分,中药材(中药饮片)不投料或少投料,有含量要求的提取物是否折算投料;是否按规定进行药材前处理加工,前处理加工记录内容是否真实、完整可追溯;中药注射剂提取用水是否符合规定要求;提取后的药渣是否按规程进行处理;三是生产所需的原料、辅料是否符合要用要求,是否严格执行供应商审计制度,重点检查企业中药材、中药提取物来源是否合法,是否使用假冒伪劣中药材、中药材非药用部位、购买直接粉碎药粉代替药材和用被污染或提取过的中药材生产药品;外购中药提取物是否有合法资质;四是企业直接接触药品的包装材料和容器是否符合药用要求。
法律依据:《药品管理法》第二十五条:药品监督管理部门在审批药品时,对化学原料药一并审评审批,对相关辅料、直接接触药品的包装材料和容器一并审评,对药品的质量标准、生产工艺、标签和说明书一并核准。《药品管理法》第一百二十五条:违反本法规定,有下列行为之一的,没收违法生产、销售的药品的和违法所得以及包装材料、容器,责令停产停业整顿,并处五十万元以上五百万元以下的罚款;情节严重的,吊销药品批准证明文件、药品生产许可证、药品经营许可证,对法定代表人、主要负责人、直接负责的主管人员和其他责任人员处二万元以上二十万元以下的罚款,十年直至终身禁止从事药品生产经营活动:(二)使用未经审评的直接接触药品的包装材料或者容器生产药品,或者销售该类药品;《药品管理法》第四十六条:直接接触药品的包装材料和容器,应当符合药用要求,符合保障人体健康、安全的标准。对不合格的直接接触药品的包装材料和容器,由药品监督管理部门责令停止使用。
化学药品是怎样分类的?1类、2类、…6类药是怎样区分出来的?
答案:A、B、C、D
实施特殊审批,加快审评审批的新药包括:(1)未在国内上市销售的从植物、动物、矿物等物质中提取的有效成分及其制剂,新发现的药材及其制剂。故A、B正确。(2)未在国内外获准上市的化学原料药及其制剂、生物制品。故C正确。(3)治疗艾滋病、恶性肿瘤、罕见病等疾病且具有明显临床治疗优势的新药。(4)治疗尚无有效治疗手段的疾病的新药。故D正确。
新修订的药品管理法什么时间实施
根据国家药品监督管理局发布的《药品注册管理办法》(局令第28号),化学药品注册的需按照法规对申报药品进行分类。对于化学药品的注册分类共分为6类。原文可下载《药品注册管理办法》(局令第28号)的附件2查看。
1、未在国内外上市销售的药品。细分如下:
(1)通过合成或者半合成的方法制得的原料药及其制剂;
(2)天然物质中提取或者通过发酵提取的新的有效单体及其制剂;
(3)用拆分或者合成等方法制得的已知药物中的光学异构体及其制剂;
(4)由已上市销售的多组份药物制备为较少组份的药物;
(5)新的复方制剂;
(6)已在国内上市销售的制剂增加国内外均未批准的新适应症。
2、改变给药途径且尚未在国内外上市销售的制剂。
3、已在国外上市销售但尚未在国内上市销售的药品。细分如下:
(1)已在国外上市销售的制剂及其原料药,和/或改变该制剂的剂型,但不改变给药途径的制剂;
(2)已在国外上市销售的复方制剂,和/或改变该制剂的剂型,但不改变给药途径的制剂;
(3)改变给药途径并已在国外上市销售的制剂;
(4)国内上市销售的制剂增加已在国外批准的新适应症。
4、改变已上市销售盐类药物的酸根、碱基(或者金属元素),但不改变其药理作用的原料药及其制剂。
5、改变国内已上市销售药品的剂型,但不改变给药途径的制剂。
6、已有国家药品标准的原料药或者制剂。
扩展资料
化学药品制剂行业一直以来都是我国医药工业中的优势子行业,具有高技术含量、高资金投入、高风险、高收益和相对垄断的行业特征。从价值链来讲,化学药品制剂处于价值链高端,按价值递增依次为通用名药(非专利药)和专利药,专利药是整个价值链的顶端。
化学药品制剂涉及国民健康、社会稳定和经济发展,是国民经济一个特殊而重要的产业。改革开放30年以来,我国化学药品制剂工业的发展驶入快车道,近几年的工业总产值增长率都保持在18%以上,销售收入增长率基本保持在20%以上。
从发展趋势看,化学药品制剂行业即将进入快速发展期,未来发展空间巨大,但利润分配将更加不均衡,行业集中度将进一步提高,具有研发、规模和产品优势的企业将强者恒强。
中国化学药品制剂行业已经完全发展成为一个竞争性的行业,在国际上的影响力也有所提高。在中国内地,外资及合资制药企业与内资制药企业之间的市场竞争非常激烈,尤其是近两三年,外资及合资企业大幅增加在华投资,强化市场力度。
截至2011年底,中国大陆规模以上的化学药品制剂企业有1032家,经过快速发展阶段和激烈的市场竞争的锤炼,基本格局初步形成。外资及合资制药企业占据着中国化学药品制剂的高端市场,但内资品牌也正在逐步进军高端。
百度百科:化学药品
因违反《药品管理法》规定,给药品使用者造成损害的,应承担什么责任
2019年8月26日,新修订的《中华人民共和国药品管理法》经十三届常委会第十二次会议表决通过,于2019年12月1日起施行。
药品管理法具体的一些制度主要有:
一是明确了鼓励方向,重点支持以临床价值为导向,对人体疾病具有明确疗效的药物创新。鼓励具有新的治疗机理,治疗严重危及生命的疾病、罕见病的新药和儿童用药的研制。
二是创新审评机制,强化审评机构能力建立,完善与注册申请人的沟通交流机制,建立专家咨询制度,优化审评流程,提高审评效率,为药物创新提供了组织保障。
三是优化了临床试验管理,过去临床试验审批是批准制,改为了默示许可制,临床试验机构的认证管理调整为备案管理,提高了临床试验的审批效率。
四是建立关联审评审批,在审评审批药品的时候,将化学原料药、相关的辅料和直接接触药品的包装材料和容器调整为与制剂一并审评审批,同时对药品质量标准、生产工艺、标签和说明书也一并核准。
五是实行了优先审评审批,对临床急需的短缺药、防治重大传染病和罕见病等疾病的新药、儿童用药开设绿色通道,优先审评审批。
六是建立了附条件审批的制度。就是对于治疗严重危及生命且尚无有效治疗手段的疾病,以及公共卫生方面急需的药品,临床试验已有数据显示疗效,并且能够预测临床价值的可以附条件审批,以提高临床急需药品的可及性,这个制度缩短了临床试验的研制时间,使那些急需治疗的患者能第一时间用上新药。
新药上市申请受理到上市要多久
应承担民事赔偿责任。药品的生产企业、经营企业、医疗机构违反本法规定,给药品使用者造成损害依法承担赔偿责任。药品也是一种产品,《药品管理法》作为管理药品质量的特别法,对药品的产品质量责任问题未作特殊规定,根据法学的一般原理,特别法未作特殊规定的,应当遵守一般法的规定。
法律分析
药品的产品质量责任问题,应当根据有关法律对产品质量责任问题的一般规定来进行处理;对于因为药品的质量方面的问题,而给药品的使用者造成损害的,药品的生产企业、经营企业和医疗机构应与其他产品的生产者、销售者一样,依据有关法律的规定,承担相应的民事赔偿责任。根据有关法律的规定,因为药品的质量问题而产生的民事赔偿责任主要包括以下两个方面:(1)瑕疵担保责任。对于不具备产品应当具备的使用性能而事先未作说明、不符合在产品或者其包装上注明采用的产品标准或不符合以产品说明、实物样品等方式表明的质量状况的药品,药品生产企业、经营企业和医疗机构应当赔偿因此给药品使用者造成的损失;(2)因产品存在缺陷造成他人损害的特殊民事侵权责任即通常所谓的产品责任。对于存在危及人身、他人财产安全的不合理的危险的产品,如果该产品造成了药品使用者的人身或该产品以外的其他财产损害的,药品的生产企业、经营企业和医疗机构要承担相应的民事赔偿责任。
法律依据
《中华人民共和国药品管理法》 第二十五条 对申请注册的药品,药品监督管理部门应当组织药学、医学和其他技术人员进行审评,对药品的安全性、有效性和质量可控性以及申请人的质量管理、风险防控和责任赔偿等能力进行审查;符合条件的,颁发药品注册证书。药品监督管理部门在审批药品时,对化学原料药一并审评审批,对相关辅料、直接接触药品的包装材料和容器一并审评,对药品的质量标准、生产工艺、标签和说明书一并核准。本法所称辅料,是指生产药品和调配处方时所用的赋形剂和附加剂。
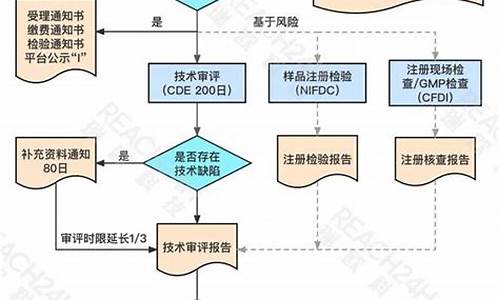
法律分析:根据现行药品注册管理办法和相关政策,根据审评类型不同,一般在中国从新药上市申请及相关资料递送国药监的审评中心并获得受理通知书之日起算,大约在180到240个工作日(大概一年到一年半的样子)左右完成审评事项并发布药品上市许可。这里的许可是指持证方可以生产并销售药品。这里的许可是指持证方可以生产并销售药品。至于药品在市场上可销售或者在医院里可以被处方,还要看药厂市场销售团队的水平,平均的话大概要再加3到6个月。
法律依据:《中华人民共和国药品管理法》
第二十四条 在中国境内上市的药品,应当经药品监督管理部门批准,取得药品注册证书;但是,未实施审批管理的中药材和中药饮片除外。实施审批管理的中药材、中药饮片品种目录由药品监督管理部门会同中医药主管部门制定。申请药品注册,应当提供真实、充分、可靠的数据、资料和样品,证明药品的安全性、有效性和质量可控性。
第二十五条 对申请注册的药品,药品监督管理部门应当组织药学、医学和其他技术人员进行审评,对药品的安全性、有效性和质量可控性以及申请人的质量管理、风险防控和责任赔偿等能力进行审查;符合条件的,颁发药品注册证书。药品监督管理部门在审批药品时,对化学原料药一并审评审批,对相关辅料、直接接触药品的包装材料和容器一并审评,对药品的质量标准、生产工艺、标签和说明书一并核准。本法所称辅料,是指生产药品和调配处方时所用的赋形剂和附加剂
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。