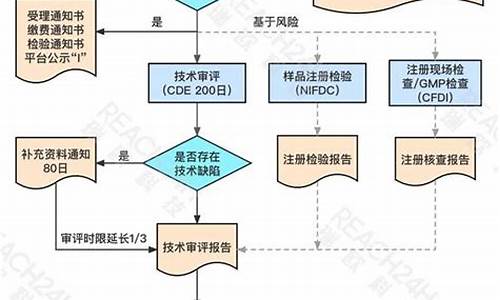
原料药注册至少要几步反应-原料药注册管理办法最新

你仔细研究一下《药品注册管理办法28号令》
如果是新药,没有原料药批文的话,那你是原料和制剂要一起申报的了。
如果已经有制剂了,那你的原料药注册大概要按新药注册流程来做,但不算新药了吧
仅供参看。
药品注册管理事项按什么原则划分
法律分析:1、未在国内上市销售的来源于植物、动物、矿物等药用物质制成的制剂和从中药、天然药物中提取的有效成份及其制剂;
2、未在国内外获准上市的化学原料药及其制剂、生物制品;
3、抗艾滋病病毒及用于诊断、预防艾滋病的新药,治疗恶性肿瘤、罕见病等的新药;
4、治疗尚无有效治疗手段的疾病的新药。
法律依据:《药品注册管理办法(试行)》 第四十九条 国家药品监督管理局对下列新药申请可以实行快速审批:
(一)未在国内上市销售的来源于植物、动物、矿物等药用物质制成的制剂和从中药、天然药物中提取的有效成份及其制剂;
(二)未在国内外获准上市的化学原料药及其制剂、生物制品;
(三)抗艾滋病病毒及用于诊断、预防艾滋病的新药,治疗恶性肿瘤、罕见病等的新药;
(四)治疗尚无有效治疗手段的疾病的新药。
原料药生产企业获得化学原料药批准通知书时,经核准的哪几个注册
1、按照《药品注册管理办法》(2020年1月22日国家市场监督管理总局令第27号公布)实施划分。
2、
《药品注册管理办法》里对药品注册的定义如下:药品注册,是指药品注册申请人(以下简称申请人)依照法定程序和相关要求提出申请,药品监督管理部门对拟上市药品的安全性、有效性、质量可控性等进行审查,作出行政许可决定的过程。
药品注册申请包括药物临床试验申请,药品上市许可申请、上市后补充申请及再注册申请。
简而言之,药品注册就是申请人(现阶段主要是指医药企业)向国家药品监督管理局(NMPA)提出药品注册申请,NMPA审查后给出药品行还是不行的一个过程。这里比较重要的地方就是,NMPA在审评过程中重点关注的是药品的安全性、有效性和质量可控性。医药研发的各项工作,其实就是向NMPA证明药品安全、有效、质量可控的过程。大家在去关注某个公司的药品最后能否顺利上市的时候,也只需要去重点关注药品的这三个方面就可以了。当然,具体如何去从这三个方面进行评估,我们在后面的文章里还会再展开讨论,这里就不再赘述。
3、药品注册分类
当前国内的药品主要分为以下几类:
化学药品:小分子药物;
治疗用生物制品:治疗用途的大分子;
预防用生物制品:主要就是疫苗;
中药、天然药物:中药材、中药提取物、中成药等等。
4、概括来说,注册分类主要需要把握以下几点:
1类创新药:研发难度较大,上市成功率较低,研发投入也大,研发周期平均在10年左右,一旦成功,将带来丰厚的回报。现在看来,国内企业对于创新药的预期相对还是偏乐观,对风险的考虑不足。历史原因再加上国内的行业环境,国内医药企业研发很少会主动宣告临床研发失败。我们在实际评估时,需要特别关注企业重要产品的临床研发进度。从逻辑上讲,如果临床进度落后于预期太多,这里面大概率是存在没有批露的问题的。
2类改良型新药:大多是原研厂家为了延长自己产品的生命周期推出的新一代产品。研发难度相对较低,上市成功概率较大。评估的核心在于是否具有临床优势,做得好可以成神。
3类仿制药:化药仿制药,“4+7”背景下,化药仿制药的逻辑除了抢首仿外,成本优势可以说是生攸关。控制成本的前提下,企业规模和原料药优势就愈发重要。未来,仿制药厂和原料药厂的并购可能会成为常态。生物类似物,因为还有较高的研发壁垒,成功上市后,短期内价格应该也不会像化药仿制药一样进入肉搏战。企业凭借领先的研发效率,还是可以获得相对长时间的竞争优势。
原料药可以委托生产吗
请问您问的是“原料药生产企业获得化学原料药批准通知书后,经核准需要哪几个注册”这个问题吗?该类企业经核准需要的注册如下:
1、药品生产企业需要按照《药品注册管理办法》等相关法规和规定。
2、药品生产企业需要持有《药品生产许可证》。
3、药品生产企业需要持有《药品GMP证书》,这证明企业的生产过程符合药品生产的要求。
根据《药品注册管理办法》,药品注册事项不包括
法律分析:部分不可以,国家明确有规定的。品、精神药品、药品类易制毒化学品及其复方制剂,医疗用毒品,生物制品,多组分生化药品,中药注射剂和原料药不得委托生产。国家食品药品监督管理总局可以根据监督管理工作需要调整不得委托生产的药品。最大的原因是,原料药没有批文,批件上市持有人持有。
法律依据:《药品生产监督管理办法》 第七条 从事制剂、原料药、中药饮片生产活动,申请人应当按照本办法和国家药品监督管理局规定的申报资料要求,向所在地省、自治区、直辖市药品监督管理部门提出申请。委托他人生产制剂的药品上市许可持有人,应当具备本办法第六条第一款第一项、第三项、第五项规定的条件,并与符合条件的药品生产企业签订委托协议和质量协议,将相关协议和实际生产场地申请资料合并提交至药品上市许可持有人所在地省、自治区、直辖市药品监督管理部门,按照本办法规定申请办理药品生产许可证。申请人应当对其申请材料全部内容的真实性负责。
根据《药品注册管理办法》,药品注册事项不包括认证事项。
药品注册申请包括新药申请、已有国家标准的药品申请、进口药品申请和补充申请。
1、新药申请:是指未曾在中国境内上市销售的药品的注册申请。已上市药品改变剂型、改变给药途径、增加新适应症的,按照新药申请管理。
2、已有国家标准的药品申请:是指生产国家食品药品监督管理局已经颁布正式标准的药品的注册申请。
3、进口药品申请:是指境外生产的药品在中国境内上市销售的注册申请。
4、补充申请:是指新药申请、已有国家标准的药品申请或者进口药品申请经批准后,改变、增加或取消原批准事项或者内容的注册申请。
5、进口药品注册:如果境外生产企业在中国没有合法办事机构,必须委托中国的专业机构代理注册。
6、再注册申请:指药品批准证明文件有效期满后,申请人拟继续生产或进口该类药品的注册申请。
国家药品监督管理局对下列新药申请可以实行快速审批:?
1、未在国内上市销售的来源于植物、动物、矿物等药用物质制成的制剂和从中药、天然药物中提取的有效成份及其制剂;
2、未在国内外获准上市的化学原料药及其制剂、生物制品;?
3、抗艾滋病病毒及用于诊断、预防艾滋病的新药,治疗恶性肿瘤、罕见病等的新药;?
4、治疗尚无有效治疗手段的疾病的新药。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。