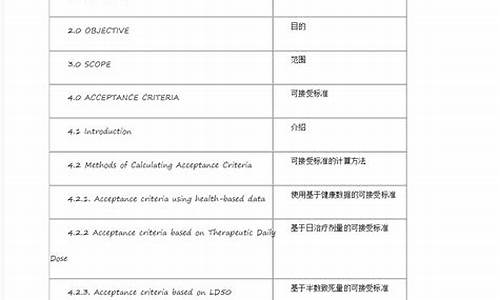
原料药与制剂的含量测定方法-原料药和制剂含量测定的范围

国家药品标准的主要内容有品名、有机药物的结构式、分子式和分子量、来源或有机药物的化学名称、含量或效价的规定、处方、制法、性状、鉴别、检查、含量或效价测定、类别、规格、贮藏及制剂等。
药品质量标准中含量或效价的规定又称为含量限度。含量限度是指用规定的检测方法测得的有效物质含量的限度。
对于原料药,用“含量测定”的药品,其含量限度均用有效物质的百分数(%)表示,此百分数均系指重量百分数。为了能正确反映药品的含量,一般应通过检查项下的“干燥失重”或“水分”,将药品的含量换算成千燥品的含量;用“效价测定”的抗生素或生化药品,其含量限度用效价单位(国际单位IU)表示。
对于制剂,含量(效价)的限度一般用含量占标示量的百分率来表示。
请教盐酸盐类原料药和制剂杂质计量方式
方法的验证:
订入质量标准的含量测定法不同于一般质量考察的方法,须经过严格的方法学验证,不同原理的测定法具有不同的验证内容及要求:
(1)容量分析法的验证:①精密度:用原料药精制品考察方法精密度,平行试验5个样本的RSD≤0.2%;②准确度:以测定原料精制品(含量>99.5%)的回收率(测定值与理论值的比值)计算,应在99.7%~100.3%之间(n=5,RSD≤0.1%);③滴定终点确定的依据:包括滴定曲线的绘制,如用指示剂法确定终点,应用电位法校准终点颜色,提供指示剂颜色与电位变化情况的对比结果;④耐用性:考察测定条件(供试液稳定性、样品提取次数、时间等)有微小变动时,测定结果不受影响的承受程度,如测试条件要求苛刻时则应在方法中注明。
(2)HPLC法的验证:①精密度:RSD≤2%(n=5);②准确度:用于制剂时,要考察辅料的影响,将一定量药物加到按处方比例配制的辅料中(为标示量的80%~120%)制成高、中、低三个剂量,混合均匀后,每个剂量取三份样品,按拟定方法测定回收率,应在98%~102%之间(n=9,
RSD≤2%)。③线性范围:用已知含量的精制品配制一系列浓度的溶液(n=5~7),用浓度C对峰面积A或峰或被测物的响应值之比进行回归处理,线性方程的相关系数r≥0.999,截距应趋于零,并提供线性关系图;④专属性:辅料、有关物质或降解产物峰对主药峰应无干扰;⑤耐用性:考察测定条件(供试液稳定性、流动相组成和pH值、不同品牌或批号的同类色谱柱、柱温、流速、样品提取次数、时间等)有微小变动时,测定结果不受影响的承受程度,如测试条件要求苛刻时则应在方法中注明;⑥灵敏度:作为常量分析法,此项可不作主要要求。
(3)UV法的验证:①精密度:RSD≤1%(n=5);②准确度:方法同HPLC法,回收率应在98%~102%之间(n=9,
RSD≤2%),同时要求辅料、有关物质或降解产物在测定波长处无吸收。③线性范围:用已知含量的精制品配制一系列浓度的溶液(n=5~7,吸收度A在0.2~0.7间),用浓度C对峰面积A或峰或被测物的响应值之比进行回归处理,线性方程的相关系数r应≥0.999,截距应趋于零,并提供线性关系图;④耐用性:考察测定条件(供试液稳定性、样品提取次数、时间、比色法中显色剂用量、反应温度、时间、pH值等)有微小变动时,测定结果不受影响的承受程度,如测试条件要求苛刻时则应在方法中注明;⑤灵敏度:作为常量分析法,此项可不作主要要求。
吸收度A在0.2~0.8间其线形关系好,利用标准品建立标准曲线后,受测溶液做适当的稀释,使其吸收度在0.2~0.8,如果太小或太大,都将影响测定的准确性的。
您好,原料药中采用盐酸盐对应盐酸盐,制剂中采用游离碱对应游离碱,这样做的结果就是,原料药和制剂方法学(校正因子等)不一致,杂质检测结果不一致,限度不一致(比如原料药中杂质A不得过0.1%说的是盐酸盐,制剂中杂质A不得过0.1%说的是游离碱,而且他们所对应的基数也不同,原料药中说的是盐酸盐,制剂中说的是主成分游离碱),具体的可以查看药智网,回答满意请您采纳,谢谢,
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。