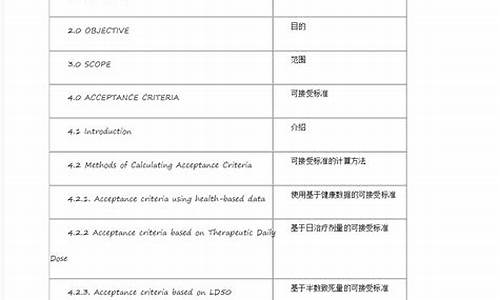
gmp原辅料要求-原料药gmp附录

原料药,通俗点讲是药品的原材料。而我们平时所吃的药品是经过加工后的成品药。
这里针对西药和中成药来讲:每一种药都有它的原料药。
例:
新康泰克
药品名称
通 用 名:复方盐酸伪麻黄碱缓释胶囊
商 品 名:新康泰克(CONTAC NT)
成份本品为复方制剂,每粒含盐酸伪麻黄碱90毫克; 马来酸氯苯那敏
(扑尔敏)4毫克。辅料为:淀粉、蔗糖、羟丙基甲基纤维素、乙基纤维素聚合物、欧巴代**干喷料、欧巴代粉红色干喷料。
其中:盐酸伪麻黄碱90毫克;就是此产品的主要原料药。
原料药在中国主要是由具有GMP证书的生产企业提供的,只有要生产资质的都可以进行生产和供应。
兽药化学原料药GMP申报材料递交何处
GMP的依据是《药品管理法》及其实施条例,其中对此有规定,见下述内容:
第十一条
生产药品所需的原料、辅料,必须符合药用要求。
第四十八条 禁止生产(包括配制,下同)、销售假药。
有下列情形之一的药品,按假药论处:
(五)使用依照本法必须取得批准文号而未取得批准文号的原料药生产的;
第四十九条 禁止生产、销售劣药。
药品成分的含量不符合国家药品标准的,为劣药。
有下列情形之一的药品,按劣药论处:
(四)直接接触药品的包装材料和容器未经批准的;
(五)擅自添加着色剂、防腐剂、香料、矫味剂及辅料的;
请我跟您们做顾问嘛!呵呵。一般是先交省局,然后再经省局提交给农业部。原料药GMP申报资料一般交省局2份(自己留4份,开首次末次会议用)。
第四条 新建(含已获得兽药生产许可证的企业拟新增产品剂型的)或改扩建的兽药GMP企业,应当提出兽药GMP检查验收申请。
第五条 申请兽药GMP检查验收的企业应当填报《兽药GMP检查验收申请表》(见附录1),并按以下要求向兽药GMP办公室报送书面及电子文档的申报资料各一份(其中电子文档应填齐生产和检验管理文件的全部内容):
(一)新建企业
1.企业概况;
2.拟生产兽药类别、剂型及产品目录;
3.企业组织机构图(须注明各部门名称、负责人、职能及相互关系);
4.企业负责人、部门负责人简历;专业技术人员及生产、检验、仓储等工作人员登记表(包括文化程度、学历、职称等),并标明所在部门及岗位;高、中、初级技术人员占全体员工的比例情况表;
5.企业周边环境图;总平面布置图;仓储平面布置图;质量检验场所平面布置图及仪器设备布置图;
6.生产车间概况及工艺布局平面图(包括更衣室、盥洗间、人流和物流通道、气闸等,人流、物流流向及空气洁净度级别);空气净化系统的送风、回风、排风平面布置图;工艺设备平面布置图;
7.拟生产兽药产品的工艺流程图、主要过程控制点和控制项目及产品的生产、质量管理文件目录;
8.生产的关键工序、主要设备、制水系统、空气净化系统、检验仪器设备及产品工艺验证报告;
9.检验用仪器仪表、量具、衡器校验情况报告;
10.农业部认可实验室出具的洁净室检测报告书;
11.其他兽药GMP管理文件目录及与文件相对应的记录、凭证样张;
12.生产设备设施、检验仪器设备目录(需注明规格、型号、主要技术参数);
13.兽药GMP运行情况报告;
14. 试产兽药国家标准产品的批生产、批检验记录复印件(每条生产线应选择具有剂型代表性的2--4个品种,每个品种至少3个批次的记录;少于2个品种或者属于特殊产品及原料药品的,应提供所生产品种的记录)。
(二)改扩建企业
除提供上述1至13项资料外,还须提供以下资料:
1.《兽药生产许可证》和《企业法人营业执照》复印件;
2.企业自查情况(包括企业概况、GMP实施情况等);
3.已获批准生产的产品目录和产品生产、质量管理文件目录及产品标准执行情况、产品批准文件(包括产品批准文号批件、质量标准的复印件等);
4.兽药GMP运行情况报告及批生产、批检验记录复印件(同上款“(一)14.”要求)。
第六条 兽药GMP办公室在收到申报资料之日起20个工作日内完成资料的审查工作。通过审查的,组织现场检查验收工作。审查不合格的,书面通知申请企业在4个月内补充有关资料,逾期未报送的按撤回申请处理。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。