三氟苯甲酸-3氟苯甲酰乙酸乙酯厂家有哪些

国标里面测定苯甲酸,糖精钠的方法有哪些
邻苯甲酰磺酰亚胺C7H5O3NS
1,1,3-三氧代-2,3-二氢-苯并[d]异噻唑
白色结晶粉末。熔点228.8~229.7℃,密度0.828克/立方厘米,微溶于水、和氯仿,溶于乙醇、乙酸乙酯、苯和丙酮。它的钠盐称做糖精钠或溶性糖精,易溶于水,稀水溶液的甜味约为蔗糖的300~500倍。少量无毒,但无营养价值。
糖精钠是有机化工合成产品,是食品添加剂而不是食品,除了在味觉上引起甜的感觉外,对人体无任何营养价值。相反,当食用较多的糖精时,会影响肠胃消化酶的正常分泌,降低小肠的吸收能力,使食欲减退。目前JECFA规定糖精的ADI值为每日每千克体重0~5mg。
氟虫腈在家禽上的应用谁知道,具体传授一下。
左氧氟单酯 中文别名:2,3,4,5-四氟苯甲酰乙酸乙酯;2,3,4,5-四氟苯甲酰乙酸乙脂 保隆化工有tel576-88702853 ETHYL 2,3,4,5-TETRAFLUOROBENZOYL ACETATE CAS号:94695-50-8
果尔除草剂怎么用,可以详细点最好
我国目前已经成为全球主要农药生产与消费国家之一,但是生产品种主要以传统和仿制的中低档品种为主。我国农药生产与开发与发达国家和地区相比存在相当的差距,尤其是技术开发水平低,新农药的创制与开发本身难度大、周期长、投入大;尽管经过多年研究与开发,我国已经开发出部分拥有自主知识产权的创制农药,但是真正走入市场的并不多;面对如此局面,我国农药除加大创制研发力度外,还应高度重视开发一些具有市场前景的专利过期或即将过期的重要农药品种。本文将主要介绍一些专利过期不久或即将过期的一些重要农药品种及其合成所需中间体开发与生产情况,为国内开发与生产这些农药及中间体提供参考。
1 氟虫腈(fipronil)
由法国罗纳-普朗克公司开发,获中国专利授权(CN86108643),该化合物专利在2006年12月19日到期;同时,拜耳公司对氟虫腈及其中间体的制备方法也在我国获得专利授权(CN95100789.0),此项专利的有效期将持续到2015年。
氟虫腈是一种苯基吡唑类广谱杀虫剂,主要是阻碍昆虫γ-氨基丁酸控制的氟化物代谢,具有触杀、胃毒和中度内吸作用,对鳞翅目、蝇类和鞘翅目等一系列害虫具有很高的杀虫活性,与现有杀虫剂无交互抗性。氟虫腈2005年全球销售额为4.2亿美元,在杀虫剂品种销售额排名第4。
目前氟虫腈工业化生产合成路线主要有两条,一是以2,6-二氯-4-三氟甲基苯胺为原料,经过重氮化得到重氮盐,再与2,3-二氰基丙酸乙酯反应得到;二是以2,6-二氯-4-三氟甲基苯肼为原料与富马腈反应,再氧化得到产品。
1.1 2,6-二氯-4-三氟甲基苯胺
2,6-二氯-4-三氟甲基苯胺主要合成路线有三条:①对三氟甲基苯胺法。对三氟甲基苯胺在溶剂中直接氯化得到2,6-二氯-4-三氟甲基苯胺。该法简单方便,但是对三氟甲基苯胺价格较贵,生产成本比较高,国外主要采用该法生产。②对氯三氟甲苯法。对氯三氟甲苯与二甲基甲酰胺和NaNH2在一定温度和压力下反应得到N,N-二甲基对三氟甲基苯胺,然后在光照下氯化,脱甲基并环上氯化得到目的产品。该法步骤较长,''三废''量较大。③3,4-二氯三氟甲苯法。以3,4-二氯三氟甲基苯胺为原料,与二甲基甲酰胺及氢氧化钠在压力釜中反应,在光照条件下氯化脱甲基并环上氯化得到产品。目前国内多家科研机构研究与开发此路线。此路线更趋于合理,产品质量高,''三废''量有一定减少。
1.2 2,6-二氯-4-三氟甲基苯肼
目前研究主要方向是以对氯三氟甲基苯为原料,在三氯化铁存在下深度氯化得到3,4,5-三氯三氟甲苯,然后与水合肼反应得到2,6-二氯-4-三氟甲基苯肼。
1.3 2,3-二氰基丙酸乙酯
2,3-二氰基丙酸乙酯合成方法,主要有分步法和一步法两种。分步法生产过程较为繁琐,生产过程中产生对人体有害的剧毒品且''三废''量比较大,因此目前主要采用一步法生产。一步法合成工艺为:将和溶剂无水乙醇混合,充分溶解后,加入多聚甲醛,溶解后接着加入氰乙酸乙酯,、多聚甲醛、氰乙酸乙酯投料比例为1:1:0.91(m:m)。然后使用盐酸酸化后,再经过萃取水洗得到粗品,最后精馏去除溶剂得到产品。目前国内泰州天源化工有限公司等数家企业采用该法生产2,3-二氰基丙酸乙酯。
2 溴虫腈(chlorfenapyr)
由美国氰胺公司开发,获中国专利授权(CN88106516.1),该专利将在2008年7月28日到期。德国巴斯夫公司在中国获得虫螨腈原药和10%虫螨腈悬浮剂临时登记。目前国内江苏龙灯化学有限公司和广东德利生物科技公司有相关登记。
溴虫腈是一种新型吡咯类广谱杀虫杀螨剂,在植物表面渗透性强,有一定内吸活性,兼有胃毒和触杀作用,可以防治多种鳞翅目、双翅目、鞘翅目、半翅目害虫和螨类,并可有效防治对氨基甲酸酯类、有机磷类和拟除虫菊酯类杀虫剂产生抗性的昆虫。
溴虫腈的合成方法主要有:①2-对氯苯基-5-三氟甲基吡咯-3-腈在光照下与溴反应,再与乙醇钠反应得到;②芳基吡咯腈在叔丁醇钾作用下,在四氢呋喃中与氯甲基乙基醚反应;③芳基吡咯腈在DMF、三氯氧磷、三乙胺存在下与二乙氧基甲烷反应得到。其中主要中间体为芳基吡咯腈,国内外研究主要集中以2-对氯苯基-5-三氟甲基吡咯-3-腈为原料的路线上。2.1 2-对氯苯基-5-三氟甲基吡咯-3-腈
有关芳基吡咯-3-腈专利报道比较多,国外公司一般采用2-对氯苯基甘氨酸为原料,三氟乙酸酐为三氟乙酰化剂,并关环成4-对氨基苯基-2-三氟甲基吡唑啉-5-酮,再与2-氯丙烯腈反应生成2-对氯苯基-5-三氟甲基吡咯-3-腈。国外在我国申请不少专利,如有三氯化磷和三乙胺存在下用三氟乙酸进行三氟乙酰化,或用三氟乙酰氯代替三氟乙酸反应的,也有选择合适的极性溶剂和碱等。
国外也有研究人员采用对氯苯基三氟乙酰胺基腈为原料,在酸存在下与酰卤反应生成恶唑胺的酰化衍生物,继而在碱性条件下与2-氯丙烯腈反应得到2-对氯苯基-5-三氟甲基吡咯-3-腈。
国内许多科研机构也进行了大量研究,如郑州大学和大连理工大学,以对氯苄胺为基础原料,在三氯化磷存在下与三氯乙酸反应,三氟乙酰化得到N-对氯苄基三氟乙酰胺;然后在三氯氧磷存在下通过氯化得到对氯苄基氯三氟乙酰亚胺;在碱的存在下对氯苄基氯三氟乙酰亚胺与氯代丙烯腈发生1,3偶极环加成反应,区域定向性地得到2-对氯苯基-5-三氟甲基吡咯-3-腈。该路线尽管步骤比较多,但是原料价廉易得,国此具有较高的应用开发价值。
国内还有一些文献报道以对氯苯基氨基丙烯腈经过溴化后与三氟甲基丙酮环合得到2-对氯苯基-5-三氟甲基吡咯-3-腈,尽管该法简单,但是原料来源比较困难。
3 四氟苯菊酯(transfluthrin)
该品种由拜耳公司开发,获中国专利授权(CN88100834),该专利将在2008年2月11日到期。拜耳公司在我国获得拜奥灵原药的临时登记,国内相关登记企业有江苏常州康泰化工有限公司和扬农化工股份有限公司。四氟苯菊酯是一种高效、低毒的卫生用拟除虫菊酯杀虫剂,具有吸入、触杀和驱避活性,对蚊虫具有快速击倒作用,用作多种蚊香、驱蚊片的原料,也可以有效防治苍蝇、蟑螂和白粉虱,其药效远高于烯丙菊酯。由于常温下的饱和蒸气压比较高,四氟苯菊酯还可用于制备野外和旅游用的杀虫产品,从而将卫生杀虫剂的应用从室内拓展到室外。
四氟苯菊酯合成主要是以2,3,5,6-四氟苄醇为原料,在甲苯作为溶剂的情况下与吡啶和二氯菊酰氯进行反应制得。其中四氟苄醇为关键的中间体,二氯菊酰氯则为多种拟除虫菊酯通用型中间体,国内山东大成农药化工股份有限公司等多家企业已经生产,因此主要介绍关键中间体四氟苄醇的合成。
四氟苄醇合成难度比较大,国外文献报道主要有两条路线生产:①采用四氟苯甲酸或者四氟苯甲醛为原料合成四氟苄醇,如欧洲专利介绍,以1,2,4,5-四氟苯与正丁基锂反应,然后与二氧化碳作用制备2,3,5,6-四氟苯甲酸,再利用LiAlH4还原制备2,3,5,6-四氟苄醇。该法过程相对比较简单,但是反应条件苛刻,原料来源比较困难;②日本和国内一些专利文献报道则采用2,3,5,6-四氯对苯二腈为原料合成四氟苄醇。具体过程以二甲基甲酰胺以为溶剂,四氯对苯二腈与无水氟化钾进行亲核取代反应,生成2,3,5,6-四氟苯腈;然后在80%浓硫酸存在下,四氟苯腈进行水解反应得到四氟对苯二甲酸;四氟对苯二甲醇在三丁胺和氢氧化钠存在下发生脱羧反应得到四氟苯甲酸;四氟苯甲酸在甲苯作为溶剂的情况下,与氯化亚砜发生酰氯化反应得到四氟苯甲酰氯,在四氢呋喃作为溶剂的情况下,四氟苯甲酰氯与硼氢化钠催化还原得到四氟苄醇。
目前国内江苏扬农化工股份有限公司和江苏激素研究所等能够生产四氟苄醇。
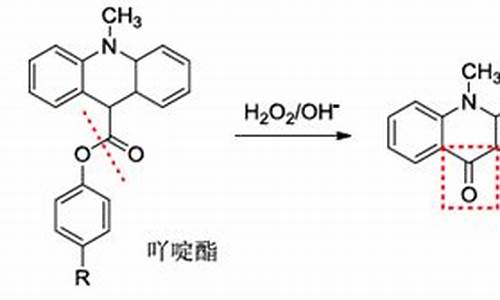
4 唑螨酯(fenpyfoximate)
该品种由日本农药株式会社开发,获中国专利授权(CN86108691),此专利于2006年12月26日到期。日本农药株式会社还在中国获得唑螨酯原药、13%炔螨•唑螨水乳剂等多种产品登记。国内山东栖霞通达化工有限公司和江苏龙灯化学有限公司也有制剂登记。
唑螨酯是一种苯氧吡唑类杀螨剂,高剂量时可以直接杀螨类,低剂量可以抑制类蜕皮或者产卵,具有击倒和抑制蜕皮作用,无内吸作用,可以防治多种螨类,尤其是多种果树上的叶螨和红蜘蛛,对幼螨和若螨具有优良活性,对天敌比较安全,对蜜蜂无不良影响,对家蚕有拒食作用。
唑螨酯合成主要以1,3-二甲基吡唑酮-5为原料,经过1,3-二甲基-5-氯吡唑甲醛-5、1,3-二甲基-5-苯氧基吡唑甲醛-5得到1,3-二甲基-5-苯氧基吡唑肟-5,然后与中间体对氯甲基苯甲酸叔丁酯进行反应得到唑螨酯。其中重要的中间体为1,3-二甲基吡唑酮-5和对氯甲基苯甲酸叔丁酯。
4.1 1.3-二甲基吡唑酮-5
国内外文献报道吡唑酮合成主要采用无水甲基肼,并以无水乙醇或甲醇作为溶剂进行吡唑酮的环化反应。由于无水甲基肼价格昂贵,且运输和使用也极不安全,国内研究人员选用了甲基肼水溶液为起始原料合成1,3-二甲基吡唑酮-5,具体过程为:40%甲基肼水溶液与乙酰乙酸乙酯在75℃下进行环化反应得到粗1,3 -二甲吡唑酮-5,产物经过重结晶纯化。
国外专利文献也介绍了1,3-二甲基吡唑酮-5的其他合成方法:①以水为反应介质,用氢氧化钠的水溶液中和硫酸甲基肼,不分离出中和产生的硫酸钠副产物,直接和乙酰乙酸乙酯反应,得到产物;但是收率比较低;②以乙醇为反应介质,用氢氧化钠的乙醇溶液中和硫酸甲基肼,不分离副产物,直接与乙酰乙酸乙酯反应,得到1,3-二甲基吡唑酮-5,收率比较高。
4.2 对氯甲基苯甲酸叔丁酯
该中间体合成相对比较简单,工业化生产一般以叔丁醇为原料,与吡啶和对氯甲基苯甲酰氯在室温下进行反应,反应后加入一定量的水,然后用甲苯萃取有机相,分离出有机层后进行蒸馏脱去甲苯,得到对氯甲基苯甲酸叔丁酯,进一步纯化得到精制产品。
5 嘧菌酯(azoxystrobin)
该品种是由先正达开发,获中国专利授权(CN1047286),该专利将于2010年2月8日到期。在美国、欧洲、日本等数十个国家有登记和销售,嘧菌酯2005年全球销售额达到6.35亿美元。
嘧菌酯是模仿天然产物Strobilurin A化学结构而产生的新型高效广谱甲氧基丙烯酸酯类杀菌剂,嘧菌酯对几乎所有各真菌纲病害如白粉病、锈病、颖枯病、网斑病、黑星病、霜霉病、稻瘟病等数十种病害均具有很好的活性。具有保护、治疗、铲除、渗透和内吸活性,适宜于禾谷类、水稻、多种果树和蔬菜杀菌抗菌,对地下水和环境安全。
嘧菌酯合成路线主要分为两种:①先合成中间体(E)-3-甲氧基-2-(2-羟基苯基)丙烯酸甲酯,然后分别与4,6-二氯嘧啶、水杨腈反应生成最终产物;②4,6-二氯嘧啶先与水杨腈反应后再与(E)-3-甲氧基-2-(2-羟基苯基)丙烯酸甲酯反应得到嘧菌酯。两种方法中(E)-3-甲氧基-2-(2-羟基苯基)丙烯酸甲酯是合成嘧菌酯的关键中间体。
文献报道(E)-3-甲氧基-2-(2-羟基苯基)丙烯酸甲酯的合成路线比较多,但是常用、具有工业化前景的主要是邻羟基苯乙酸为原料经过3步反应得到丙烯酸甲酯的路线,具体工艺过程为:将邻羟基苯乙酸、乙酸酐先进行反应,然后在氮气保护下,与原甲酸三甲酯反应,分离出低沸点物质,将剩下混合物加入甲醇后,加热回流然后冷却结晶得到中间产物3-(α-甲氧基)亚甲基苯并呋喃-2(3H)-酮(Ⅰ);将甲醇钠、四氢呋喃和甲醇混合后冷却,在氮气保护下分批加入上述反应得到的化合物Ⅰ中,然后进行成环反应得到(E)-3-甲氧基-2-(2-羟基苯基)丙烯酸甲酯。有的文献报道合成(E)-3-甲氧基-2- (2-羟基苯基)丙烯酸甲酯可以选用乙酸甲酯、N,N-二甲基甲酰胺等溶剂。
6 烟嘧磺隆(nicosulfuron)
该品种由日本石原产业株式会社开发,获得中国专利授权(CN87100436),该专利于2007年1月27日到期。日本石原产业株式会社在中国获烟嘧磺隆原药和多种制剂的登记,国内相关登记企业有浙江金牛农药有限公司(80%烟嘧磺隆可湿性粉剂、40g/L烟嘧磺隆悬浮剂)和天津中农化农业生产资料有限公司(40g/L烟嘧磺隆悬浮剂)。
烟嘧磺隆是一高效玉米田选择性苗后除草剂,是目前磺酰脲类除草剂中销售额最大的品种,2005年全球销售额2.38亿美元。低剂量苗后使用能有效防除玉米田多种一年生禾本科杂草、阔叶杂草及莎草科杂草,其被叶和根迅速吸收,并通过木质部和韧皮部迅速传导,玉米对该药物有较好耐药性,该药剂对哺乳动物毒性低。
国外专利报道烟嘧磺隆主要从2-氨基-4,6-二甲氧基嘧啶在三乙胺存在下与光气反应生成相应的异氰酸酯,再与2-氨磺酰基-N,N-二甲基烟酰胺在乙腈中反应制得。文献还报道其他多种合成路线,但是多数路线均涉及重要的中间体2-氨基-4,6-二甲氧基嘧啶和2-氨磺酰基-N,N-二甲基烟酰胺。
6.1 2-氨基-4,6-二甲氧基嘧啶
2-氨基-4,6-二甲氧基嘧啶是磺酰脲类除草剂的重要中间体,以其为原料除合成烟嘧磺隆外,还用于合成苄嘧磺隆、吡嘧磺隆、嘧啶磺隆、玉嘧磺隆等。该中间体合成主要采用硝(盐)酸胍与丙二酸二乙酯反应制得。目前国内开发比较成熟的工业技术是采用硝酸胍与丙二酸二乙酯合成。具体工艺过程:在催化剂乙醇钠存在下,硝酸胍与丙二酸二乙酯反应得到2-氨基-4,6-二羟基嘧啶;2-氨基-4,6-二羟基嘧啶在溶剂存在的情况下,与三氯氧磷反应得到2-氨基- 4,6-二氯嘧啶;二氯嘧啶与甲醇钠发生甲氧基化反应得到2-氨基-4,6-二甲氧基嘧啶。目前国内有企业采用该法生产,生产过程中产生一定数量的''三废'',有待进一步改进与完善。
6.2 2-氨磺酰基-N,N-二甲基烟酰胺
2-氨磺酰基-N,N-二甲基烟酰胺国内文献报道的合成路线主要采用2-氯烟酸为原料合成,也有专利报道以2-羟基-2-氰基吡啶为原料,但是该原料供应紧张,价格昂贵,不适合工业化生产。国外专利报道以2-氯烟酸为原料,用氯气对2-位的巯基进行氧化后,用Al(CH3)3及NH(CH3)2进行3-位的酰胺化得到目的产物。国内研究人员在此基础上进行改进,提高收率,目前已具备工业化生产水平。具体工艺过程:2-氯烟酸、氯化亚砜及二甲胺反应得到2-氯-N,N-二甲基烟酰胺(Ⅰ);化合物Ⅰ与Na2S•9H2O及S加热反应得到2-巯基-3-N,N-二甲基烟酰胺(Ⅱ);化合物Ⅱ溶解于氨水中,然后在酸性条件下与过氧化氢及次氯酸钠发生反应得到2-氨磺酰基-N,N-二甲基烟酰胺。该工艺以2-氯烟酸为原料经过四步反应合成目的产物,收率可以达到86%以上,反应条件比较温和,反应中使用的有机溶剂均可回收套用。
7 吡螨胺(tebufenpyrad)
该品种由日本三菱化成株式会社开发,获中国专利授权(CN88102427),该专利将于2008年4月23日到期。必螨立克10%可湿性粉剂曾在中国获得临时登记(LS93021)。
吡螨胺是一种吡唑酰胺类新型杀虫杀螨剂,具有独特的化学性质和新颖的作用方式,对各种螨类的各生育期均有速效和高效,持效期长、毒性低、无内吸性,具有优异的越层渗透活性,对目标物具有极佳的选择性,能控制经药剂处理的植株中未接触药剂部位上的害螨,这是其他杀螨剂所没有的功能。与常用的杀螨剂无交互抗性,对蚜虫、叶蝉、粉虱及鳞翅目、半翅目害虫也有一定防治效果。
吡螨胺主要从吡唑甲酰氯与对叔丁基苄胺反应得到,其中对叔丁基苄胺是关键中间体。
有关对叔丁基苄胺的合成文献报道比较多,主要有:①日本三菱化成公司主要采用对叔丁基苯甲醛与氨在催化剂作用下发生还原反应得到,该法可以制得高纯度对叔丁基苄胺,但是反应需要在高压下进行,对设备要求比较高,投资也比较大;②国内研究人员开发Delepine反应,以对叔丁基苄氯与乌洛托品反应,形成的季铵盐在甲醇-盐酸中水解生成对叔丁基苄胺,该法反应条件相对温和,适合工业化生产。
国内浙江大学及浙江工业大学研究人员对Delepine反应进行反复实验,具体工艺过程如下,对叔丁基苄氯与乌洛托品在仲丁醇作为溶剂下进行反应,然后加入盐酸和甲醇继续反应,反应混合物冷却过滤,滤液浓缩得到土**固体后,加入一定量的水溶解,再用氢氧化钠进行碱化,析出大量的**液体,然后用氯仿萃取**液体得到对叔丁基苄胺。优化反应条件为:反应温度40℃,对叔丁基苄氯与乌洛托品投料比为1:1.2(m:m)。
8 烯啶虫胺(nitenpyram)
该品种由日本武田公司开发,获得中国专利授权(CN88104801.1),该专利将于2008年8月1日到期。国内相关登记企业有江苏南通江山农药化工股份有限公司和江苏连云港立本农药化工有限公司,未查到外国公司在中国登记。
烯啶虫胺属于烟酰亚胺类杀虫剂,具有独特的化学和生物性质,对害虫的突触受体具有神经阻断作用,对各种蚜虫、粉虱、水稻叶蝉显示卓越的活性,并同时具有高效、低毒、内吸、无交互抗性、对作物无药害等优点,广泛用于水稻、果树、蔬菜和茶防治多种害虫。
烯啶虫胺合成是以2-氯-5-甲基吡啶为原料经过N-乙基-2-氯-5-吡啶甲基胺,然后与1,1-二甲硫基-2-硝基乙烯和乙醇混合液进行反应,再与甲胺水溶液反应得到。其中关键中间体为2-氯-5-氯甲基吡啶。
2-氯-5-氯甲基吡啶是重要的农药中间体,不仅用于合成烯啶虫胺,还是其他重要烟碱类农药吡虫啉、啶虫脒、噻虫啉等的中间体。2-氯-5-氯甲基吡啶的研究与生产随着吡虫啉、烯啶虫胺的研究而兴起。国内外工业化生产的主要方法有:①以3-甲基吡啶为原料经过N-氧化物反应得到3-氯甲基吡啶,然后定向氯化得到;②环合法,以苄胺和丙醛反应,经过环氯化得到3-氯甲基吡啶,再经过氯化得到;③国内研究人员在美国瑞利公司开发的环戊二烯直接环合基础上,开发了以环戊二烯为原料通过关环反应直接制备2-氯-5-氯甲基吡啶,该路线原料易得,生产成本比较低,目前国内大连凯飞化工股份有限公司、江苏化工农药集团公司、江苏克胜股份有限公司多采用该法生产;④江苏农药研究所开发了以吗啉为原料的生产路线,以吗啉为原料经过N-丙烯基吗啉、1-氯-2-(4-吗啉)-3-甲基环丁基腈、2-氯-4-甲酰基戊腈、2-氯-5-甲基吡啶等中间体合成2-氯-5-氯甲基吡啶,该法具有原料成本低、反应条件温和等优点,具有工业化前景。
9 双草醚(bispyribac-sodium)
该品种由日本组合化合物公司开发,获中国专利授权(CN88108904.4),该专利将于2008年12月22日到期。日本组合化学公司还在中国获得双草醚原药(PD20040015)和10%双草醚悬浮剂(PD20040014)登记。国内相关登记企业有江苏激素研究所有限公司和上海菱农化工有限公司等。
双草醚是一种嘧啶型水杨酸类广谱除草剂,通过阻碍支链氨基酸的生物合成而起作用,主要在水稻直接田中使用,能有效防除一年生及多年生禾本科和阔叶杂草,特别能防除1~7叶期的稗草,且用量极低,具有广阔的应用前景。该农药在日本、欧美等国家已申请登记。
双草醚的合成主要有两条路线,一是非酯基保护法,由2,6-二羟基苯甲酸和2-取代-4,6-二甲氧基嘧啶在碱性条件下反应生成双草醚;二是酯基保护法,由2,6-二羟基苯甲酸先酯化,然后酯化物与2-取代-4,6-二甲氧基嘧啶在碱性条件下反应生成双草醚的酯,再经过催化加氢、中和得到双草醚。其中关键的中间体为2-取代-4,6-二甲氧基嘧啶,通常选用4,6-二甲氧基-2-甲硫基嘧啶。
文献报道4,6-二甲氧基-2-甲硫基嘧啶的合成路线主要有:①碘甲烷法,碘甲烷与4,6-二羟基-2-甲硫基嘧啶反应制备,该法收率不高,同时磺甲烷价格昂贵;②硫酸二甲酯法,硫酸二甲酯与4,6-二羟基-2-巯基嘧啶反应,该法收率比较低,且''三废''排放量较大;③3-氨基-1,3-二甲氧基-2-甲磺酰基嘧啶与过氧化氢氧化制备,该法原料来源困难;④浙江工业大学研究人员开发以丙二酸二乙酯和硫脲为原料的合成路线,在甲醇钠存在下缩合成4,6-二羟基-2-嘧啶硫酸钠,再经过甲基化、氯化、甲氧基化等一系列反应得到4,6-二甲氧基-2-甲硫基嘧啶,尽管步骤较多,但是反应条件温和,原料价廉易得,具有工业化应用前景。
上面介绍了部分农药及其中间体的合成,这些农药具有一些共同特点,就是国外公司开发,且在中国取得专利授权,同时这些品种都在中国已经或曾经登记过,同时专利已经到期或即将到期。专利一旦到期可以进行仿制,同时由于在国内取得登记或者临时登记,具有一定推广应用基础,产品开发生产后比较容易被市场所接受,可以大大缩短进入市场的时间。而这些农药开发的关键在于重要中间体的开发与研究,因此国内相关科研机构和农药生产企业,应积极跟踪国外专利农药法律保护状态,加强中间体开发研究,期待改进和完善中间体合成工艺,降低中间体生产成本,为生产这些高效低毒具有良好市场前景的农药打下坚实基础。
有人知道氧氟沙星合成路线吗?
[guǒ ěr]
果尔
中文通用名乙氧氟草醚,[通用名称] fluoroglycofen,[化学名称] 0-[5-(2-氯-a,a,a-三氟-对-甲苯氧基)-2-硝基苯甲酰基]羟基乙酸乙酯。
中文名
果尔
分子式
C18H13ClF3NO7
分子量
447.8
规 格
原药含量 ≥95%
简介
[CAS登记号] [ 77501- 60-1 ]
[分子式] C18H13ClF3NO7
[结构式]
[分子量] 447.8
[理化性质] 纯品为深琥珀色固体,熔点65°C,相对密度(d25)1.01,蒸汽压<1.33×105mPa(25°C)。溶解性(25°C):水<1mg/l、大多数有机溶剂>100g/kg。
[毒性] 大鼠急性经口LD501500mg/kg,兔急性经皮LD505000mg/kg,低毒。
[用途] 本品属于二苯醚类除草剂,是原仆啉氧化酶抑制剂。芽前、芽后使用,可防除小麦、大麦、花生、大豆和稻田阔叶杂草和禾本科杂草,尤其是猪秧秧、婆婆纳和堇菜。
[规格] 原药含量 ≥95%
[包装] 25kg/纸板桶,也可按客户要求包装。
[制剂与厂家] 12.5%EC 20%乳油(江苏响水县农药厂);24%乳油(美国罗门哈斯公司)
[除草特点] 选择性触杀型芽期除草剂。主要通过胚芽鞘、中胚轴进入植物体内,根部也可少量吸收,芽前及芽后早期适用效果好。药剂在光照条件下发挥作用。施入田间很快被土壤吸附,20-30天分解。对后茬无残留毒害。
[适用作物] 稻、大豆、棉花、花生、玉米、甘蓝、番茄、甘蔗、甘薯、林业苗圃。
防治对象
可以防治一年生单双子叶杂草,如稗草、牛毛毡、狗尾草、马唐、鸭舌草、野荸荠、野苋菜、铁苋菜、蓼、藜、苘麻、龙葵、曼陀罗、田荠、苍耳、牵牛花、节节草、异型莎草等。对大部分多年生杂草无效,如荠菜、香附子、眼子菜、水花生、瓜皮草等。
使用技术
1、已在稻田。在长江流域及以南稻区,秧龄30天以上一季中稻和双季稻,用24%乳油10-20ml/亩,用水100-200ml稀释成母液后混毒土撒施,保水3-5cm5-7天。
2、陆稻、大豆、花生、玉米、甘蓝、番茄、油菜田,播后苗前用24%乳油30-50ml/亩,加水30kg喷于土表。
3、棉田。棉花播后芽前兑水土壤封闭,用24%乳油10ml/亩,可有效防治多种杂草,持效期40-60天。也可在棉花16cm以上时对棉花下部定向喷雾。
4、玉米田。玉米40cm 高时,定向喷雾。
5、果园、茶园、针叶苗圃,用24%乳油40-50ml/亩,加水稀释后用低压喷雾器定向喷雾。
注意事项
果尔虽然在水稻上取得登记,但从对作物安全角度考虑,北方地区不宜在水稻上使用。
2.果尔为触杀型除草剂,喷药时要求均匀周到,施药剂量要准。采用定向喷雾时,应避开果树、林木,以免造成药害。
3.初次使用时,应根据不同气候带,先经小规模试验,找出适合当地使用的最佳施药方法和最适剂量后,再大面积使用。
4.果尔施用剂量随土质和早涝情况作相应调整,沙质土用低药量,壤质土、粘质土用高药量。
5.重点防除牛繁缕、苍耳等石竹科或菊科杂草,应在杂草子叶期施药;防除小旋花应在杂草6-8叶期施药;防除看麦娘、野燕麦等禾本科杂草,应在杂草1-2叶期施药。
6.果尔在播后采用土壤处理时,要求土表湿润,但不能积水。应避免翻动土壤表层,以保持药膜层完整。覆膜田遇高温时,应注意揭膜降温,防止产生药害,当温度低于6℃时,禁止使用果尔。
7.在大蒜1叶1心至2叶期施用果尔,易造成心叶折断或严重灼伤,此期间严禁施用。2叶1心期后施用果尔,大蒜叶片出现褐色或白色斑点,对中后期生长无影响。白皮蒜比紫皮蒜对果尔的耐药性强。
左旋氧氟沙星(levofloxacin,1)化学名为(S)-(-)-9-氟-2,3-二氢-3-甲基-10-(4-甲基-1-哌嗪)-7氧代-7氢吡啶骈〔1,2,3-de〕〔1,4〕苯骈?嗪-6-羧酸,是氧氟沙星的(S)-(-)异构体,它的抗菌活性为氧氟沙星的2倍,毒副作用小,成为第三代氟喹诺酮抗菌药中最优秀的品种之一,最早由日本第一制药株式会社开发上市〔1,2〕.
1 合成路线设计
化合物(1)的合成文献〔3〕报道按起始原料可分为两大类:方法一,由2,3,4,5-四氟苯甲酸为原料,经酰氯化后与丙二酸二乙酯缩合、部分水解脱羧、与原甲酸三乙酯缩合、(S)-(+)-2-氨基丙醇置换、环合、水解后与4-甲基哌嗪缩合精制而得〔4,5〕;方法二,以2,3,4-三氟硝基苯为起始原料,先合成关键中间体(S)-7,8-二氟-3-甲基-3,4-二氢-2H-1,4-苯骈?嗪,再与乙氧亚甲基丙二酸二乙酯缩合、环合、水解、上甲基哌嗪精制而得〔6~8〕.方法二尽管与目前国内氧氟沙星的合成工艺近似,但关键中间体(S)-7,8-二氟-3-甲基-3,4-二氢-2H-1,4-苯骈?嗪的合成存在步骤长、收率低、光学纯化难度大等缺点,难以适合大量制备.方法一因国内已有2,3,4,5-四氟苯甲酸及(S)-(+)-2-氨基丙醇工业品供应,成为不对称合成左旋氧氟沙星较为理想的选择,故采用方法一作为试制路线,并对合成工艺进行优化和改进,以2,3,4,5-四氟苯甲酸为原料,经8步反应制得左旋氧氟沙星,总收率为39.2%,最终产物结构经元素分析,IR,1H-NMR,13C-NMR,DEPT,MS鉴定.合成路线见图1.
Fig.1 The synthesis route of levofloxacin
2 实验部分
熔点采用北京泰科仪器有限公司的XT-4双目显微熔点仪测定,温度未经校正.元素分析用美国PE-240C型元素分析仪.红外光谱仪为Nicolet 170SX型.热重分析用美国PE-7系列热重分析仪.核磁共振谱用Bruker AM 500 MHz核磁共振仪测定,d6-DMSO为溶剂,TMS为内标.质谱用VG-ZAB-HS GC-MSZ质谱仪测定.旋光度用WZZ-1自动指示旋光仪测定.
2.1 2,3,4,5-四氟苯甲酰基乙酸乙酯(5)的合成
化合物(2)38.8 g(0.200 mol)、SOCl2 150 mL(2.05 mol)、DMF 0.4 mL依次加入到反应瓶中,搅拌加热回流5 h,常压蒸出过量的SOCl2,加甲苯40 mL再减压蒸干得化合物(3).
于另一个反应瓶中依次加入镁粉5.0 g(0.206 mol)、无水乙醇50 mL、四氯化碳0.5 mL,加热引发反应后,搅拌下滴加丙二酸二乙酯32.8 g(0.206 mol)和无水甲苯60 mL的混合液,30 min加完后于60℃继续反应2 h,冷至-5℃后滴加化合物(3)的甲苯80 mL溶液,1 h加完后继续在0℃搅拌反应2 h,倾入浓盐酸90 mL和冰水90 mL的混合液中,分出有机相,水相用甲苯(50 mL×3)萃取,合并有机相,减压蒸出甲苯得橙**油状液体(4),在化合物(4)的反应瓶中加入水100 mL和对甲苯磺酸0.1 g(0.500 mmol),加热回流6 h,TLC检测原料点基本消失〔乙酸乙酯-甲醇(V∶V=4∶0.5)为展开剂〕,冷至室温,以二氯甲烷(50 mL×3)萃取,有机相用水洗至中性,无水硫酸钠干燥,减压蒸干得橙色液体(5)44.4 g,收率:84.0%(文献〔4〕收率:93%),化合物(5)不经纯化,直接用于下一步反应.
2.2 (S)-(-)-9,10-二氟-2,3-二氢-3-甲基-7氧代-7氢吡啶骈〔1,2,3-de〕〔1,4〕苯骈?嗪-6-羧酸乙酯(8)的合成
在含有化合物(5)44.4 g(0.168 mol)的反应瓶中,加入醋酐82 mL(0.876 mol),原甲酸三乙酯66.6 mL(0.400 mol),搅拌加热回流4 h,并在反应中蒸出生成的乙酸乙酯,使反应完全,减压蒸干后加二氯甲烷450 mL溶解,于室温搅拌滴加(S)-(+)-2-氨基丙醇13.5 g(0.180 mol)和二氯甲烷50 mL的混合液,1 h滴完后继续搅拌反应2 h,回收二氯甲烷并减压蒸干得橙红色粘稠性油状物(7),在含化合物(7)的反应瓶中加入DMF 400 mL及无水K2CO3 46.4 g(0.336 mol),在120℃搅拌反应8 h,减压回收DMF后向反应瓶中加入冰水250 mL,搅拌析出固体,放置过夜,过滤,固体用水洗涤,以氯仿-乙醇(V∶V=3∶2)进行重结晶,烘干得化合物(8)34.0 g,收率:65.4%,mp 254~256℃(文献〔6〕mp 254~255℃).
2.3 (S)-(-)-9,10-二氟-2,3-二氢-3-甲基-7氧代-7氢吡啶骈〔1,2,3-de〕〔1,4〕苯骈?嗪-6-羧酸(9)的合成
按文献〔8〕操作,收率为:87%,mp>300℃(文献〔8〕收率:88%,mp>300℃).
2.4 (S)-(-)-9-氟-2,3-二氢-3-甲基-10-(4-甲基-1-哌嗪基)-7氧代-7氢吡啶骈〔1,2,3-de〕〔1,4〕苯骈?嗪-6-羧酸(1)的合成
化合物(9)28.1 g(0.100 mol)、N-甲基哌嗪26 mL(0.230 mol)、DMSO 75 mL依次加入反应瓶中,130℃加热搅拌反应6 h,减压回收DMSO及过量的N-甲基哌嗪,残留物用95%乙醇重结晶,得淡**晶体(1)的半水合物30.3 g,收率:82%,(文献〔8〕收率:75.06%),mp 224~226℃,〔α〕24D=-76.7°(c=0.39,0.05 mol/L NaOH)〔文献〔7〕mp 225~227℃,〔α〕24D=-76.9°(c=0.385,0.05 mol/L NaOH)〕.TG分析:化合物(1)在35.466~82.453℃失重2.632%,相当于含0.5个结晶水(理论含0.5个结晶水值为2.430%).元素分析,实测值(%):C 58.29,H 5.72,N 11.16,F 5.07;理论值(%):C 58.32,H 5.72,N 11.34,F 5.13.IR(KBr)cm-1:3267(—COOH),3081(ArH),2974~2802(RH),1724.3(—COOH,CO),1621(7—CO),1542~1453(Ar—CC—),1395.6~1315.4(C—H,C—N),1291.8~1241.0(C—O,C—F),1089.9(C—N),927.5(—OH),802(C—H).1H-NMR(DMSO-d6)δ:15.22(1H,br s,—COOH),8.96(1H,s,5-H),7.56(1H,d,8-H),4.92(1H,d,3-H),4.58(1H,d,2βH),4.36(1H,d,2αH),3.26~3.36(4H,m,1,1′哌嗪环质子),2.44(4H,br s,2,2′哌嗪环质子),2.23(3H,s,N—CH3),1.45(3H,d,3-CH3).13C-NMR(DMSO-d6)δ:176.27(7-C),165.95(-COOH),155.38(9-C),146.06(5-C),140.03(11-C),132.01(10-C),124.72(12-C),119.55(13-C),106.55(6-C),103.21(8-C),68.01(2-C),55.25(哌嗪环2,2′-C),54.78(3-C),50.05(哌嗪环1,1′-C),46.01(N-CH3),17.88(3-CH3).13C-NMR(DEPT)δ:146.06(5-C),103.21(8-C),54.78(3-C)为CH碳原子;δ:68.01(2-C),55.25(哌嗪环2,2′-C),50.05(哌嗪环1,1′-C)为CH2碳原子;δ:46.01(N—CH3),17.88(3-CH3)为CH3碳原子.EI MS m/z:361(M+).
3 讨论
文献〔4〕报道化合物(5)的合成以化合物(2)为原料经酰氯化后与丙二酸单一酯在丁基锂作用下,于-55℃低温下缩合,水解精制而得,收率为93%,但该合成方法成本高,反应条件苛刻,本文在参考文献〔9,10〕类似物合成方法基础上,由(2)经酰氯化后与乙氧基镁丙二酸二乙酯缩合,用0.1%对甲苯磺酸部分水解脱羧制得,收率为84%.由(5)制备(9)时,本实验在(5)与原甲酸三乙酯和醋酐反应时,将生成的乙酸乙酯蒸出使反应完全,并以无水K2CO3和DMF替代文献〔5〕中的50%NaH和DMSO,以冰醋酸和盐酸替代KOH进行水解,四步反应收率为56.9%(文献〔5〕收率:23.5%),以DMSO替代吡啶为溶剂进行缩N-甲基哌嗪反应,收率为82%(文献〔8〕收率为75.06%),以2,3,4,5-四氟苯甲酸计,总收率为39.2%,本研究对左旋氟沙星的工业化生产有一定的参考价值.
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。