原料药登记状态如何查询真伪-原料药登记状态如何查询
深圳市金寿康药业有限公司是2006-07-24在广东省深圳市注册成立的有限责任公司(自然人独资),注册地址位于深圳市龙华区观澜街道新澜社区观光路1301-23号车间区601。
深圳市金寿康药业有限公司的统一社会信用代码/注册号是91440300791721268R,企业法人艾小刚,目前企业处于开业状态。
深圳市金寿康药业有限公司的经营范围是:货物与技术进出口;健康养生管理咨询(不含医疗行为);物业管理;自有物业租赁;^批发:中药材(收购)、中药饮片、中成药、化学原料药、化学药制剂、抗生素原料药、抗生素制剂、生化药品、生物制品(除疫苗)、蛋白同化制剂、肽类激素;保健食品批发;预包装食品(不含复热预包装食品)的批发;药品技术咨询。在广东省,相近经营范围的公司总注册资本为614545万元,主要资本集中在1000-5000万和5000万以上规模的企业中,共311家。本省范围内,当前企业的注册资本属于良好。
深圳市金寿康药业有限公司对外投资6家公司,具有0处分支机构。
通过百度企业信用查看深圳市金寿康药业有限公司更多信息和资讯。
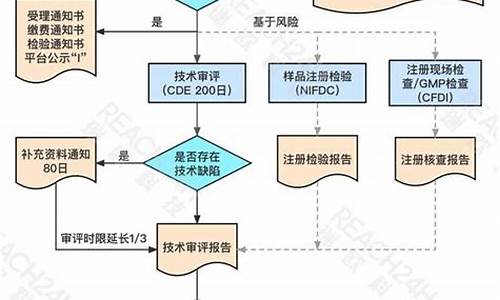
药品生产管理流程
武汉联合药业是在原武汉第九制药厂基础上,经过资产重组、股份制改造,于1998年10月19日注册成立的有限责任公司。入选国家中药现代化科技产业(湖北)基地骨干企业,获得“国家中药现代化科技示范企业”、“湖北省市场行业十佳信誉单位”、国家高新技术企业等称号。过去5年,公司主营收入保持年均50%快速增长,并呈现出加速发展态势,近几年专利申请量迅速增长。2013年,公司获得东湖高新技术开发区“瞪羚企业”称号。
企业名称: 武汉联合药业有限责任公司
企业类型: 有限责任公司
注册号: 420100000082917
经营状态: 存续
法定代表人/负责人: 徐春庭
住所: 武汉市东湖开发区关山二路33号
邮政编码: 430000
核准日期: 2011-03-25
成立日期: 1998-10-19
经营截至期限: 2044-10-18
一般经营范围: 中西药品(颗粒剂、片剂、硬胶囊剂、原料药)的生产;生产及销售保健食品(风靡牌康欣胶囊、风靡牌蜂眠宁胶囊、东方之子牌蚂蚁胶囊、东方之子牌双岐胶囊、状态佳慷体胶囊)。(凭许可证在核定期限内经营);药品、保健食品、新产品、新技术的研制、技术开发、技术信息咨询与服务(国家有规定的除外)生产及销售保健食品。
许可经营范围: 中西药品(颗粒剂、片剂、硬胶囊剂、原料药)的生产;生产及销售保健食品(风靡牌康欣胶囊、风靡牌蜂眠宁胶囊、东方之子牌蚂蚁胶囊、东方之子牌双岐胶囊、状态佳慷体胶囊)。(凭许可证在核定期限内经营)
登记机关: 武汉市工商局东湖分局
管辖工商所: 光谷所
专利号查询CN103610825A
药品生产管理流程
管理是人类各种组织活动中最普通和最重要的一种活动。以下是我收集的药品生产管理流程,欢迎查看!
批生产记录批
生产记录是一批药品生产各工序全过程(包括中间控制)的完整记录,应具有质量的可追踪性。
一、批
批的概念:在规定限度内具有同一性质和质量,并在同一连续生产周期中生产出来的一定数量的药品为一批。
1. 大、小容量注射剂一般以同一配液罐一次所配制的药液所生产的均质产品为一批。
2.粉针剂一般以同一批原料药在同一连续生产周期内生产的均质产品为一批。
3.冻干粉针剂以同一批药液使用同一台冻干设备在同一生产周期内生产的均质产品为一批。
4.固体、半固体制剂在成型或分装前使用同一台混合设备一次混合量所生产的均质产品为一批。
固体制剂如采用多次混合后的产品作为一个批号,必须经过验证,证明产品质量的均一性后,在规定限度内所生产的产品为一批。一般以最终所采用的混合设备如多维运动混合机混合一次的数量为一个批次。
5.液体制剂(包括膏滋、浸膏及流浸膏等)以灌封(装)前经最后混合的药液所生产的均质产品为一批。
6.连续生产的原料药,在一定时间间隔内生产的在规定限度内的均质产品为一批。
间歇生产的原料药,可由地定数理的产品经最后混合所得的在规定限度内的均质产品为一批。混合前的产品必须按同一工艺生产并符合质量标准,且有可追踪的记录。
7.生物制品生产应按照中国生物制品规程中的“生物制品的分批规程”分批和编制批号。
应注意两台或两台以上的压片机(胶囊充填机)所压制出来的片子,必须分别做片重差异(装量差异)检查,确认在同一合格的范围之内并且符合其质量要求后才可作为一批。
二、批号
批号的定义:用于识别“批”的一组数字或字母加数字,用以追溯和审查该批药品的生产历史。生产中的每一个批次都必须要编制生产批号。
批号的编制方法
1. 正常批号:年—月流水号,如011201批,即2001年12月的第1批。或采年—月—日流水号,如0112012批,即2001年12月1日的第二次配制所生产的批号。或采用数字加字母,以英文字母表示生产车间或剂型等。
2. 重新加工批号:重新加工后的批号不变,只是在原批号后加一代号以示区别,代号由企业自定,如年—月—日流水号(代号)。
3.混合批号:年—月—流水号(代号),如0112/03-05,表示所混合的批号为2001年12月第3批至第5批共3 批,代号由企业自定,并由车间填写混合批号登记表。
应注意的是药品的零头包装只限于两个批号为一合箱,合箱外应标明全部批号,并建立合箱记录。
三、批生产记录
1.批生产记录的定义:一个批次的待包装品或成品的所有生产记录。批生产记录应能提供该批产品的生产历史、以及与质量有关的情况。
2.批生产记录的内容:产品名称、生产批号、生产日期、操作者、复核者的签名、有关操作与设备、相关生产阶段的产品数量、物料平衡的计算、生产过程的控制记录及特殊问题的记录。
3.批生产记录的填写
岗位操作记录由岗位操作人员填写,岗位负责人、工艺员审核并签字;批生产记录由车间技术人员汇总,车间技术主任或车间专职工程师审核签字,跨车间的产品,各车间分别填写,由厂生产技术部门指定专人汇总审核并签字。成品发放前,厂质量管理部门审核批生产记录并签字,决定产品的最后放行。
GMP中规定填写批生产记录应字迹清晰、内容真实、数据完整,并由操作人及复核人签名。记录应保持整洁,不得撕毁和任意涂改,更改时,在更改处签名,并使原数据仍可辨认。
填写批生产记录的要求:
①内容真实,记录及时;
②字迹清晰,不得用铅笔填写;
③不得任意撕毁和涂改,需要更改时,应用一条或二条横线划在更改处,在旁边重写正确的数据并签名及日期,要使原数据仍可辨认;
④按表格内容填写齐全,数据完整,除备注栏外,不准留有空格,如无内容可填写,要用“—”表示;
⑤内容与前面相同时应重复填写,不得用“……”或“同上”、“同左”来表示;
⑥品名等应写全名并按标准名填写,不可简写;与其他岗位、班组或车间有关操作记录应做到一致性、连贯性;
⑦填写日期一律横写,不得简写;
⑧签名时应写全名,不得简写;
⑨数据的修约应采用舍进机会相同的修约原则,即“4”舍、“6”入、“5”成双。
4.复核批生产记录的注意事项:
必须按每批岗位操作记录串联复核;
必须将记录内容与生产工艺规程,岗位操作规程对照复核;
上下工序及成品记录中的数量、质量、批号、容器号必须一致、正确;
对生产中不符合要求的填写方法,必须由填写人更正并签字;
若发现异常情况必须查明原因,作出合理的说明,并作详细的记录,经办人,复核人要签字。
5.批生产记录的保存:
批生产记录应按产品种类按批归档保存至产品有效期后一年,未规定在效期的药品,其批生产记录至少应保存三年。
生产过程的技术管理
一、生产准备阶段的技术管理
1.生产管理部门按照企业的生产销售情况安排生产计划,并编制批生产指令发放到生产、物料及质量等相关部门。同时,将相应的批生产记录发放至操作车间。
2.生产车间按批生产指令、生产工艺规程及岗位标准操作规程,由车间工艺技术员向各工序分别下达生产计划,各工序根据计划向仓限额领取物料,领料时需核对品名、规格、批号、生产厂家、数量、及检验合格报告单等,并填写领料记录。
3.对制剂或原料药成品质量有影响的原辅料,在货源、批号改变时,应先进行小样试制确认符合要求后填写小样试制合格报告单,经质量管理部门审核签署后方可投入生产。
4.生产操作开始前,操作人员必须对工艺卫生、设备状况等进行检查,检查内容有:
①检查生产场所卫生是否符合该区域卫生要求;
②更换批号品种及规格前要有上一批产品的“清场合格证副本”,未取得“清场合格证副本”不得进行另一个品种或同品种不同规格或不同批号产品的生产;
③设备清洁完好,有“设备清洁状态标志”;
④计量器具与称量范围相符,清洁完好,有“计量检定合格证”,并在周检有效期之内;
⑤正在检修或停用的设备应挂上“不得使用”的状态标志,检修完毕后应由设备员验收合格并清洁干净、符合要求,有设备完好状态标志才允许使用;
⑥衡器、量具使用前应进行检查、校正,对生产上用于测定、测试仪器、仪表,进行必要的调试;
⑦所用各种物料、中间产品应按质量标准核对检验报告单,中间产品有质管员签字的传递单,仔细辨别,盛装容器要桶、盖编号一致,并有明显标志;
⑧盛放物料的容器外必须具有标签,标签上应注明品名、规格、批号、重量(皮重、毛重、净重)或数量、本批容器数及加工状态、工序名称、操作日期及班次、操作人、复核人等。
二、生产过程中的技术管理
1.按GMP规定,生产过程中物料的投料、称量、计算等操作,都必须要有人复核,操作人、复核人应在操作记录上签名,车间工艺技术员、质量员均应对此关键操作进行监督。对于麻醉的药品、精神的药品、毒品、放射品及贵细药品,应按国家有关规定严格执行,使用后剩余的散装物料应及时密封,由操作人在容器上注明启封日期,剩余数量、使用者、复核者签字后,由专人办理退库手续。再次启封使用过后原辅料时,应核对记录,检查外观性状,如发现有异常情况或性质不稳定时,应再次送检,合格后方可使用。
每批生产结束后的剩余物料,操作人员应及时退库,车间不得存放未使用完的剩余物料,但中间站存放的中间产品除外。
2.生产工艺规程和标准操作规程
生产工艺规程:规定为生产一定数量成品所需起始原料和包装材料的数量,以及工艺、加工说明、注意事项、包括生产过程中控制的一个或一套文件。
标准操作规程:经批准用以指示操作的通用性文件或管理办法。
岗位操作需按生产工艺规程所规定的工艺条件和标准操作规程所规定的操作方法进行。生产工艺规程、标准操作规程一经制定,不得任意更改,如需更改时,应按照规定的程序办理修订、审批手续。
企业生产技术部门和车间工艺技术员须对生产工艺规程和标准操作规程的执行情况进行检查,即制定工艺查证制度并定期进行工艺查证,并详细记录,保证工艺规程及操作规程的准确执行。工艺查证内容由企业按各岗位操作规程的要求,检查各工艺参数执行情况、洁净区(室)温湿度以及定期检查尘埃粒子数、微生物数、质量抽查记录、工艺卫生及批生产记录。操作人员必须熟悉相关岗位的工艺控制点,质量控制点,并严格进行自控。
中药制剂车间一般生产工艺控制点有:(以片剂为例)
①提取浸膏的比重,数量,醇沉的酒精浓度等;
②中药材粉未的粒度、水份、微生物数量、粉碎物料平衡收率等;
③制粒工序的粘合剂配比、使用量,制粒温度,颗粒粒度、水份、含量均一性等;
④压片片剂的硬度、脆碎度、崩解时限或溶出度、片重差异、外观等;
⑤片剂包衣的包衣液情况、包衣片外观、崩解度、片剂增重等;
⑥内包装工序的包装数量、外观、密封性试验等;
⑦外包装工序的标签、使用说明书领用情况,外包装数量、包装质量等。
3.不同产品品种、规格的生产操作不得在同一操作意见时进行,同一品种同一规格不同批号的制剂生产及包装操作在同一操作间内进行时,应采取隔离或其它有效防止污染或混淆的措施。
生产操作人员在操作过程中动作要稳、轻、少,不做与生产无关的动作及不必要的交谈,更不能在生产操作现场嘻笑和打闹或高声唱歌。
4.生产过程中各关键工序要严格进行物料平衡的计算,符合规定的范围方可流入下一道工序。如超出范围,要按偏差处理程序进行分析调查,采取措施要经质量管理部门批准,在得出合理解释,确认无潜在的质量事故后,方可进入下一道工序。
生产过程中如发现物料异常情况,或可能存在的质量问题,操作人员不能自作主张,需向相关人员及车间领导汇报,按偏差处理程序进行处理。最终由质量管理部门决定物料的使用权。质量管理部门应遵循“三不放过”的原则,即不合格的原辅料不得投入生产,不合格的中间产品不得流入下一道工序,不合格的成品不得出厂。
生产过程、中间产品都必须在质量管理部门质管员的严格监控下,各种监控凭证要纳入批记录背面,无质管员签字发放的各种放行凭证,不得继续操作。
生产过程中如发生问题需对设备进行调节或维修时,应停机进行操作,切不可开机操作,以免造成安全事故,对人员造成伤害。
5.定置管理
为了便于养成良好的.生产习惯,减少发生差错的可能性,车间应进行定置管理。
生产操作与设备应按工艺流程的顺序合理布局,使物料的生产按同一方向顺序流动,避免物料的交叉流动,减少交叉污染的可能性,且不遗漏任何生产工序。
操作间的定置管理是指严格规定操作间的设备、各种物料及容器、操作台等的摆设位置。生产中所使用的工器具,在使用完毕后都应放回原位,不能到处丢放或放在设备里面,以免发生生产事故。
中间站等其它房间也应进行定置管理,如洁具间应规定各种清洁工具的存放位置,并严格执行制定的定置管理制度。
6.状态标志管理
与设备连接的主要固定管道包括工艺用水管道应标明管道内物料的名称及流向。管道应安装整齐、有序,或用不同的颜色进行喷涂以示区别。如物料管道
——**、蒸汽管道
——红色、饮用水管道
——蓝色、压缩空气管道
——白色等,可由各企业按自已的实际情况自定。以喷涂颜色的方向表示物料的流向。
各生产操作间也应有状态标志来说明操作间现在的生产状态。生产时应标明所生产的品种、规格、批号、生产日期、操作者等;未生产时应用清洁、待清洁等表示,清洁状态应标明清洁有效期、上批产品名称等;未使用的房间应用备用标志表示。
设备的状态有清洁、使用、备用、维修、待修等。使用时应标明所生产的品种、规格、批号、生产日期、操作人等,设备固定状态标志应标明设备的型号、设备负责人等。 物料和使用容器也应有状态标志,其内容如前面容器标签所示。
7.包装与贴签管理
对符合生产工艺规程要求,在质量管理部门和车间工艺技术员、质量员的监控下完成生产全过程,并检验合格的产品可由生产管理
部门下达批包装指令。对于一些检验周期长,需要在检验结果前包装的制剂产品,则允许先包装后按待检寄库的产品处理,检验合格后才办理入库手续。
包装所使用的标签和使用说明书,必须由车间填写领料单,派人到标签库限额领取,并由领料人及发料人签字。已打印批号的标签,发剩的和残缺标签或该批号取消时,或车间贴签工序剩余标签不得回收利用,应由经手人会同质管部门派人监督销毁,并做好记录,经手人及监督人员签字。
车间应设标签库,由专人负责标签的领用和发放,并按品种、规格分类,存放在标签库内,
上锁保管,并有记录登记,已印批号的标签,按批存放。产品包装时,由包装工序根据批包装指令派专人向车间领取并填写领用记录。
每批产品在包装完成后应及时填写包装记录,如实填写所领用的包装材料数量。如果使用数+剩余数+残损数之和与领用数不相符合时,应查明原因,并做好记录。标签不得改做他用或涂改后再使用。
8.中间站的管理
车间生产的中间产品,应存放在中间站内,不得长时间存放于操作间。中间站存放的范围包括:中间产品、待重新加工的产品、清洁的周转容器等,除上述范围以外的物品不得存放于中间站,中间站应随时保持清洁,不得有散落的物料,地上散落的物料不得回收!进入中间站的物品其外包装必须清洁,无浮尘。
中间产品在中间站应有明显的状态标志,注明品名、批号、规格、数量、并按品种、批号码放整齐,不同品种,不同批号,不同规格的产品之间应有一定的距离,物料应加盖密封保存。并以“红色牌”表示不合格,以“**牌”表示待验,以“绿色牌”表示合格,以 “白色牌”表示待重新加工,并且分堆存放。
操作人员每天及时将物料存放入中间站,并填写中间站进站记录,中间站管理员核对品名、规格、批号、重量(数量)容器数、工序名称、加工状态等,无误后检查外包装清洁情况,并由送料人及中间站管理员共同签字,填写进站日期,并将物料按规定堆放整齐。中间站管理员填写中间产品台帐及中间站物料卡,中间站进站记录应附于批生产记录上。
中间站存放的物料要求帐、卡、物一致,质量管理部门监督员及车间工艺技术员、质量员应定期对中间站的物料状况进行检查。
中间站管理员对中间产品进行请验,此时物料应挂待验状态标志,只有经检验合格后,才能挂合格的状态标志,或由质量管理部门发放中间产品合格证。
根据车间下达的工序生产指令,中间站管理员可向下一工序发放合格的中间产品,并填写中间产品出站记录,由下一工序的领料人员复核品名等到,在中间站出站记录上共同签字,同时填写中间站台帐及库卡。
中间站应上锁管理。管理人员离开时应上锁后方可离开。
9.不合格品的管理
经质量管理部门检验确认不合格的产品,由检验部门发放不合格品检验报告单,车间及时将不合格品存放于规定的不合格品存放区内,并挂上红色不合格品标志,按不合格品处理程序及时进行处理。
不合格品一般由生产管理
部门会同有关部门分析提出处理意见后报质量管理部门审核同意后,由主管领导批准,规定部门执行,限期处理,并填写处理记录。
10.模具、筛网的管理
车间设备员应对生产使用的模具建立档案,存放于相应的模具间。模具使用前后均应检查其光洁度,零配件是否齐全,有无破损,是否符合生产要求等,并填写模具使用发放记录。对破损的模具应进行维修,合格后方可使用,无法继续使用的,应办理报废手续,并根据实际情况申请采购。
筛网使用前应检查其完好程度,是否符合生产工艺的要求,每一存放的筛网都应标明其规格(目数)。生产过程中应经常检查筛网的使用情况,如发现破损应追查原因,是否对产品造成了质量影响,进行必要的处理后方可继续生产。如为质量问题应及时报告车间领导及质量管理部门进行解决。
生产过程中一般使用不易与药品产生化学反应的不锈钢或尼龙筛网。
11.生产过程中产生的特殊物料的管理
①粉头的管理
粉头是指生产过程中产生的合格的,可以回收利用的或未用完的少量物料。如胶囊充填完成后剩余的加料盘中的物料等。
生产结束后产生的粉头应及时装入洁净的容器中,注明品名、规格、批号、重量(数量)、生产日期、操作人及复核人等,送入中间站保存并做记录,报送车间工艺技术员。
车间工艺技术员根据生产安排情况,将合格的粉头投入下一批生产的同一规格品种的产品中,并要求在批生产记录中注明粉头的物料流动情况。粉头必须规定使用周期,超过规定的周期后必须进行复检,合格后才能继续使用。不合格的粉头应作为废弃物处理。
②生产中产生的废弃物的管理
生产中的废弃物是指生产过程中产生的不合格的物料及其它不能继续使用的物品,包括掉落在地上的物料、压片或胶囊充填中做装量差异(片重差异)后的片子(胶囊)、盛放物料的塑料袋等。它应按照废弃物管理规程,由生产操作人员及时将废弃物装入专门的盛放废弃物的容器中,在规定的时间,由专门的人员收集后由物料通道传出洁净区。
如下例生产过程中产生的物料如何处理?
粉碎后操作后留在粉碎机内的药物;
制粒时不小心掉在地上的颗粒;
干燥过程中取出观察颗粒外观的颗粒;
压片前试压(调机)后留下的片子;
取样检查片重差异的素片;
胶囊充填过程中怀疑有装量差异不合格的胶囊;
制粒后发现有钢丝筛网破损后的颗粒。
12.物料平衡的管理
建立并规定物料平衡检查标准,严格控制生产过程中物料收率的变化,进行严格的收率控制,使之在合理的范围内,对不正常的情况进行分析处理,这是防止差错和混淆的有效方法之一。
①物料平衡计算公式
实际值 ? 收率= ×100% ? 理论值 ? 其中:
理论值:为按照所用的原料(包装材料)理论产量(在生产中无任何损失或差错的情况下得出的最大数量)。
实际值:为生产过程中实际产出量。
如制粒工序的物料平衡计算公式
所得颗粒的总重量(kg) ? 物料平衡= ×100% ? 投入的原料辅料重量+粉头重量(kg) 口服固体制剂车间一般需计算物料平衡的工序有:
备料(粉碎、过筛);制粒、和药;制丸、压片、胶囊充填;包衣;内包装;外包装。
中药前处理工序:药材拣选;炮制加工;提取浓缩;药材干燥。
②在生产过程中如发生有跑料情况,应及时通知车间管理人员及质量管理部门,并详细记录跑料过程及数量,跑料数量也应计入物料平衡之中,加在实际值范围之内。
凡物料平衡收率不符合生产工艺规程的规定,应立即贴上待处理品的状态标志,不能递交到下一道工序,并填写偏差处理单,按偏差处理程序进行处理。
清场管理
一、定义和目的
为了防止混淆和差错事故,各生产工序在生产结束,转换品种、规格或批号前,均应进行清场。
清场的频次:每天生产结束后应进行清理,将设备表面,操作间清理干净;换品种、批号时应进行彻底的清场;连续生产规定的时间(一般三天)后,也应进行彻底清场;长时间的生产间隔后,再次开始生产之前也应进行清场。
清场必须严格按照岗位与设备等的清洁规程进行操作,车间工艺技术员、质量员及质量管理部门的质监员应对清场工作进行监督。
二、清场的内容及要求
1.地面无积灰,无结垢,门窗,室内照明灯、风管、墙面、开关箱等外壳无积尘室内不得存放与下次生产无关的物品(包括物料、文件、记录和个人杂物);
2.使用的工具、容器、应清洁,无异物、无油垢;
3.设备内外无生产遗留的药品,无油垢;
4.非专用设备、管道、容器、工具应按规定拆洗或灭菌处理;
5.凡直接接触药品的设备、管道、工具、容器应每天或每批清洗或清理。同一设备连续生产同一无菌产品时,基清洗周期可按生产工艺规程及标准操作规程执行;
6.包装工序清场时,多余的标签及使用说明书等包装材料应全部按规定处理。
三、清场记录及合格证
清场时应填写清场记录,记录内容包括工序名称、上批生产品名、规格、批号、清场日期、清场项目及检查情况、清场人及检查人签字。
清场结束由车间质量员复查合格后发放清场合格证正副本,正本纳入本批批生产记录,副本流入下一批生产记录中,清场合证应规定有效期,超过有效期的应重新进行检查。无上批清场合格证副本,车间不得进行下一批产品的生产。
;包材备案流程备案包材
发明
一种用于治疗肝衰竭的中药灌肠液
状态:审中-实审
申请号:201310607321.3 申请日:2013-11-27
摘要:本发明公开了一种用于治疗肝衰竭的中药组合物,其原料药的重量份为:大黄15-30份,厚朴10-20份,枳实10-20份,地黄20-40份,丹参20-40份,赤芍20-40份,地榆20-40份,紫草20-40份。本发明原料易得且成本低,通过各味药材协同发挥清热解毒、逐瘀泻浊、凉血退黄之功效,与内科治疗具有协同增效作用,显著提高了治疗肝衰竭的有效率。本发明中药组合物制备的灌肠液渗透压为285-315mosm/kg,对肠道壁安全,PH值为5-6,有利于提高疗效。
发明(设计)人: 王波 杨俊清 靳桂贞
主分类号: A61K36/804(2006.01)I
分类号: A61K36/804(2006.01)I A61K9/08(2006.01)I A61P1/16(2006.01)I
关联审评审批是什么
药品登记状态a和i是什么意思?
1、原料药登记状态为“I”有三种情况,第一是单独审评审批未通过,第二是未与制剂注册进行关联,第三是关联审评审批未通过。在原料药登记过程中,只要提交的资料通过审核,药审中心官网都可以查到该原料药,登记状态为“I”。在与药品进行关联审评审批时未通过,原料药登记状态还是显示为“I”,但这并不代表原料药质量不过关,有可能是药品审评不通过,待药品审评通过后,原料药登记状态才变为“A”。
2、标识为“A”的原料药发生技术变更的,按照现行药品注册管理有关规定提交变更申请,经批准后实施。原料药的其他交更应及时在登记平台更新信息,并在每年第一季度提交的上一年年度报告中汇总。
状态标识为“A”的原料药,按照药品进行上市后管理,并开展药品GMP检查。
缘生源的东西可靠吗?
是可靠的。
广州缘生源化妆品有限公司位于广州市白云区人和镇西城工业区,是一家集化妆品OEM/ODM/OBM研发制造、生产销售、策划服务于一体的实力型企业。致力于为客户量身定做自主品牌,从产品策划,产品设计、配方定制、包材选购、生产灌装、包装出货、送检备案,以市场为导向,以科技为依托,以质量求发展服务理念,为客户提供多样化的产品一站式的售后服务。
包材备案都需要准备什么啊?
一般是需要携带与身份相关的证明材料,比如身份证、户口本、营业执照、组织机构代码证等等。按备案性质准备:
1、性质为个人,提供资料:备案书面文档、网站负责人身份证、域名证书、备案核验单(个人签名)、照片。
2、性质为企业,提供资料:备案书面文档、网站负责人身份证、域名证书、备案核验单(负责人签名+盖公章)、照片外加营业执照。
仓库管理员简历自我评价范文
药品与药用原辅料和包装材料实行关联审批,即原辅包与制剂共同审评审批的管理制度,对原辅包不单独进行审评审批。在共同审评审批制度下,药品制剂申请人对选用原料药、药用辅料和药包材的质量负责,若关联的原料药、辅料、包材中有一个未通过审评,则面临被退审的风险。
《国家药监局关于进一步完善药品关联审评审批和监管工作有关事宜的公告》第一条总体要求:
(一)原辅包的使用必须符合药用要求,主要是指原辅包的质量、安全及功能应该满足药品制剂的需要。原辅包与药品制剂关联审评审批由原辅包登记人在登记平台上登记,药品制剂注册申请人提交注册申请时与平台登记资料进行关联;因特殊原因无法在平台登记的原辅包,也可在药品制剂注册申请时,由药品制剂注册申请人一并提供原辅包研究资料。
(二)原辅包登记人负责维护登记平台的登记信息,并对登记资料的真实性和完整性负责。境内原辅包供应商作为原辅包登记人应当对所持有的产品自行登记。境外原辅包供应商可由常驻中国代表机构或委托中国代理机构进行登记,登记资料应当为中文,境外原辅包供应商和代理机构共同对登记资料的真实性和完整性负责。
(三)药品制剂注册申请人申报药品注册申请时,需提供原辅包登记号和原辅包登记人的使用授权书。
(四)药品制剂注册申请人或药品上市许可持有人对药品质量承担主体责任,根据药品注册管理和上市后生产管理的有关要求,对原辅包供应商质量管理体系进行审计,保证符合药用要求。
(五)监管部门对原辅包登记人提交的技术资料负有保密责任,对登记平台的技术信息保密,登记平台只公开登记品种的登记状态标识(A或I)、登记号、品种名称、企业名称(代理机构名称)、企业生产地址、原药品批准文号(如有),原批准证明文件有效期(如有),产品来源、规格、更新日期和其他必要的信息。
深圳市永祥药房连锁有限公司怎么样?
只有制度没有 文化 :要么执行有力,要么执行崩盘!只有文化没有制度:要么自然推动,要么软弱无力!只有文化和制度是相溶匹配的,才能将执行力度发挥到极致!下面是我为大家整理的仓库管理员 简历 自我评价 五篇,希望对您有所帮助。欢迎大家阅读参考学习!
仓库管理员简历自我评价1
时光飞逝,弹指之间,20__年已接近尾声,回首过去的一年,内心不禁感慨万千……时间如梭,又将跨过一个年度之坎。
作为基层管理者,成本是公司的关键之一,对成本管理水平的要求应不断提升,对采购瓶箱、到各部门生产的使用更应加以控制。回顾即将过去的这一年,在公司领导的正确领导下,我们的工作着重于公司的经营方针、宗旨和效益目标上,紧紧围绕公司提出的重点展开工作,紧跟公司各项工作部署。在核算、管理方面做了应尽的职责。
透视,工作的风风雨雨时时在眼前隐现,但我们却必须应对现实,不仅仅要能做的到工作时埋下头去忘我地工作,还要能在回过头的时候,对工作的每一个细节进行检查核对,对工作的 经验 进行评价分析,从怎样节俭时间,如何提高效率,尽量使工作程序化、系统化、条理化、流水化!从而在百尺杆头,更进一步,到达新层次,进入新境界,创新为了更好地做好今后的工作,评价经验、吸取教训,必将有利于自我的前行。
回首过去,是为了更好地面向未来。为了评价经验,发扬成绩,克服不足,现将20__年的工作做如下简要回顾和评价
一、回首过去一年
1、我们正生活在服务经济时代。服务已渗透到生活中的诸多细节,每个人既是享受服务的“客户”,又是为“客户”供给服务的个体。正因如此,我们的工作也应当更完善以为生产服务为中心,来为生产供给更快捷、高效、优质的服务。实实在在做人做事,是我们秉承的理念,尽我们的全力去满足每一个生产细节的要求。确保了2012年生产旺季瓶箱供应,顺利完成了生产任务。
2、能严格执行公司仓库保管制度,防止收发瓶箱差错出现。入库及登帐,检验不合要求瓶源不准入库;做到以公司利益为重,爱护公司财产,不监守自盗。
3、合理安排瓶箱在仓库内的存放次序。按产品种类、规格、等级分区堆码,不得混和乱堆,随着成套瓶区和回退瓶区堆位划线完工,使各堆位摆放比以前更加整齐,坚持库区的整洁简洁。
4、进取配合财务部和采购部。负责定期对仓库产品盘点清仓,做到帐、物、卡三者相符。能真正掌握材料的进、出、存的工作流程,同时也真正做到了物尽其用,人尽其才的作用。
进取配合财务部门做好仓库库存的盘点工作,保证库存报表的每一天上交时间和数据的准确性,真实性。
5、12年塑箱损坏严重,塑箱的管理权限在瓶箱库,可是使用塑箱的是(瓶箱库,包装车间,成品库)。其中大部损坏应当是瓶箱库叉车司机供箱在通道推挤坏,倒一次瓶至少损坏7—10个塑箱,包装车间在卸垛是摔坏塑箱,塑箱卡在链道上,包装车间的员工是用棍打塑箱,洗620ML瓶时码垛机乱码时把塑箱挤坏,成品库转运塑箱瓶时损坏一些。瓶箱库缺少对塑箱使用的监管。
每一天的工作中都有很多问题发生,我们有必要做到要善于发现问题,把握问题,并在第一时间去解决,来提升自身的业务本事。
二、展望来年
在恪守以往取得的成绩和好的工作 方法 外,争取在20__年能改善去年的不足,使工作再上一个新的台阶,特在此列出如下的仓库20__年 工作计划 和工作目标
1、加强日常管理工作。
⑴加强对叉车司机的 入职 培训,督促操作人员严格执行《叉车安全操作规程》进行安全操作,确保操的人身安全。定期维护保养设备,减缓设备的自然磨损,杜绝因人为操作使用和维护保养不当造成事故,监督叉车各岗位操作人员严格按照各种规范操作,对主观因素违反操作规程的人员予以纠正。提升在职叉车司机的安全驾驶意识,防止出现安全事故。
⑵按规定时间瓶箱进行盘点,及时核算出各生产班所使用瓶箱情景。在月终报表中通报给生产主管、及时指出各生产班存在浪费瓶子现象,进取配合各部门查找瓶损非正常损耗分析原因。杜绝后续再出现浪费现象。争取做到低成本高效益的管理理念。
⑶在紧张的工作之余,加强团队建设,打造一个业务全面,工作热情高涨的团队。作为一个管理者,对下属充分做到发挥他们的主观能动性及工作进取性。提高团队的整体素质,树立起开拓创新、务实高效的部门新形象。
⑷作为基层管理者,我充分认识到自我既是一个管理者,更是一个执行者。要想真正把公司成本降低,除了对员工的合理安排调动外,还需要认真实在培训员工,首先要以身作则,这样才能让自我的下属有榜样看,大家都能够主动构成节俭意识。
⑸加强对叉车司机的驾驶技能培训,和安全职责意识,减少倒瓶率,同时要对包装车间在生产使用塑箱过程监管,严禁把塑箱做 其它 用途使用,制订塑箱使用管理规定,职责到人,加大对故意损坏塑箱的惩罚力度。
2、在仓库管理及数据管理本事上提高。
⑴为提高物料的管理,对所有进出仓物料必须按仓库管理制度执行,对经销商严格把关回退瓶质量和数量。为确保采购部、生产部及销售部能及时了解瓶箱库存情景,对金蝶数据及库存日报表需要实时录入。确保在进出仓前查询并录入相关数据再收发料,确保数据的准确性与及时性。
⑵加强对本部门职员的培训学习,真正掌握物料进、出、存的工作流程,使他们真正发挥技术骨干和模范带头作用,使物品能起到物流顺利周转,同时也真正做到物尽其用,人尽其才的作用,使其仓库管理工作得到有效的改善。进取配合采购部和销售部,对库存呆滞物品的积压进行整改,避免原材物料的浪费,节俭原材料,处理部分呆滞物品,并改善仓库物品和堆放位置的紧缺现象,就能给生产周转瓶箱转运供给了合理空间。
⑶重新对仓库库位成套瓶放置进行更有效合理的规划,使成套瓶摆放更加整齐,盘点更加方便,塑造目视仓储管理。
三、瓶箱库提出的提议
车间生产延时和生产变动,应及时尽早通知瓶箱库,瓶箱库好合理的安排叉车司机上班,避免在人资源上的浪费。今年每周都有生产改动不通知瓶箱库,瓶箱库和包装车间信息交流优化,才能提高整个生产效率。
在此祝各位领导和各位同事身体健康!万事如意!
多谢!
仓库管理员简历自我评价2
一、仓库保管员的工作
1、负责仓库大库(原辅料区.阴凉库)、危库、剧毒品库、冷库、中药材库及阴凉库的日常卫生和安全工作及各项记录;
2、责所有有关原辅材料、中药材、危险品、化试、冷藏物品等的入库、出库工作,按标准操作程序和标准管理制度做好各项工作及记录。
二、配合车间生产
1、生产计划,负责制造部固体车间、液体车间、注射剂车间、原料药车间、中药提取车间、合成车间等的分料工作,及时填写相关的记录;
2、配合以上各车间的领料工作,及时填写货位卡,分类帐,核准现场物料等,做到帐目清晰,可查。发现问题及时汇报,改正。
三、配合GMP的认证
1、配合做好了各车间GMP认证所需很多的调帐工作;
2、完成了仓库GMP认证期间的很多帐目清查、整理工作,做到了帐目一目了然,现场整洁,到达了帐、卡、物一致;
3、配合化验中心做好现场核准工作。
四、负责仓库洁净区的管理和清洁工作
1、做好洁净区空调机组的维护工作;
2、每个星期一做好洁净区的清洁工作及填写相关记录;
3、化验中心、质保部取样后,做好清洁工作;
4、分料后,做好清洁工作及清场记录。
五、配合其他的工作
1、负责中药材外加工所需材料的入库,领料工作及相关记录;
2、负责生命能在我厂合成时所需原辅材料的入库、分料、领料工作及相关记录;
3、负责技研部做小试或新产品开发所需物料的入库、分料、领料工作及相关记录;
4、配合化验中心的取样工作;
5、每月协助财务做好盘点工作;
6、配合成品保管员做好出库、退货、搬运工作,辅助包材保管员做好日常工作。
以上为本人工作评价,请领导批评指正。
仓库管理员简历自我评价3
时间过的真快,转眼__年就要过去,我们即将迎来新的一年。回想这一年的工作来,在公司领导的正确指挥和同事们的并肩努力下,我们仓库管理员的各项工作始终围绕着库存货物安全、库存数据准确、作业标准规范化、热情服务高质量的目标开展工作。现将__年的不足和缺陷评价出来,以望在今后的工作中加以提高和改善。
一、仓库保管工作
第一:出入库管理,见单作业,凭什么能够收发,凭什么进行收发,单据,认真核实,细心清点,当面交接,当面签章;认真按严密的程序办事。
第二:订购管理,仓管担当部份物控职能,理解安全库存,周转库存,最高存量,采购批量,严密跟进每一款物品的进销存,及时提请欠料申购;一方面要保证能持续供应产线,一方面保证能降低库存,一方面要兼顾采购周期及采购成本,找平衡,统计每款物料的各月领用规律,理解采购的经济批量与周期,综合分析好,连续关注。
第三:5s管理,各项现场管理工作的基础,对仓库管理一样重要,仓库的定点定位定量原则,就是要做好整顿工作,仓库的物品分仓分类分管,整理好了才能分,仓库的物品多,在接收搬运储存交付的各类活动中,都需要一个有序整洁的工作环境,仅有做好整理整顿清扫工作,才能保证这些工作的效率与质量。仓库管理是一件长期的重复性工作,所以必须养成一个好习惯,天天坚持做好,日清日洁,5s的素养对此有十分大的帮忙。
第四:先进先出管理,是仓库管理的三大原则之一,不执行先进先出易造成超期库存,易产生物品变质,易产生工程变更的报废风险。执行先进先出的办法有色标法,双区库品移位法,重力法,最严密批次记录台账追索法等。
二、存在问题及计划
在过去的工作中,在公司领导和同事的帮忙下,经过自我的努力,顺利完成了岗位规定的工作,也使客户对自我有了较高地评价。但仅仅限制于目前工作岗位,对公司其他业务和流程几乎一片空白,公司系统也没有较深入地了解和认识,对物流专业知识也有很大的不足。
为了适应新形势、谋划新发展,我决心在今后的工作中,发扬成绩、克服不足、加强学习、努力工作,为新的一年做好准备工作,决心做好以下几方面:
1、力争在提高自身专业素质上取得新突破,经过制定 学习计划 ,做到与时俱进,当然不仅仅要学习书上的东西,并且要学习做人的道理,处世的方法,不断增强服务客户的本事,增强与客户沟通的本事,增强解决客户问题的本事,使自我成为一个综合素质比较好的员工。加强思想认识,做到学以致用。
2、要坚持个人自学,经过阅读物流专业知识书刊,利用自我的业余时间加强学习。
3、进取参与公司各类新知识的培训,及时更新自我的知识,提高自我的工作和专业本事,虚心向同事学习,取他人之长,补自我之短。
4、加强物流管理、供应链 管理知识 方面的学习,并在工作中不断应用这些知识,做到理论实际相结合,不断发现工作的问题,使自我和公司能够共同提高。五、确立目标,不折扣行动,大胆思考,细心求证,力求做得更好。
在新的一年里我将努力学习、评价经验、克服不足、再接再厉、一如既往的做好我的本职工作,努力使我在仓库管理员的位置上有更大的起色,与同事劲往一处使、心往一处想,不计较得失,只期望把工作圆满完成,决不辜负领导对我的信任和期待。这份仓库管理员的职业是我人生很大的财富,我真心地感激那些曾指导和帮忙过我的领导和同事们。
今后我还要继续脚踏实地、勤勤恳恳、认认真真、努力完成各项工作。要自觉地做好每一项工作,就必须正视自我的工作,无论工作是繁重、繁忙还是清闲,都要适应那里的环境,要用进取的态度去完成领导交给的每一份工作,使自我在普通的岗位上发挥自我的光和热!
仓库管理员简历自我评价4
仓库管理员在一个企业中扮演着重要的主角,对仓库管理员要严格要求及管理,今日就给大家晒晒我们公司的仓库管理员工作评价,期望大家能从这份仓库管理员工作评价中学到一些东西。
我于三月份进入公司后,担任公司仓库管理员职位,现将这段时间的工作评价及工作体会叙述如下。
刚进入公司时,应对陌生的环境和工作,我感到无从下手、充满迷茫,对业务操作也是一窍不通,连一些最简单的工作术语都不懂。在公司领导合理安排岗位和同事的帮忙下,很快便对工作业务有了必须掌握,较好地熟悉了入库操作、在库管理、出库操作等。在公司领导的指导和同事的帮忙下,目前已经熟练工作,能准确、及时地与客户协调处理异常情景,能较好地处理各种工作细节和服从上级、公司的工作安排和管理制度。
同时,在领导指导、同事帮忙以及自身的努力下,我对仓库管理工作也有了更深刻的认识。具体而言:1、对仓库的认识,熟悉了马士基、三运仓库基本情景,包括库房库区、货架、货品摆放等;2、对流程的认识,熟悉马士基仓库的进出库操作流程和系统流程、三运仓库的操作流程和系统流程;QC流程;增值服务操作流程;异常处理流程;盘点流程等;3、对管理的认识,较好地熟悉了5S管理;仓库安全管理;库区规划;货品摆放;成本节俭;人员安排等;4、对职责的认识,明白了团队的重要性;工作合理安排、保障效率的重要性;较好地协调本组人员的工作和保障准确性;对工作能够负责和能够按时顺利完成。
工作体会:
1、高效服务,全力做好客户服务工作我们的工作本职是服务,服务客户是我们赖以生存的主旋律,仅有做好了客户服务,得到了客户的认可。客户才会真正地认同我们。能做到高效服务,对于客户的电话咨询,我都耐心解释并给予解决,客户提到的问题和需要,都能及时解答和解决。
2、专业学习是做好工作的动力源泉我们的工作价值是什么是在工作中,得到不断地提升,不断地去学习得到提高。假如我们甘于落后,那么我们的价值将会一降再降,直到自我都不能认可自我。专业的学习,使自我的实际操作得到理论的支持,理论知识得到实际操作的验证,不断地提升不断地提高,才真正是我们的工作价值。点的精通,线的发展,交织成面的扩张,使自我能够覆盖更大的领域,才能在各方面不断地提升自我。
3、因势而变,顺势而为,全力做好自我在各种突发情景和紧急中,我迅速转变思路,找准自我的工作定位,进取和同事讨论改善方法。讨论在工作过程中的问题,有一些专业上不懂的地方我虚心向其他有经验的同事学习。
仓库管理员简历自我评价5
回首今年的工作,有与同事的联手攻关艰辛,也有遇到困难和挫折的惆怅,时间过得飞快,不知不觉中,充满期望的一年伴随着新年伊始而即将来临。
现就本年度相关工作作出如下评价:
一、虚心学习
在最短时间内熟悉自我所管物料的规格以及所属供应商的区分,尽快熟悉公司内部的操作流程。
二、心系本职工作,落实工作职责制
努力配合各部门完成的入库和出库工作,争取更加完善仓库管理制度,对于本人工作中的失职勇于承担职责,并杜绝再次出现类似失职事件的发生。
三、加强检查仓库内部的安全设施
确保所管的物料的防尘、防潮以及防盗工作,每一天对当天进出物料进行抽盘,确保常用物料的账目与实物的准确率到达95%以上。
四、总的看来还有存在不足的地方,亟待我们去解决的问题,主要表此刻以下方面:
1、仓库收发料区大门,时常处于敞开状态,原材料仓内置为良品、不良品以及报废料的放置区,来料未经检验,可列为不明状态物料,若将其放置于材料仓不太妥当。
2、仓库办公室为仓管人员办公之地,非仓库人员却随意进出仓库办公室,还曾出现办公文具被损坏现象。
3、材料仓非仓库人员随意进出,让人感觉就像菜市场一样,完全无视仓管员的存在,若送货员搬货进仓都有仓管员随行。
4、账目管理混乱,每月对物料进行抽盘,实物与系统账目的准确率几乎为20%。
5、库存样机全部裸机入库,导致业务出货为了寻找适宜包材很多浪费时间。
五、下一步打算
针对本年中存在的不足,为了更加完善管理制度,做好新一年的工作突出,作出以下几个方面。
1、严格执行仓库管理制度,禁止非仓库人员随意进入仓库。
2、加强仓库物料账目管理。
3、库存样机必须配包材入库,节省仓库和业务的工作时间。
4、系统内存在一个物料多种编码的情景,对于不使用的物料编码进行删除整改。
5、库内呆滞料和报废品过多,很多占用库存且不美观,及时处理增加空间利用率。
6、财务应加大对仓库数据的监控。
六、个人认为给予改善的相关方面
1、生产退料过于频繁,导致有时仓库办公室人满为患。
提议在生产部购置针式打印机一台,打好单据后到仓库退料或者领料:除了急需出货的物料,其他物料一天退料2次。
2、生产退料不写生产任务订单号
提议生产退料必须写明该物料的所属订单号。
3、生产领料实物编码和数量与单据上的物料编码和数量不一致
提议生产任务订单领料必须由PMC开出的生产领料单并有PMC签字的单据方可发料,若一个BOM的同类物料有多种编码,必须有工程下发的更改通知单。
4、生产领料和业务发货、采购到料无计划生产当天要使用的物料,PMC应提前4个小时打出领料单给仓管员备料并把物料放置发料区;业务当天需要发的货物必须在当天生成发货计划表通知仓库和生产部,计划表必须包含发货时间,精确到分。采购必须提前一天告知仓库当天到料计划和数量,便于仓库安排存储空间。
5、成品往往是先出库后入库,成品机入库单无相关人员签字。
成品必须先入库再出库,否则财务无法预算成本。生产根据发货计划表的发货时间提前入库,入库单必须有生产主管、PMC以及品质检验员签字方可生效,仓管员确认手续齐全到生产部确认入库数量以及产品规格,根据由财务审核的出库单将货物交给发货员。
6、调拨单的含义的误解。
调拨单的作用分为仓库与仓库之间的调拨和仓位与仓位之间的调拨,而不是部门之间的调拨。对于目前生产领用不算调拨,调拨出良品,调拨回不良品完全不贴合调拨单的根本使用意义。
提议取消部门之间的调拨单,生产订单领料超领必须有生产主管和PMC以及财务签字方可生效,品质领料采取领料单而非调拨单,且该单据有品质主管签字,业务领取样品机必须有销售样品领取单,且有业务经理签字。
7、职责制度不到位
生产超领以及业务样品借料有多少未归还仓库是由财务成本会计核算,生产任务单下发多少,欠料多少,订单成品入库多少应由PMC进行跟踪,采购订单物料到货多少,退货多少以及补退货多少应由采购进行跟踪。目前我司要求以上都由仓管员跟踪完全属于职责过度。仓管员的职责是凭单领料,凭单发料,保管物料的外在品质以及物料的物帐卡一致。
8、业务样机领取频繁
样机很多是一种机子一天领出或者归还多次,业务回复业务部没有专门放置样品的柜子,提议业务部购买几个样品展柜,一则避免样机领取频繁,二则便于客户参观。
9、先入库后检验这个完全不贴合正规流程
正规系统都有品质部这个模块,品质检验后系统会自动入库,仓管员再根据系统入库单打出纸质单据,作为入库依据交由财务。
10、相关整体流程
材料入库流程:供应商快递送货—仓管员确认采购订单号、规格型号以及数量、物料编码—仓管员在系统品质模块进行来料登记填写—品质收到送检信息后到待检区检验送检物料—检验完毕(合格和特采系统会自动入库并生成入库单,拒收直接退货)—仓管员根据入库单打出纸质单据并将检验好的物料入仓归位。
生产领料流程:
1、生产任务单领料:PMC提前4小时打出生产任务领料单交由仓管员把物料放置于仓库发料区内—领料人根据领料单确认物料规格以及物料编码、数量—确认无误后签字并领走。
2、非正常领料:领料人打出领料单—部门主管、PMC签字—仓库备料(备料时间至少5分钟)—领料员确认物料规格以及物料编码、数量—确认无误后签字并领走。
3、生产超领:生产打出超领单—PMC、成本会计签字—仓库备料—领料人员确认物料规格以及物料编码、数量—确认无误后签字并领走。
生产退料流程:生产整理出需退仓物料—在品质模块填写送检登记—品质确认状态—品质开出检验 报告 (检验报告必须包含物料规格以及编码、供应商)—PMC和部门主管签字—仓库确认签字。
产成品或者半成品入库流程:生产开出入库单—在系统品质模块填写生产成品送检登记表—品质检验开出出货报告并签字—PMC和部门主管签字—仓管员确认数量,规格以及外箱标识是否齐全—确认无误签字。
产成品出货流程:发货员开具销售出库单—财务审核并签字—仓管确认手续齐全将货物交由发货员—发货员确认产品型号以及数量并签字。
销售退货流程:客户退货—业务文员确认退货型号以及数量—开具销售退货单—财务审核并签字—业务文员携销售退货单以及客退品交给仓库—仓库确认型号和数量签字。
11、呆滞料处理方法
(1)工程确认能用于公司其他产品的物料优先使用。
(2)对于市场上存在价值且我司无法使用的物料,进行与其他公司或者供应商进行换料或者折价出售
(3)对于市场上无法回收的物料进行就地报废。
(4)呆滞料放的时间长不但不会增值只会贬值,且大大占用空间利用率,且其外箱灰尘过多,给客户参观带来不美观的视觉,并非库存过多就证明生意越好,相反,库存越多,越体现出公司的周转率低,公司效益的不好。
12、注意事项:
个人系统账号密码属于保密,除持有者明白外任何人不得知晓,防止他人栽赃,若持有人自我泄露,造成的后果由持有人承担。
仓库管理员简历 自我评价 范文 相关 文章 :
★ 仓库管理员自我评价简历五篇
★ 应聘仓管员简历优秀自我评价
★ 仓管员个人简历自我评价
★ 仓管员个人自我评价范文
★ 仓管人员优秀简历自我评价
★ 应聘仓管员个人简历自我评价
★ 2019仓管员简历自我评价范文
★ 2019仓管员优秀简历自我评价
★ 物流个人简历自我评价范文
★ 库管求职简历自我评价
深圳市永祥药房连锁有限公司是2001-01-12在广东省深圳市龙岗区注册成立的有限责任公司,注册地址位于深圳市龙岗区布吉街道宝丽路100号6号厂房401。
深圳市永祥药房连锁有限公司的统一社会信用代码/注册号是914403007261806020,企业法人张洪霞,目前企业处于开业状态。
深圳市永祥药房连锁有限公司的经营范围是:网上从事国内贸易、网上从事信息咨询(不含限制项目)、网上从事广告业务、经营电子商务、数据库服务、数据库管理;农产品的销售;消毒卫生用品的销售;计算机软件、信息系统软件的开发、销售;信息系统设计、集成、运行维护;信息技术咨询;化妆品的销售及相关信息咨询;日用百货的销售;企业管理咨询;品牌管理策划;市场营销策划;国内贸易(法律、行政法规、决定规定在登记前须经批准的项目除外);货物及技术进出口(法律、行政法规禁止的项目除外;法律、行政法规限制的项目须得许可后方可经营)。^中药材、中药饮片、中成药、化学原料药、化学药制剂、抗生素原料药、抗生素制剂、生化药品的批发、生物制品(除疫苗);中药饮片、中成药、化学药制剂、抗生素制剂、生化药品、生物制品(除疫苗)的零售(连锁);预包装食品销售(含冷藏冷冻食品)、特殊食品销售(保健食品销售、其他婴幼儿配方乳粉销售、特殊医学用途配方食品销售);三类医疗器械批发;二类医疗器械批零兼营;网上销售药品。在广东省,相近经营范围的公司总注册资本为1664996万元,主要资本集中在100-1000万和1000-5000万规模的企业中,共5427家。本省范围内,当前企业的注册资本属于良好。
深圳市永祥药房连锁有限公司对外投资13家公司,具有166处分支机构。
通过百度企业信用查看深圳市永祥药房连锁有限公司更多信息和资讯。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。