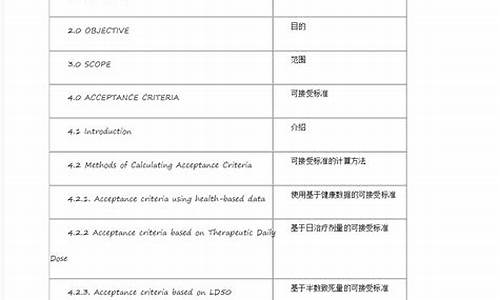
原料药合成车间级别-原料药合成车间

(1)原料的危害分析:首先要清楚使用的是什么原料或主要成分;这些原料表面和原料中是否可能存在有关的微生物,如果有,是什么微生物;原料是否有毒性或含有毒性物质,如果有,可能是什么毒性物质。具体应根据原料的品种、来源、规格、质量指标等情况作具体分析,一般从细菌性(菌落总数、大肠菌群和相关的致病菌等)、化学性(农药、杀虫剂、抗生素、洗消剂、激素、化学污染物等)和物理性(玻璃碎片、小石子、金属碎片等杂质)方面进行危害分析。此外,企业对生产所用的水和辅料的卫生状况也应加以危害分析。 (2)加工过程的危害分析:在加热或消毒过程中,有关微生物或毒性物质是否能被灭绝;经加热或消毒后是否会被有关的微生物或毒素进一步污染;如果使用防腐剂,防腐剂浓度是否足以能防止有关的微生物生长。在制作和贮藏过程中,有哪些有害微生物会存在,是否有繁殖和产生毒素的可能性;每一制作,加工和贮存过程需要多少时间,这些时间是否有利于微生物的生长繁殖和产生毒素。为产品需要而加入的有关成分(如硒、铬、亚硝酸钠等)是否超过规定限量。产品的水分活度是否有助于微生物的生长;产品的PH值是否能防止微生物生长或灭活特殊致病菌。产品的包装材料、包装方式能否防止微生物污染、细菌侵袭及毒素物质形成(有氧或无氧包装)。产品的贮存方式及环境条件是否会给某些微生物的生长、繁殖创造条件。含有生物活性物质的产品是否会受到微生物的污染;生产工艺是否能确保最终产品的功效成分不损失、不破坏、不转化和不产生有害中间体。产品的运输条件和运输过程是否有利于微生物生长、繁殖。上述有害成分是否可能在流通、贮藏时形成对人体健康不安全的因素。 (3)从业人员的危害分析:在操作过程中,从业人员是否明确自己的健康和个人卫生会影响加工产品安全的重要性;自己是否患有碍食品卫生的疾病(痢疾、伤寒、病毒性肝炎等消化道传染病(包括病原携带者),活动性肺结核,化脓性或渗出性皮肤病以及其它有碍食品卫生的疾病);是否有感染病灶(如咽喉部、鼻腔部金**葡萄球菌携带者)。是否经常洗头、洗澡、剪指甲、换衣服;工作服是否保持每天清洁;是否穿上清洁的工作服、帽,鞋后才上岗;暂时离开与自己工作岗位无关的场所(会议室、食堂、盥洗室等)是否脱掉工作服;是否能做到在任何时候都会洗净双手上岗,接触直接入口的食品是否洗净并消毒双手;消毒水的浓度是否保持一直有效;双手的消毒是否能达到要求;从业人员是否清楚如果不按要作可能会出现的各种危害及严重后果。 (4)设计、设备与设施的危害分析:厂房设计、设备与设施的配置是否符合GBl4881的要求;工艺流程布置是否将原材料与成品分开;人流与物流是否有交叉污染存在;产品是否按照生产工艺和卫生、质量要求,划分洁净级别;洁净级别是否能满足生产加工保健食品对空气净化的需要;生产片剂、胶囊、丸剂以及不能在最后容器中灭菌的口服液等产品是否采用十万级洁净厂房;十万级洁净级区是否安装了具有过滤装置的相应的净化空调设备;洁净厂房的温度和相对湿度是否与生产工艺要求相适应;下水道、洗手间及其它卫生清洁设施是否会对保健食品的生产带来污染。此外,生产过程是否会产生不安全因素,如玻璃容器的破碎、维修机械设备时落下的碎金属和机油渗漏等;设备清洗消毒是否符合要求;洗涤剂、消毒剂是否会产生不安全因素;包装区域是否具备正压条件,设备及各种仪器仪表(如温度、时间)运行是否稳定。
药企或者医药研发单位里面的制剂部,合成部,质量部,中试车间等等 这些部门分别是干什么的?
比较适合。宜昌人福原料药车间是面向全国的一家原料药生产基地,拥有完备的原料药制造设备和现代化的生产工艺,它符合国家有关职业健康安全要求,适合女性工作,可以为女性提供安全、平等的就业机会。宜昌人福原料药车间是位于湖北省宜昌市的一家集研发、生产、销售为一体的原料药制造基地,其拥有多条国外先进的原料药制造设备,以及现代化的萃取、干燥、粉碎、包装等全套生产工艺。
制药厂那个车间最累
制剂部:主要进行药物剂型的开发,像什么片剂啊、颗粒剂、注射剂啊、缓控释制剂啊等。
合成部:主要是是原料药或中间体的合成,包括化学合成、生物合成等方法。化学合成包括有机合成和无机合成。生物合成包括全生物合成和部分生物及部分化学合成。
质量部:主要是主要是进行质量控制,像检查质量何不合格啊等等的。
中试车间:主要是药物从研发阶段,首先要经历小试,中试,大生产三个阶段。而中试车间就是从小试到中试,用于放大的车间。
原料药GMP车间设计装修应符合什么要求?
配制车间最累。制药厂制药厂是指生产抗生素、化学合成药、生物化学药、植物化学药等原料药和各种药物制剂或中药的工厂,该厂中最累的为配置车间因为需要了解药品的性质在分配时得把握分量和各种药性所以十分消耗精力所以最累,加工车间和其他车间都是机器化生产对于体力精力消耗少。
原料药GMP车间设计、建设、装修要求,SICOLAB
一、非无菌原料药精制、干燥、粉碎、包装等生产操作的暴露环境应当按照D级洁净区的要求设置。
二、质量标准中有热原或细菌内毒素等检验项目的,厂房的设计应当特别注意防止微生物污染,根据产品的预定用途、工艺要求采取相应的控制措施。
三、质量控制实验室通常应当与生产区分开。当生产操作不影响检验结果的准确性,且检验操作对生产也无不利影响时,中间控制实验室可设在生产区内。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。