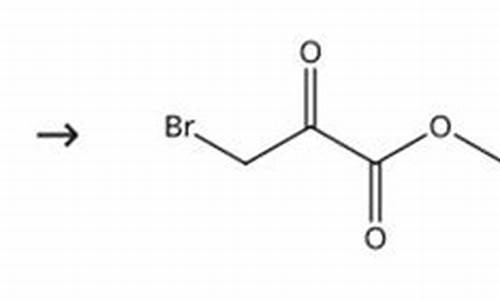
原料药申报状态A和i-原料药申报注册需要提交的内容

研发过程需要经过药物的设计与筛选、化学合成与改造、药剂学与药动学研究、工艺与制剂、质量检测与控制、安全性与临床评价、市场反馈等等许多步骤,面临问题复杂。
按照工作内容的不同可将新药研发分为四个阶段:发现和甄别、临床前研究、临床研究、新药申报及后续工作。
第一、发现和甄别包括基础研究和应用研究(包括药品制备和初筛),发现和筛选药物来源。
第二、临床前研究包括为了确定药物安全性和有效性所作的实验和动物试验及其准备工作,既药学、药效、药理和毒理并进行临床申报。
第三、临床研究包括I(初步临床药理学研究、人体安全性研究),II(治疗作用初步评价、安全性研究,III期临床试验及其准备工作(扩大临床试验、特殊临床试验、补充临床试验、不良反应观察)。
第四、新药申报及后续工作包括新药申报,以及由于SFDA(国家食品药品监督管理局)对新药申报进行复查所要求做的额外工作。
进口药用辅料怎么登记?
在输液领域,科伦药业已占据龙头地位,其还构建起了从中间体、原料药到制剂的抗生素全产业链护城河;而通过研发体系的建设和多元化的技术创新,其已为长期发展奠定了坚实基础
成立20多年来,科伦药业稳扎稳打,通过持续的产业升级和品种结构调整,已在输液领域占据龙头地位。
2018年科伦药业实现营业收入163.52亿元,同比增长43.00%;实现归母净利润12.13亿元,同比增长62.04%。随着公司抗生素中间体产量释放,输液产品结构持续优化,新产品陆续获批上市,科伦药业有望驶入业绩增长的快车道。
据《投资时报》研究员了解,2018年科伦药业新获批仿制药销售额已接近7亿元。在去年一年内,该公司有18个重要仿制药物连续获批生产,其中中国首仿品种4项,首家一致性评价品种4项,草酸艾司西酞普兰4+7集采中标。后续还有数十个仿制药正在申报生产当中,未来一到两年内有望获批生产。而科伦药业也有望成为中国仿制药龙头企业。
渤海证券近日指出,随着医药行业供给侧改革进一步深化,行业集中度逐步提升,仿制药及高值类耗材价格下行大势所趋,具有突出临床价值的创新药品种或将长期受益。因此建议投资者关注包括科伦药业在内的,以发挥原料药优势、建立仿制药产品集群的原料药制剂一体化企业。
而科伦药业近期来的连续回购行为,也为公司二级市场的投资者持续注入信心。公告显示,截至6月30日,该公司累计实施回购数量为375.6万股,占公司目前总股本的比例为0.17%,成交最高价为23.9元/股,成交最低价为21.23元/股,支付总金额为8545.93万元(包含交易费用等)。
行业龙头地位稳固
科伦药业是一家高度专业化的创新型医药集团,2000年在深交所上市后,科伦立即启动百亿产业投资计划,开始实施“三发驱动、创新增长”的发展战略。
所谓“三发驱动”,即第一台发动机是通过持续的产业升级和品种结构调整,保持科伦在输液领域的绝对领先地位;第二台发动机是通过对优质自然资源的创新性开发利用,构建从中间体、原料药到制剂的抗生素全产业链竞争优势;第三台发动机是通过研发体系的建设和多元化的技术创新,积累企业基业持续发展的驱动力量。
在该战略的指导下,科伦药业成为了一家盈利能力强劲,技术优势突出,护城河深厚的领先医药集团。
目前科伦药业生产和销售包括大容量注射剂(输液)、小容量注射剂(水针)、注射用无菌粉针(含分装粉针及冻干粉针)、片剂、胶囊剂、颗粒剂、口服液、覆膜透析液以及原料药、医药包材、医疗器械,以及抗生素中间体等共计568个品种981种规格的产品。
据《投资时报》研究员了解,科伦药业拥有124个品种共292种规格的输液产品、393个品种共636种规格的其它剂型医药产品、51个品种共53种规格的原料药、10个品种的抗生素中间体、4个品种共7个品规的医用器械,是中国输液行业中品种最为齐全、包装形式最为完备的医药制造企业之一。
大输液一直是该公司的主要业务。2018年科伦药业输液产品实现营业收入98.80亿元,同比增长30.37%。该业务毛利率达到71.18%,行业内市场占有率超过40%。
此外,2017年和2018年科伦药业还有7项肠外营养输液产品获批,随着相关产品的持续丰富,未来有望成为新的增长点。而通过投资石四药股权,科伦药业进一步夯实了行业龙头地位。从产品结构来看,该公司销售的中高端可立袋、软袋,不断取代中低端的塑瓶、玻瓶,有望持续提升大输液营收和盈利能力。
据业内人士介绍称,经过“限抗”、门诊限制输液等政策带来的行业调整,大输液行业逐步筑底,底部基本能够反映刚性的需求。因此,在下半年市场“吃药”行情继续的情况下,科伦药业有望迎来一波强势增长。
重研发业绩待释放
随着国家“4+7”带量采购政策逐渐落地,中国医药行业开始进入了挑战与机遇并存的行业变革新时代,创新将成为医药企业未来发展的关键路径。
成立20多年以来,科伦药业持续发力研发,不断提升核心竞争力。公司稳定的盈利能力和现金流也为高研发投入创造了良好条件。
数据显示,自2012年以来,科伦药业研发投入超过40亿元,仅2018年一年的研发投入就达到11.14亿元,这个金额在所有A股医药上市公司中排名第六。2012年至2018年内,公司研发支付复合增长率达到31%。此外,公司研发费用支付占归母净利润比值达到72.98%,在同业公司中排名第一位。
2018年,科伦药业获得创新药物临床试验批件5项,其中创新小分子2项,生物大分子3项,向美国FDA提出创新药物IND申请1项,并已获准开展临床研究;KL-A167进入关键临床Ⅱ期,KL-A166注射液在中、美同步进行I期临床研究标志着科伦药业的药物研究迈出了国际化坚实步伐。
大批人才的引进也为科伦药业的研究发展注入动力。2017年8月,科伦研究院启动了“百名博士招募计划”,面向国内外各大院校及科研机构招募百名优秀博士及博士后。截至2018年年底,科伦药业博士博士及以上学历人员有223人;本科以上学历人员数量为4781人,占总员工数比例为23.92%。丰富的人才储备为公司的未来发展奠定了坚实的基础。
目前该公司项目储备丰富,以仿制药为代表的新品种不断获批。一方面科伦药业可以通过持续的品种申报,形成产品集群,借助公司强大的招标准入及销售能力,实现销售的迅速增长;另一方面,该公司可以积极推进一致性评价,参与集中采购贡献增量,同时加强上游原料的掌控,形成一体化竞争优势。
有业内人士表示,近年来供给侧改革持续深入推进,环保态势持续趋严,原料药及中间体的行业进入壁垒进一步提升,未来有成本优势的企业有望进一步胜出,而以科伦药业为代表的构筑起强大护城河的企业发展前景广阔。
?
gmp认证怎么申报
1、生产者合法生产资格证明。 2、申报品种生产企业授权的中国代理机构申报的授权文件、公证文件和中文译本。申报品种生产企业中国代理机构的工商许可证复印件或中国常驻代表机构登记证复印件。 3.申报品种在国外的生产、销售、应用情况、在中国申请注册的理由及其中文译文。 4、申报品种的配方、原辅材料标准及原辅材料检测报告。 5、申报品种的生产工艺资料及其中文译文。 6、与申报品种包装的药品联合进行的稳定性试验研究资料(包括试验药品的质量标准)。七、申报品种的质量标准。 (如果是企业标准,还应提供编制说明)。 8、三批申报品种生产企业自检报告原件。 9、申报品种的生产厂区和洁净室(区)平面图。 10、洁净室(区)洁净度检测报告。如需注册药包材,请联系GJPC
药物主文件 DMF是干嘛的啊? 有哪位知道吗? 我们要出口苯甲酸钠 一个客户德国的要这个东西
一、申报企业到省局受理大厅提交认证申请和申报材料
相关材料:
1 药品GMP认证申请书(一式四份)
填写细节要求:
a、企业名称、注册地址、生产地址应与《药品生产许可证》一致;
b、企业法人、企业负责人应与《药品生产许可证》一致;
注意:企业填报的联系人应熟悉企业生产、质量管理情况,****应有效、快捷。
c、企业申请认证范围应在《药品生产许可证》生产许可范围;
d、企业申请认证剂型应与该品种的注册批件剂型一致;
e、中药丸剂申请认证时应展开,如:丸剂(蜜丸、水蜜丸、水丸、浓缩丸、微丸、糊丸、蜡丸) ;
注意:相近剂型的确认-----喷雾剂和气雾剂、合剂和口服液、口服液和口服溶液剂等等
f、认证品种中有青霉素类、头孢菌素类、激素类、抗肿瘤药、避孕药、放射品应注明;
g、原料药认证应注明原料药名称;
h、既有口服也有外用的制剂,外用的应在制剂后注明外用。
i、医用氧企业认证申请范围应注明气态、液态;
j、中药饮片企业认证申请范围应明确饮片的炮制方法,如:中药饮片〔净制,切制,炮炙(炒、烫、煅、制炭、蒸、煮、炖、燀、酒制、醋制、盐制、姜汁炙、蜜炙、油炙、水飞、煨),粉碎(不包括直接口服饮片),包括毒性饮片的净制、切制、炒制与蒸煮制〕;
k、企业申请认证范围有中药前处理及提取车间的应予以注明;
m、企业申请认证范围有动物脏器、组织的洗涤、提取车间的应予以注明。
注意:企业中药前处理及提取委托生产的应在安监处办理相关委托手续。
2 GMP认证之《药品生产企业许可证》和《营业执照》复印件
复印件细节要求:a.证照应在有效期内b.《药品生产许可证》生产范围应涵盖认证申请范围,否则不予受理c.属新增生产线、生产地址、生产范围的,应在《药品生产许可证》变更完成后申请认证注意: 企业首次认证或新增生产线、生产范围的,认证时须报送该范围三批试生产记录复 印件。
3 GMP认证之药品生产管理和质量管理自查情况
细节要求:
a.企业概况和历史沿革情况应包含以下内容:
企业原名或前身,改为现公司的时间,企业占地面积,建筑面积、绿化面积,绿化率等;通过GMP认证的情况;本次申请认证车间的竣工时间,面积,净化级别及面积,年设计生产能力,车间生产品种的情况等。
b.企业GMP实施情况应包含以下内容:
前次认证缺陷项目的改正情况,到期认证的应提供原认证GMP证书复印件及缺陷项目的整改情况;
人员培训情况;
企业负责人、生产、质量管理人员及其他技术人员情况;
本次认证品种相对应的车间及生产线情况;
原料药应分别写明合成及精制车间情况;
如有原料药多品种共用生产线情况,应详细说明;
本次认证各剂型生产线车间分布情况;
本次认证品种车间洁净级别;
仓储情况并注明阴凉库情况和危险品库情况;
化验室情况;
公用设施,水、电、汽供应情况;
工艺用水制备情况;
空气净化系统情况;
物料管理情况;
卫生管理情况;
生产管理情况;
质量管理情况;
安全消防情况;
三废处理情况。
4GMP认证之药品生产企业组织机构图
细节要求:a.应有合理的组织机构图,并注明各部门名称、相互关系、部门负责人;b.企业质量管理部门应由企业负责人直接领导c.质量管理部门负责人与生产部门负责人不能兼任
5 药品生产企业负责人、部门负责人简历;依法经过资格认定的药学及相关专业技术人员、工程技术人员、技术工人登记表,并标明所在部门及岗位;高、中、初级技术人员占全体员工的比例情况表。
5 GMP认证之相关人员5.1 药品生产企业负责人、部门负责人简历注:企业负责人、部门负责人简历应包括受教育情况、每一时段工作情况,特别是从事药品生产、经营情况。 新条款要求主管生产和质量的企业负责人、部门负责人都应具医药或相关专业大专以上学历; 中药制剂企业主管生产和质量的企业负责人、部门负责人应具有中药专业知识。5.2 依法经过资格认定的药学及相关专业技术人员、工程技术人员、技术工人登记表,并标明所在部门及岗位表格要求:姓名,学历,毕业学校,专业,职称,职务,从药年限等5.3 高、中、初级技术人员占全体员工的比例情况表
6 GMP认证之药品生产企业生产范围剂型和品种表
6.1 药品生产企业生产范围全部剂型和品种表;
有青霉素类,头孢菌素类,性激素类避孕药,激素类,抗肿瘤类品种的应予注明
表格要求:表中应包含通用名,规格,剂型,批准文号等字段
6.2 申请认证范围剂型和品种表(注明常年生产品种);
有青霉素类,头孢菌素类,性激素类避孕药,激素类,抗肿瘤类品种的应予注明
表格要求:表中应包含通用名,规格,剂型,执行标准,批准文号等字段,并注明常年生产品种
6.3 生产批件(或新药证书)等有关文件资料的复印件;
6.4 常年生产品种的质量标准;
[注:中药饮片生产企业需提供加工炮制的全部中药饮片品种表;申请认证炮制加工范围和炮制加工品种表(注明常年生产品种),包括依据标准及质量标准等;]
7 GMP认证之药品生产企业周围环境图、总平面布置图、仓储平面布置图、质量检验场所平面布置图(含动物室)
7 药品生产企业周围环境图、总平面布置图、仓储平面布置图、质量检验场所平面布置图(含动物室)
详细要求:
周围环境图、总平面布置图要求:
a.药品生产企业周围环境图应注明企业周围道路、 相邻建筑物、 相邻单位的名称。
b.药品生产企业总平面布置图应注明所有车间位置、名称或车间编号,并注明申请认证车间位置、名称或车间编号,常年风向。
仓储平面布置图要求:
注明注明企业仓储位置,注明危险品库位置;
需注明合格品库、不合格品库、阴凉库、危险品库等位置;
应注明原料库、成品库、包材库、标签库及特殊管理药品库位置;
中药制剂企业应注明中药材库、净药材库位置。
质量检验场所平面布置图要求:
注明质检场所位置;
质量检验场所平面图需注明理化室、仪器室、留样室等各功能间位置;
微生物限度测定室、阳性菌室、无菌室、生物效价检测室应注明位置及洁净级别。
8 GMP认证之药品生产车间概况及工艺布局平面图
8 药品生产车间概况及工艺布局平面图
应包括所在建筑物每层用途和车间的平面布局、建筑面积、洁净区、空气净化系统等情况。其中对β-内酰胺类、避孕药、激素类、抗肿瘤类、放射品等的生产区域、空气净化系统及设备情况进行重点描述;
·
8.1 生产车间工艺布局平面图
应注明生产车间各功能间名称;
中药前处理车间、中药提取车间、动物脏器,组织洗涤车间,也应有工艺布局平面图;
应注明各功能间空气洁净度等级;
应标明人流物流流向
·
8.2 生产车间工艺设备平面图
应注明生产车间各功能间使用设备名称;
中药提取车间使用设备较大、占用多层空间时应标明每层设备;
部分设备辅机与主机不再同一洁净级别的应注明。
原料药应有合成工序、精制工序设备平面图;
企业的工艺设备应与所生产品种工艺相匹配;
激素类、抗肿瘤类药物使用的独立设备应标明。
·
8.3 空气净化系统的送风、回风、排风平面布置图
洁净车间风管平面图中送风口、回风口和排风口的应明确标识;
送风管、回风管、排风管应该清晰明确
常见问题:
企业质量检验场所洁净区送风、回风、排风平面布置图是最易漏报项。
空气净化系统送风图不清晰
空气净化系统送风图送风不够
空气净化系统送风图管道不全
空气净化系统送风管道图未按要求
空气净化系统回排风图不清晰
洁净区、普区间无缓冲
洁净区与厕所共用回风
9 GMP认证之申请认证型或品种的工艺流程图,并注明主要过程控制点及控制项目
本次申请认证剂型、品种工艺流程图应齐全;
应有工艺控制点及控制项目;
中药制剂工艺含前处理及提取的应有前处理提取工艺流程图;
生化制剂工艺含前处理的应有前处理工艺流程图;
原料药应包括全部批准生产工艺;
工艺流程图应注明工艺过程的洁净级别;
工艺流程应与质量标准一致 。
10 GMP认证之药品生产企业(车间)的关键工序、主要设备、制水系统及空气净化系统的验证情况;检验仪器、仪表、衡器校验情况
10 药品生产企业(车间)的关键工序、主要设备、制水系统及空气净化系统的验证情况和检验仪器、仪表、衡器校验情况
细节描述:
关键工序验证应能代表申请认证品种、剂型的整个生产过程。如:企业同时有中药制剂和化药制剂验证时应选中药制剂进行验证,应包括中药前处理及提取;
主要设备验证应包括设备验证情况应与工艺流程图和设备平面图上的内容相匹配;
共用设备应有清洗验证情况;
制水系统验证应包括整个使用点验证情况;
空气净化系统验证应包括每一个功能间;
本次申请认证剂型及原料药所有品种都应验证。
11 GMP认证之检验仪器、仪表、量具、衡器校验情况
相关细节:
企业应按照质量检验标准的要求配备成品的所有质量检验仪器;
需要委托检验的,应符合《国食药监安[2004]108号:关于药品GMP认证过程中有关具体事宜的通知》要求,并且受托方应有计量认证证书;
应有相关仪器、仪表、衡器的校验情况,包括校验日期、校验周期和校验单位等。
12 GMP认证之药品生产企业(车间)生产管理、质量管理文件目录
12 GMP认证之药品生产企业(车间)生产管理、质量管理文件目录
注意:有特殊要求的药品等的管理文件,
如毒麻物料管理相关文件
13 GMP认证之企业符合消防和环保要求的证明文件
gmp认证细节:
消防证明应是公安消防部门出具的相关证明或证书,其他任何证明无效;
环保证明应是环保监测部门出具的废水、废渣、废气的监测报告,环评部门出具的环评报告不予认可。
二、省局药品安全监管处对申报材料形式审查 (5个工作日)
三、认证中心对申报材料进行技术审查 (10个工作日)
四、认证中心制定现场检查方案(10个工作日)
五、省局审批方案 (10个工作日)
六、认证中心组织实施认证现场检查 (10个工作日)
七、认证中心对现场检查报告进行初审 (10个工作日)
八、省局对认证初审意见进行审批(10个工作日)
九、报国家局发布审查公告(10个工作日)
高效液相色谱(HPLC)系统适用性试验是指哪些内容?进行该试验的目的是什么?
DMF的全称是Drug Master Files,即药物管理档案。是一份提交给美国FDA的保密文件,是关于产品化学、生产和质量控制信息的一套完整文件资料,内容包括产品的一般信息、生产工艺、杂质研究、稳定性等方面的资料和数据它提供了关于用于生产药物的原料、活性中间体及其设施、流程、包装及仓储等相关的信息。主要的种类有:I型,生产地点和厂房设施、人员(已取消);II型,中间体、原料药和药品;III型,包装物料;IV型,辅料、着色剂、香料、香精及其它添加剂;V型,非临床数据资料和临床数据资料。虽然美国FDA没在正式文件中规定出口到美国的厂家必须上报DMF资料,若该产品被用做处方药时,则美国FDA一定派员对生产厂家进行检查,以确定该厂的生产是否与上报资料所述相符,是否是按美国CGMP(现行GMP)要求进行。美国的DMF文件库是全世界制剂厂家广泛参照的一个供应商资源库,所以几乎所有想让产品推向国际的制药厂都进行DMF备案。DMF注册后有以下几个优势: 1 简化了制剂厂家申请的内容,直接以DMF备案号来代替制剂申请资料中有关单元的具体资料,减少了因向众多制剂客户提供资料而造成企业技术秘密外泄的风险; 2 取得DMF备案号的企业和其产品均会在FDA网站上公示,持有FDA给予的DMF备案号可以吸引更多的制剂客户共建合作发展关系,并在企业的竞争中被制剂客户优先考虑而获得竞争优势;所有归档的DMF被录入FDA的DMF数据库,FDA每季度会更新DMF数据库,公众可以下载查询备案的DMF列表(Excel和ASCII格式)。数据库中的DMF有4中状态:·“A” = Active,表示该DMF未被终止,处于活跃状态;·“I” = Inactive,表示该DMF已被持有者或FDA终止,处于非活跃状态;·“P” = Pending,表示该DMF等待行政审核;·“N” = Number not assigned, 表示该DMF由于撤销等原因未分配编号。DMF备案制其实相当于DMF持有者、用户与FDA间的一种保密协议,当用户需要向FDA递交药品申请(包括IND、NDA、ANDA、其他DMF、出口申请或以上文件的修订和补充),只需在申请中附上DMF持有者的授权书,FDA就可以在评审过程中对涉及的DMF进行考察,这样既实现了DMF中的信息对用户保密,又不影响用户的FDA申请。
土耳其原料药出口注册流程
一、在高效液相色谱法系统适用性试验中,有常用的四个内容:分离度、柱效、重复性和拖尾因子。
1、分离度(resolution,R)——相邻两峰的保留时间之差与平均峰宽的比值。也叫分辨率,表示相邻两峰的分离程度。R≥1.5称为完全分离。
2、柱效:色谱柱是色谱仪最重要的部件(心脏)。柱子内径一般为1~6 mm。常用的标准柱型是内径为4.6 或3.9mm ,长度为15 ~30cm 的直形不锈钢柱。填料颗粒度5 ~10μm ,柱效以理论塔板数计大约 7000 ~10000。减小填料粒度和柱径以提高柱效。
3、拖尾因子(tailing factor,T),用以衡量色谱峰的对称性。也称为对称因子或不对称因子。
二、目的:按各品种项下要求对仪器进行适用性试验,即用规定的对照品对仪器进行试验和调整,应达到规定的要求;或规定分析状态下色谱柱的最小理论板数、分离度和拖尾因子。
扩展资料
高效液相色谱法(High Performance Liquid Chromatography \ HPLC)又称“高压液相色谱”、“高速液相色谱”、“高分离度液相色谱”、“近代柱色谱”等。
LLPC与GPC有相似之处,即分离的顺序取决于K,K大的组分保留值大;但也有不同之处,GPC中,流动相对K影响不大,LLPC流动相对K影响较大。
百度百科-高效液相色谱法
土耳其原料药出口注册流程
原料药是我国医药产业参与国际竞争的优势长板,新冠疫情发生以来,全球医药产业链受到冲击,使得我国原料药产业的战略地位进一步提升。据国家发改委统计,我国几乎可以生产全部品种的原料药,种类高达1500多种,其中60%产量用于出口。截止到2019年,我国原料药共出口到189个国家和地区,主要集中于亚洲、欧洲和北美洲三大市场,国际认证是出口必不可少的一道手续。原料药出口需要递交大量的产品相关资料给当地政府或相关机构获得认证后才能出口,如果不是相同语言的国家出口原料药,所递交的资料和各类说明文件还要进行翻译。原料药认证所需的相关资料对格式要求非常严格,并且专业术语多、难度大。
原料药认证翻译拥有以下资质能更快更好地获得认证:
翻译人员是药学或医学相关专业
熟悉各国的认证流程和相关政策
熟悉认证资料格式和相关术语
国际上常见的三种原料药认证分别为美国的FDA认证、欧洲EDQM认证和日本PMDA认证
FDA认证
美国FDA认证分为五类:I型-生产地点和厂房设施、II型-中间体、原料药和药品、III-型包装物料、IV-型辅料、着色剂、香料、香精及其他添加剂、V-型非临床数据资料和临床数据资料
一般情况下中国厂商的申报认证程序如下:
显示所有大图
EDQA认证
欧洲的CEP 只适用于已有《欧洲药典》( EP) 标准的原料,即 EP 收载的原料药品种。
申请CEP的基本程序包括:
PMDA认证
日本的PMDA认证只能通过日本国内的管理人将MF申请递交给PMDA官方,不能由自己直接递交。
申请MF的基本程序包括:
无论是哪一个国家的申请都离不开CTD文件、GMP检验报告、官方提出的修改意见及问题和补充文件及回复说明。各国文化背景的不同使语言成为了横亘在中间最急需攻克的难题。
国家
修改意见及问题
补充文件及回复说明
美国
483表问题
现场检查及483表的回复说明
欧洲
EDQM提出的修改意见
GMP检查的回复补充说明
日本
PMDA提出的缺陷问题
对PMDA提出的缺陷进行回复
CTD的排版要求
CTD中信息的表达要明确、清楚,申请人不应修改CTD的整体结构,以利于审查内容和快速查找。
纸张大小:欧洲和日本-A4,美国letter纸(8.5X11``)文档和表格应留出余地,以方便在纸张上打印。左手边空白部分应保证装订不受影响
字体:文档和表格的字符大小应足以清楚阅读,建议描述性文档采用Time New Roman,12的字符。
缩写词应在每模块中第一次使用时进行定义。
每页必须有编号页码。
美国DMF文件M1要求
CUVER LETTER(首页)
STATAMENT OF COMMITMENT(声明信)
Administrative Page(行政信息)
US Aent Appointment Letter(美国代理人的指定)
Letter of Authorization(授权信)
Holder Name Transfer Letter(证书持有人转移)
New Holder Acceptance Leeter(新持有人接受函)
REQUEST TO(WITHDRAW,CLOSE) a DMF(DMF的取消与关闭)
Paten satement(专利声明)
欧洲CEP申请文件M1要求
申请表
letter ofAuthorisation(授权信)
declaration in cases where the manufacturer is not the intended holder of a Certificate of Suitability(证书持有人与生产厂商不同的声明信)
letter of declaration of willingness to be inspected(愿意接受检查声明)
letter of declaration of substances of animal/human origin(TSE风险的声明)
letter of commitment to provide samples upon requert by the EDQM(愿意提供样品的声明
模块M2:质量综述
项目
2.3.S.1基本信息
2.3.S.1.1药品名称
2.3.S.1.2结构
2.3.S.1.3理化物质
2.3.S.2生产信息
2.3.S.2.1生产商
2.3.S.2.2生产工艺和过程制作
2.3.S.2.3物料控制
2.3.S.2.4关键步骤和中间体控制
2.3.S.2.5工艺验证和评价
2.3.S.2.6生产工艺的开发
2.3.S.3结构确证
2.3.S.3.1结构和理化性质
2.3.S.3.2杂质
2.3.S.4原料药的控制
2.3.S.4.1质量标准
2.3.S.4.2分析方法
2.3.S.4.3分析方法的验证
2.3.S.4.4批检验报告
2.3.S.4.5质量标准制定依据
2.3.S.5对照品
2.3.S.6包装材料和容器
2.3.S.7稳定性
2.3.S.7.1稳定性总结
2.3.S.7.2上市稳定性承诺和稳定性方案
2.3.S.7.3稳定性数据总结
模块M3: 质量部分
项目
3.1目录
3.2.S原料药
3.2.S.1一般信息
3.2.S.1.1命名
3.2.S.1.2化学结构
3.2.S.1.3一般特性
3.2.S.2生产
3.2.S.2.1生产商
3.2.S.2.2生产工艺和过程控制的描述
3.2.S.2.3物料控制
3.2.S.2.4关键工艺步骤和中间体的控制
3.2.S.2.5工艺验证
3.2.S.2.6生产工艺的改进与变更控制
3.2.S.3结构表征
3.2.S.3.1结构表征和其他特性
3.2.S.3.2杂质
3.2.S.4原料药控制
3.2.S.4.1质量标准
3.2.S.4.2分析方法
3.2.S.4.3分析方法验证
3.2.S.4.4批分析报告
3.2.S.4.5质量标准合理性分析
3.2.S.5对照品
3.2.S.6包装容器和密封方式
3.2.S.7稳定性实验
3.2.S.7.1稳定性实验概述和结论
3.2.S.7.2申请批准后的稳定性实验方案和稳定性保证
3.2.S.7.3稳定性实验结果列表
雅瑞思医学翻译一直专注于医药、医疗器械领域翻译,拥有上百名药学、医学、物理学、生物学、制造学、工程学专职翻译专家。医药翻译部由药理学、毒理学、生药学、药物化学、药物分析学、药剂学、临床医学、临床药理学背景的专业翻译人员组成,都曾在药厂或者大学药学院工作、学习过,对原料药DMF、IND、AND的全套文件翻译极为熟悉,多数成员都具备医学或者药学硕士及以上文凭。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。