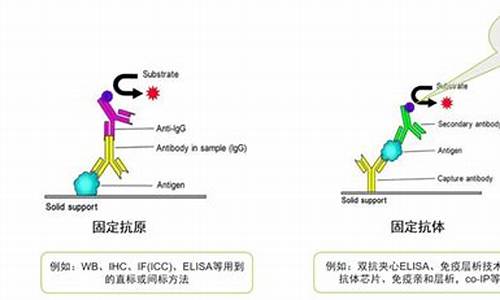
原料药项目申报流程-原料药申报资料审查要点

为使您的产品顺利出口,我们将贸易出口货物的基本流程介绍给您,以使您对产品出口程序做到心中有数、万无一失 。
出口货物流程主要包括:报价、订货、付款方式、备货、包装、通关手续、装船、运输保险、提单、结汇。
一、报价
在国际贸易中一般是由产品的询价、报价作为贸易的开始。其中,对于出口产品的报价主要包括:产品的质量等级、产品的规格型号、产品是否有特殊包装要求、所购产品量的多少、交货期的要求、产品的运输方式、产品的材质等内容。
比较常用的报价有: FOB"船上交货"、CNF"成本加运费"、CIF"成本、保险费加运费"等形式。
二、订货(签约)
贸易双方就报价达成意向后,买方企业正式订货并就一些相关事项与卖方企业进行协商,双方协商认可后,需要签订《购货合同》。在签订《购货合同》过程中,主要对商品名称、规格型号、数量、价格、包装、产地、装运期、付款条件、结算方式、索赔、仲裁等内容进行商谈,并将商谈后达成的协议写入《购货合同》。这标志着出口业务的正式开始。通常情况下,签订购货合同一式两份由双方盖本公司公章生效,双方各保存一份。
三、付款方式
比较常用的国际付款方式有三种,即信用证付款方式、TT付款方式和直接付款方式。1、信用证付款方式
信用证分为光票信用证和跟单信用证两类。跟单信用证是指附有指定单据的信用证,不附任何单据的信用证称光票信用证。简单地说,信用证是保证出口商收回货款的保证文件。请注意,出口货物的装运期限应在信用证的有效期限内进行,信用证交单期限必须不迟于信用证的有效日期内提交。
国际贸易中以信用证为付款方式的居多,信用证的开证日期应当明确、清楚、完整。中国的几家国有商业银行,如中国银行、中国建设银行、中国农业银行、中国工商银行等,都能够对外开立信用证(这几家主要银行的开证手续费都是开证金额的1.5‰)。
2、TT付款方式
TT付款方式是以外汇现金方式结算,由您的客户将款项汇至贵公司指定的外汇银行账号内,可以要求货到后一定期限内汇款。
3、直接付款方式
是指买卖双方直接交货付款。
四、备货
备货在整个贸易流程中,起到举足轻重的重要地位,须按照合同逐一落实。备货的主要核对内容如下:
1、货物品质、规格,应按合同的要求核实。
2、货物数量:保证满足合同或信用证对数量的要求。
3、备货时间:应根据信用证规定,结合船期安排,以利于船货衔接。
五、包装
您可以根据货物的不同,来选择包装形式(如:纸箱、木箱、编织袋等)。不同的包装形式其包装要求也有所不同。
1、一般出口包装标准:根据贸易出口通用的标准进行包装。
2、特殊出口包装标准:根据客户的特殊要求进行出口货物包装。
3、货物的包装和唛头(运输标志):应进行认真检查核实,使之符合信用证的规定。
六、通关手续
通关手续极为烦琐又极其重要,如不能顺利通关则无法完成交易。
1、属法定检验的出口商品须办出口商品检验证书。
目前我国进出口商品检验工作主要有四个环节:
○接受报验:报验是指对外贸易关系人向商检机构报请检验。
○抽样:商检机构接受报验之后,及时派员赴货物堆存地点进行现场检验、鉴定。
○检验:商检机构接受报验之后,认真研究申报的检验项目,确定检验内容。并仔细审核合同(信用证)对品质、规格、包装的规定,弄清检验的依据,确定检验标准、方法。(检验方法有抽样检验,仪器分析检验;物理检验;感官检验;微生物检验等)
○签发证书:在出口方面,凡列入〖种类表〗内的出口商品,经商检机构检验合格后,签发放行单(或在"出口货物报关单"上加盖放行章,以代替放行单)。
2、须由专业持有报关证人员,持箱单、发票、报关委托书、出口结汇核销单、出口货物合同副本、出口商品检验证书等文本去海关办理通关手续。
○箱单是由出口商提供的出口产品装箱明细。
○发票是由出口商提供的出口产品证明。
○报关委托书是没有报关能力的单位或个人委托报关代理行来报关的证明书。
○出口核销单由出口单位到外汇局申领,指有出口能力的单位取得出口退税的一种单据。
○商检证书是经过出入境检验检疫部门或其指定的检验机构检验合格后而得到的,是各种进出口商品检验证书、鉴定证书和其他证明书的统称。是对外贸易有关各方履行契约义务、处理索赔争、议和仲裁、诉讼举证,具有法律依据的有效证件,同时也是海关验放、征收关税和优惠减免关税的必要证明。七、装船
在货物装船过程中,您可以根据货物的多少来决定装船方式,并根据《购货合同》所定的险种来进行投保。可选择:
1、整装集装箱
集装箱(又称货柜)的种类:
(1)按规格尺寸分:目前,国际上通常使用的干货柜(DRYCONTAINER)有:
外尺寸为20英尺X8英尺X8英尺6吋,简称20尺货柜;
40英尺X8英尺X8英尺6吋,简称40尺货柜; 及近年较多使用的40英尺X8英尺X9英尺6吋,简称40尺高柜。
20尺柜:内容积为5.69米X2.13米X2.18米,配货毛重一般为17.5吨,体积为24-26立方米.
40尺柜:内容积为11.8米X2.13米X2.18米,配货毛重一般为22吨,体积为54立方米.
40尺高柜:内容积为11.8米X2.13米X2.72米.配货毛重一般为22吨,体积为68立方米.
45尺高柜:内容积为:13.58米X2.34米X2.71米,配货毛重一般为29吨,体积为86立方米.
20尺开顶柜:内容积为5.89米X2.32米X2.31米,配货毛重20吨,体积31.5立方米.
40尺开顶柜:内容积为12.01米X2.33米X2.15米,配货毛重30.4吨,体积65立方米.
20尺平底货柜:内容积5.85米X2.23米X2.15米,配货毛重23吨,体积28立方米.
40尺平底货柜:内容积12.05米X2.12米X1.96米,配货毛重36吨,体积50立方米.
(2)按制箱材料分:有铝合金集装箱,钢板集装箱,纤维板集装箱,玻璃钢集装箱.
(3)按用途分:有干集装箱;冷冻集装箱(REEFER CONTAINER);挂衣集装箱(DRESS HANGER CONTAINER);开顶集装箱(OPENTOP CONTAINER);框架集装箱(FLAT RACK CONTAINER);罐式集装箱(TANK CONTAINER).
2、拼装集装箱
拼装集装箱,一般按出口货物的体积货重量计算运费。
八、运输保险
通常双方在签定《购货合同》中已事先约定运输保险的相关事项。常见的保险有海洋货物运输保险、陆空邮货运输保险等。其中,海洋运输货物保险条款所承保的险别,分为基本险别和附加险别两类:
(1) 基本险别有平安险(Free from Paricular Average-F.P.A)、水渍险(With Average or With Particular Average-W.A or W.P.A)和一切险(All Risk-A.R.)三种。平安险的责任范围包括:由于海上自然灾害引起的货物全损;货物在装卸和转船过程中的整体灭失;由于共同海损引起的牺牲、分担和救助费用;由于运输船只触礁、搁浅、沉没、碰撞、水灾、爆炸引起的货物全损和部分损失。水渍险是海洋运输保险的基本险之一。按中国人民保险公司的保险条款,其责任范围除了承担平安险所列各项风险外,还承担恶劣气候、雷电、海啸、洪水等自然灾害的风险。一切险的承报保责任范围相当于水渍险和一般附加险的总和。
(2) 附加险别。附加险别有一般附加险和特别附加险两种类型。一般附加险有偷窃提货不着险、淡水雨淋险、抽窃短量险、渗漏险、破损破碎险、钩损险、混杂沾污险、包装破裂险、霉变险、受潮受热险、串味险等。特别附加险有战争险、罢工险等。
九、提单
提单是出口商办理完出口通关手续、海关放行后,由外运公司签出、供进口商提货、结汇所用单据。
所签提单根据信用证所提要求份数签发,一般是三份。出口商留二份,办理退税等业务,一份寄给进口商用来办理提货等手续。
进行海运货物时,进口商必须持正本提单、箱单、发票来提取货物。(须由出口商将正本提单、箱单、发票寄给进口商。)
若是空运货物,则可直接用提单、箱单、发票的传真件来提取货物。
十、结汇
出口货物装出之后,进出口公司即应按照信用证的规定,正确缮制(箱单、发票、提单、出口产地证明、出口结汇)等单据。在信用证规定的交单有效期内,递交银行办理议付结汇手续。
除采用信用证结汇外,其它付款的汇款方式一般有电汇(TELEGRAPHIC TRANSFER(T/T))、票汇(DEMAND DRAFT(D/D))、信汇(MAIL TRANDFER(M/T))等方式,由于电子化的高速发展,现在汇款主要使用电汇方式。(在中国,企业出口享有出口退税优惠政策)
***常用的出口单据和凭证***
(一)汇票(Draft: Bill of Exchange)
它是由一人向另一人签发的要求在见票时或在指定的或可以确定的将来时间向特定的人或其持票人无条件支持一定金额的书面命令。
国际贸易中的货款结算,绝大多数使用跟单汇票(即附有提单等货运单据的汇票)。
在缮制汇票时应注意以下几个问题:
(1)必须列明出标根据,在信用证收付方式下,须说明是根据哪家银行在何日开立的哪一份信用证出具的。
(2)在信用证方式下,应按信用证的规定填写付款人;在托收方式时,付款人的名称一般应为进口方。
(3)信用证方式下的汇票受款人通常应为议付行;托收方式下的受款人应为托收行。
(4)汇票一般开具一式两份,两份具有同等效力,任何一份付讫,另一份自动失效。
(二)提单(Bill of Landing,B/L)
它是由船长或船公司或其代理人签发的、证明已收到特定货物,允诺将货物运至特定目的地, 并交付给收货人的凭证。提单是代表货物所有权的凭证, 因而也是卖方提供的各项单据中最重要的一种, 所以在制作提单时须注意提单的各项内容(如提单的种类、收货人、货物的名称和件数、 目的港、有关收取运费的记载、提单的份数等)一定要与信用证相符。
在我国出口业务中、国外来证通常要求提供"全套清洁已装船作成凭指示和空白背书的提单"。 对此要求,当货物装船时应十分注意,如果大副收据上有"货物受损"或"包装不良"等批注, 凭此换取的提单中,也将均有同样的批注,即成为"不清洁提单",而银行一般都不接受"不清洁提单"。提单一般是一式两份,在托运人要求下,也可签发三份或更多份。份正本提单具有相同效力,但是只要凭其中一份提了货, 其余各份即失效。需要注意的是,倒签提单和预借单中是托运人和承运人串通弄虚作假的行为, 一旦暴露,后果严重。我国出口贸易中应避免这些做法。
(三)保险单(Insurance Policy)和保险凭证(Insruance Certificate)
它们是保险人(即保险公司)与被保险人(即投保人,一般为进出口商)之间订立的保险合同, 当被保险货物遭受保险合同责任范围内的损失时,它们是被保险人索赔、保险人理赔的依据。
保险单(俗称"大保单"),是一种正规的保险合同,它一般包括下列内容:被保险人的名称, 被保险货物的名称、数量或重量、唛头、运输工具的种类和名称,承保险别,起讫地点, 保险期限和保险金额,还列有保险人的责任范围以及保险人与被保险人各自的权利、 义务等方面的详细条款。
保险凭证(俗称"小保单"),是一种简化的保险合同,除对保险人和被保险人的权利、 义务等方面的详细条款不予载明外,其余的内容与保险单相同,并且与保险单有同等的效力。 但在实际业务中,我国保险公司大都签发保险单,较少使用保险凭证。
(四)商业发票(Commercial Invoice)
简称发票。它是出口企业开立的凭此向买方收款的发货价目清单,是供买卖双方凭此发货、 收货、记帐、收付货款和报关纳税的依据。发票并无统一格式,但其内容大致相同, 主要包括:发票编号、开立日期、有关出口合同号码、信用证号码、收货人名称地址、 运输标志以及商品的名称、规格、数量、包装方法、单价、总值和装运地、目的地等。 发票内容必须符合买卖合同规定,在采用信用证付款方式时,则应与信用证的规定严格相符, 绝不能有丝毫差异。另外,发票必须有发货人的正式签字方为有效。
(五)产地证明书(Certificate of Origin)
它是一种证明货物原产地或制造地的证件, 主要用途是提供给进口国海关凭此确定货物的生产国别, 从而核定进口货物应征收的税率,有的国家限制从某些国家或地区进口货物, 也要求以产地证明书来证明货物的来源。产地证明书一般由出口地公证行或工商团体签发。 在我国,它由进出口商品检验局或中国国际贸易促进委员会签发。
(六)检验证书(Certificate of Inspection)
各种检验证书是分别用以证明货物的品质、数量、重量或卫生条件。在我国, 这类证明一般由中国进出口商品检验局出具,如合同或信用证无特别规定, 也可区分不同情况,由进出口公司或生产企业出具, 但应注意证书的名称及所列项目或检验结果,应与合同及信用证规定相同。
(七)包装单(Packing List)和重量单(Weight Memo) 包装单和重量单是商业发票的补充单据。 包装单主要用于工业品,对每件包装内的货物名称、规格、花色等逐一作详细说明, 以便进口地的海关检验和进口商核对。重量单多用于以重量计价的初级产品, 载明每件商品的重量,有的还分别列明每件商品毛重、净重,其作用与包装单相同。
(八)普惠制单据(Generalized System of Preferences,G.S.P.)
普惠制是工业发达国家对来自发展中国家的某些产品, 特别是工业制成品和半制成品给予的一种普遍的关税减免优惠制度。 目前,已有日本、加拿大、澳大利亚、新西兰和欧共体成员国等19个国家给予我国普惠制待遇, 向这些国家出口货物,须提供普惠制单据,作为进口国海关减免关税的依据。
作一个药物项目,哪些途径能帮助立项报告?
1、与药品直接接触的包装材料的生产企业生产这些材料是需要生产许可证。
许可证名称为国家食品药品监督管理局核发的《药包材注册证》
2、
(国产)直接接触药品的包装材料和容器生产审批?
2006年02月20日?发布?
一、项目名称:直接接触药品的包装材料和容器审批?
二、许可内容:(国产)直接接触药品的包装材料和容器生产审批
实施注册管理的药包材产品包括:
1、输液瓶(袋、膜及配件);?
2、安瓿;?
3、药用(注射剂、口服或者外用剂型)瓶(管、盖);?
4、药用胶塞;?
5、药用预灌封注射器;?
6、药用滴眼(鼻、耳)剂瓶(管);?
7、药用硬片(膜);?
8、药用铝箔;?
9、药用软膏管(盒);?
10、药用喷(气)雾剂泵(阀门、罐、筒);?
11、药用干燥剂。?
三、设定和实施许可的法律依据:
《中华人民共和国药品管理法》第五十二条、《中华人民共和国药品管理法实施条例》第四十四条、《直接接触药品的包装材料和容器管理办法》
四、收费:不收费
五、数量限制:本许可事项无数量限制
六、申请人提交材料目录:
《药包材注册申请表》
资料编号(四)申请企业营业执照;
资料编号(五)申报产品生产、销售、应用情况综述;
资料编号(六)申报产品的配方;
资料编号(七)申报产品的生产工艺及主要生产、检验设备说明;
资料编号(八)申报产品的质量标准;
资料编号(九)三批申报产品的生产企业自检报告书;
资料编号(十)与采用申报产品包装的药品同时进行的稳定性试验(药物相容性试验)研究资料;
资料编号(十一)申报产品生产厂区及洁净室(区)平面图;
资料编号(十二)申报产品生产企业环境保护、废气废水排放、安全消防等符合国家有关法律规定,所取得的有关合格证明。
以上申报材料具体要求详见《直接接触药品的包装材料和容器管理办法》附件二。
七、对申请资料的要求:
(一)申报资料的一般要求:
1、申报资料按《直接接触药品的包装材料和容器管理办法》(国家食品药品监督管理局令第13号)附件二规定的资料顺序编号,按编号分别装订,申报资料首页为申报资料目录。
2、申报资料应使用A4纸打印,内容完整、清楚,不得涂改。
3、资料封面应包含以下信息:药包材名称、资料项目编号、项目名称、申请机构联系人姓名、电话、地址,试验资料完成机构名称、主要完成人、参加人、电话、原始资料保存地点。并须加盖各机构公章。
4、资料按套装入档案袋,档案袋封面注明:申请分类、注册分类、药品名称、本袋所属第X套第X袋每套共X袋、原件/复印件、申请机构、联系人、电话。
5、注册申请报送2套完整申请资料(其中至少1套为原件)和1套综述资料(可为复印件),各袋均应包含1份申请表。
6、《药包材注册申请表》:从国家食品药品监督管理局网站(www.sfda.gov.cn)下载,按要求填写后打印并保存,用于提交的申请表电子文件与书面申请表的数据核对码必须一致,并一并提交。
(二)申报资料的具体要求:
1、《药包材注册申请表》
(1)《药包材注册申请表》是受理审查的重要文件之一,各项均应当填写,不得缺项、漏项,如果某一项无填写内容,应当填写“无”。
(2)产品名称项目应当与申报品种的质量标准中的名称一致。需要注意以下几点:
①没有颁布国家标准的产品应当尽量参照已颁布的相关药包材国家标准的命名原则对产品进行命名。
②对于复合膜(袋)产品,如果申报单位无制“袋”生产条件,则产品名称项目填写为“XXX复合膜”,?如果申报单位有制“袋”生产条件,并同时申请“膜”、“袋”注册,则产品名称项目填写为“XXX复合膜、袋”。
丁基胶塞类产品应当在名称中明确其具体卤化种类,如应当填写为“注射液用氯化丁基橡胶塞”而不要笼统的填写为“注射液用卤化丁基橡胶塞”。
(3)英文名项目:进口申请需要填写,生产申请不需要填写。
(4)规格项目应当填写申报品种的物理尺寸。需要注意的是:
药品包装用复合膜、多层共挤输液用膜(袋)等产品用产品的不同复合材质表示其规格,如复合膜产品分为PET/PE、PET/AL/PE等,且不同规格视为不同品种应当分别申报。
(5)配件名称项目:
①输液瓶和输液袋产品如果同时申报组合盖、接口、胶塞等配件应当在此处填写申报注册的配件名称。如果不申报此类配件,则在此处填写“无”,不得空白。
②预灌封注射器产品应当在此处填写各部分组件的名称。
③其余品种可不必填写此项。
(6)配方项目:
①应当写明申报产品的原材料及添加剂(着色剂、防腐剂、增塑剂、遮光剂及油墨等)的名称,注意与申报资料中的配方一致,无需填写用量。
②申报配件的产品,还应当按照上述(1)的要求,分别写明各配件的配方。
(7)质量标准项目应当填写质量标准的名称与编号。如果同时申报上文5中所列配件,还应当填写配件质量标准情况。
(8)申请人项目:
生产企业名称项目应当填写法人机构的名称,并与所附的证明性文件一致。
注册地址项目应当与企业法人营业执照中的注册地址一致。
生产地址项目指申报产品的实际生产地址。
对于生产单位为不具备法人资格的分支机构的,可以按照以下方式办理:应当填写法人机构的注册地址,生产地址填写实际生产单位(不具备法人资格的分支机构)的名称和地址。分别由法人机构和分支机构加盖公章并由法人签字。另外,在证明性文件中应当提供法人机构的《企业法人营业执照》、法人机构出具的《特别授权与保证》原件(见附件1)及分支机构与法人机构的关系证明。
电话、传真项目应当填写能直接找到联系人的号码,并且应当填写区号。
(9)“各申请机构名称、公章、法定代表人签字、签字日期”及“进口申报品种注册代理机构名称、公章、法定代表人签字、签字日期”项目:
应当确保申请机构的名称、公章、法定代表人签字、日期等项目填写完整。法定代表人不能签名时,可由法定代表人授权的负责人签名,并同时提供委托签字授权书原件。
(10)申请表应当经省局经办人审查,并确保经办人签字、日期,填写完整。
2、申报资料
(1)申报产品的配方资料。
①应当明确说明原料及添加剂(着色剂、防腐剂、增塑剂、遮光剂及油墨等)的化学名称、质量标准、来源、在配方中的作用、用量以及用量比例(以重量计算)。对于添加剂,还应当提供安全用量范围的使用依据。
②其中,输液袋用膜材、药品包装用复合膜(硬片及软膏管)等产品,配方中应当说明产品由几层材料组成及每层材料的名称。
③输液袋用膜材还必须明确说明每层材料原料及添加剂的化学名称、质量标准、来源、在配方中的作用、用量以及用量比例(以重量计算)。
④如果生产复合膜产品的单层膜是外购的,只需要提供外购膜材的来源和质量标准。
⑤如果同时申报不同复合材质的输液袋用膜材、药品包装用复合膜(硬片、铝箔及软膏管),应当视为不同品种分别提供配方资料。
⑥药用塑料瓶的瓶盖和瓶身应当按照上述规定分列配方。
⑦输液瓶和输液袋品种无论是否同时申报组合盖、接口、胶塞等配件,均应当提供组合盖、接口、胶塞的来源及质量标准等资料。若同时申报组合盖、接口、胶塞等配件,应当分列各配件的配方。
(5)申报产品生产、销售、应用情况综述资料。
应当同时说明产品的用途及用法。
(6)申报产品的生产工艺及主要生产、检验设备资料。
①生产工艺资料应当包括工艺流程图、起始原料、有机溶媒、生产条件(温度、压力、时间、催化剂等)和操作步骤,以及原料、产物的主要理化性质,并注明生产工艺过程中可能产生的杂质或者其他中间产物。
塑料输液瓶产品应当说明封口方式,并提供清洗工艺和密封性的验证资料。
②生产、检验设备资料可以按照下述表格形式提交
药包材生产设备一览表
序号 设备名称 ?型号 ?数量 ? 生产厂
药包材检验设备一览表
序号 设备名称 ?型号 ?数量 ? 生产厂
(7)申报产品的质量标准
①执行国家食品药品监督管理局颁布的YBB系列标准的品种,应当提供所执行标准的复印件。
②执行自拟标准的品种,应当提供标准草案及起草说明,并且其格式应当符合国家食品药品监督管理局YBB系列标准的格式,并使用其术语和计量单位。
③应当附产品结构图。
④同时申报配件的应当提交配件的质量标准。
(8)三批申报产品生产企业自检报告书。
应当提供连续3批样品的自检报告书。如果有委托外单位检验的项目应当予以说明。此项资料需提交原件。
(9)采用申报产品包装的药品同时进行的稳定性试验(药物相容性试验)研究资料
①模拟上市包装进行试验,注意选择有代表性的试验药品,试验药品的稳定性考察项目应当参照《中国药典》2000年版附录XIX?C《原料药及药物制剂稳定性重点考察项目表》所列相应剂型的项目设置。设置的项目不得缺少含量、有关物质、水分、粒度检测等重要项目,不得随意减少或者改变项目。
②应当附试验药品的质量标准。
③药品批号及药包材的名称、规格、批号均不得缺少。(几批包材几批药品)
④应当提供6个月加速试验或者12个月长期试验结果。
⑤试验结果中,能够给出具体数值的项目应当用数字表示,不得以“符合规定”等字样代替。加速试验和长期试验的取样点应当与《中国药典》2000年版二部附录XIX?C相符。
⑥推荐的加速试验条件
⑦应当说明试验样品的摆放位置,如直立、倒置或者横置等。胶塞类产品应当倒置进行试验。
⑧此项资料需提交原件。
八、申办流程示意图:
九、许可程序:
(一)受理:
申请人向省局受理部门提出申请,按照本《须知》第六条所列目录提交申请材料,工作人员按照《直接接触药品的包装材料和容器管理办法》附件2:药包材生产申请资料要求对申请材料进行形式审查。申请事项依法不需要取得行政许可的,应当即时告知申请人不受理;申请事项依法不属于本行政机关职权范围的,应当即时作出不予受理的决定,并告知申请人向有关行政机关申请;申请材料存在可以当场更正的错误的,应当允许申请人当场更正;申请材料不齐全或者不符合法定形式的,应当当场或者在五日内一次告知申请人需要补正的全部内容,逾期不告知的,自收到申请材料之日起即为受理;申请事项属于本行政机关职权范围,申请材料齐全、符合法定形式,或者申请人按照本行政机关的要求提交全部补正申请材料的,应当受理行政许可申请。
(二)现场考察:
省级食品药品监督管理局完成审查后,30日内对生产企业组织现场检查,抽取连续3批样品,通知药包材检验机构进行注册检验。
(三)检验:
药包材检验机构在收到注册检验通知单和样品后在30日内对样品进行检验,出具检验报告并提出意见,报省级食品药品监督管理局并通知申请人.(新药包材的注册检验在60日内完成)
(四)资料移送:
省级食品药品监督管理局在收到药包材检验机构的检验报告书和有关意见后10日内将形式审查意见,现场检查意见和检验报告书,其他意见及申请人报送的资料和样品报送国家食品药品监督管理局.
(五)技术审评:
国家食品药品监督管理局收到资料后,在80日内组织完成技术审评.(需要补充资料的,国家食品药品监督管理局一次性告知申请人,申请人在4个月内一次性补齐)
(六)行政许可决定:
国家食品药品监督管理局应当在完成技术审评后20日内完成审批。以《药包材注册证》形式,决定是否同意;不同意的决定应当说明理由,发给《审批意见通知件》;如需要换发《药包材注册证》或者《进口药包材注册证》的,换发新证后,原证予以公告注销。(注:国家食品药品监督管理局在完成技术审评后20日内完成审批,20日内不能完成审批的,经主管局领导批准,可以延长10日;时限延长超过10日的,须报批准。
(七)送达:
自行政许可决定之日起10日内,SFDA行政受理服务中心将行政许可决定送达申请人。
(八)复审:
申请人对不予批准决定有异议的,可以在收到审批决定后10日内向国家食品药品监督管理局提出复审。复审的内容仅限于原申请事项、原报送的资料和样品。
接到复审申请后,国家食品药品监督管理局应当在50日内作出复审决定。决定撤销原不予批准决定的,应当发给相应的药包材批准证明文件;决定维持原决定的,国家食品药品监督管理局不再受理再次的复审申请。
十、承诺时限:
自受理之日起170/200(新药包材)日内作出行政许可决定。但不包括申请人补充资料所需的时间。(注:国家食品药品监督管理局在完成技术审评后20日内完成审批,20日内不能完成审批的,经主管局领导批准,可以延长10日;时限延长超过10日的,须报批准。)
十一、实施机关:
实施机关:省级食品药品监督管理局
受理地点:各省级食品药品监督管理部门
十二、许可证件有效期与延续:
国家食品药品监督管理局核发的《药包材注册证》或者《进口药包材注册证》的有效期为5年。有效期届满需要继续生产或者进口的,申请人应当在有效期届满前6个月申请再注册。
药包材补充申请批件与《药包材注册证》有效期相同。
十三、许可年审或年检:无
十四、受理咨询与投诉机构:
咨询:国家食品药品监督管理局
投诉:国家食品药品监督管理局驻局监察局、政策法规司执法监督处
注:本须知工作期限以工作日计算,不含法定节假日
药品注册上市申报时提交完善的药品生产工艺资料至少是
可利用数据库帮助药物立项,无论是调研药物基本信息、国外获批上市情况、国内注册申报情况、市场准入信息,还是国内外市场销售、临床价值、竞品比较、专利分析等都能查询。
1、列如查询药物基本信息(药物产品规格、剂型、原研企业、注册类别、适应症以及作用机制用法用量和不良反应)、国内注册申报情况(按新注册分类申报/一致性评价申报企业、临床试验登记情况、药品审批进度、临床获批情况数量等)
以上这些可以在全球药物研发数据库、药品审评数据库、药物临床数据库等查询相应的数据帮助药企在立项提供决策分析。
药物立项基本信息调研
2、国内外获批上市情况(了解同剂型/不同剂型获批情况、不同规格、同剂型、同靶点等等、原料药登记备案信息、全球首次获批信息)。
以上信息可以在“全球上市药品数据库”中查询了解各个国家上市药品信息,主要时对比中、美、日、欧的上市药品信息,为药物立项调研提供上市药品数据支持。
药品上市数据
原料药数据库包含原料药登记信息,可供查询原料药数据信息。
原料药信息
3、调研市场准入信息(是否医保品种、集采品种、药品中标价(最高、最低、平均))这些数据在合理用药下的医保目录数据库中查询,市场信息下的国家药品集中采购、药品招投标数据中查询获取相关药品数据,分析医药市场,调研研发品种市场的竞争力。
医药中标、集采
医保目录
4、国内外医药市场销售数据分析(近五年全球或者国内药品销售情况分析),使用药品销售下的(医院、样本医院、药店、全球药物销售数据等)查询分析药品销售数据,包含了单个品种销售数据的可视化分析、活性成分销售数据可视化分析、某个用药领域销售数据的可视化分析、药企销售数据的可视化分析,利用这些销售数据能帮助药企的立项部门筛选分析药品品种,市场部和销售部通过销售数据能及时调整销售策略,创造更高销售额度,主要是计算投入产出比。
国内外药品销售市场
5、临床价值(治疗领域概况、临床试验方案、国内外指南推荐情况)、竞品比较(临床价值/治疗地位比较、市场表现比较),以上可以通过临床试验数据库,临床诊疗指南数据库等等,分析临床价值,竞品的分析也能通过数据库的数据实现。
6、专利信息(障碍专利、专利到期时间、同族专利等),利用全球专利数据库、中国专利数据库查询专利信息,了解药品的专利情况,避免侵权,也能在专利信息中可以查询相关的工艺参数等。
药品专利信息调研方式
除了以上这些还要考虑自己企业研发、生产、营销的匹配性,以及研发投入、生产投入分析,研发药物,药企主要是为了挣钱,投入分析、生产分析一定要认真对待。
医药原料药申报中易出现的几点问题
三点要求。
1、药品处方、生产工艺、药品标准是指该品种现行的处方、工艺及质量标准。如与取得药品批准证明文件时相比有变化的,须按批准时间列出历次变更项目及内容,并提供补充申请批件。药品处方包括活性成分或中药药味、辅料的种类和数量。现行生产工艺包括完整的生产流程、每个单元操作、单元操作的主要工艺控制参数及主要质量控制参数等。药品标准需提交复印件,现行版本药典标准可不提供。
2、同时提交药品处方、生产工艺与国家药品监督管理局审批一致的真实性承诺书,承诺书必须有法人代表亲笔签名并加盖公章。
3、应当提供经核准的生产药品制剂所用化学原料药、中药材和中药饮片、中药提取物、制剂中间体等的来源,其中按照药品管理的,应提供药品批准证明文件。变更或增加原料药来源的,应当提供批准证明文件或备案情况公示内容。
原料药的质量是药品质量的基础,其质量不能仅依靠最终的质量标准来控制和保证,还必须对整个制备过程加以控制。结合目前原料药的审报情况,分析整理出以下问题,提请申报者关注:(一)合成工艺 1、缺乏对合成用起始原料、关键原料的合理控制。起始原料内控标准的制订不仅仅是研究资料完整性的一个方面,更重要的是有利于申报单位加强对原料药合成的 起点控制,最大限度地降低可能引入的杂质,保证终产品的纯度。审评中发现申报资料部分研究单位往往忽视制订起始原料的内控标准,或者即使制定,也不是结合 起始原料的工艺设定合理的质控项目(比如未结合工艺,制定相应的杂质控制以及残留溶剂控制)。2、缺少反应终点的监测方法与中间体质控方法。对于反应终点的监测以及中间体的控制,是构成产品质量控制体系的一部分重要内容。建议研发者尽量采用TLC等方法监测反应进程,对关键中间体应建立HPLC法等定量分析方法进行质控,以保证工艺与质量的稳。尤其需要强调的是目前手性原料的合成中,对引入手性的原料、中间体的控制过于粗略。研究单位多采用比旋度的方法对手性原料药合成中的关键原料及中间体进行 光学活性控制,但比旋度对光学纯度的质控而言,是个较为粗略的指标,其数值受样品的化学纯度、水分等的影响而会产生较大的波动,无法较准确体现样品的光学 纯度。同时,由于手物尤其是多个手性中心的药物空间结构确证以及质量控制仅依靠终点控制有一定难度,通常尚需结合起始材料以及中间体的情况进行判断, 故建议此类药物合成中采用手性HPLC法、毛细管电泳等更具专属性的方法控制相关样品的光学纯度。(二)、结构确证 1、结构确证中的对照品问题:结构确证不一定都要使用对照品,在没有对照品时,只需根据结构确证的一般原则:在全面分析化合物结构特征的基础上,结合制备 工艺、文献数据等已有的研究信息,选择针对性强的分析方法来确证化合物的结构。如果选用对照品,则需关注对照品选择的合理性:如以自研产品精制后样品作为 对照品,对结构确证而言,无专属性及特异性意义,因此并不适宜作为结构确证时的对照品;以上市制剂中提取、精制的原料为对照品,可作为部分结构确证时使 用,但由于提取、精制用溶剂及方法的差异,此类对照品与样品有可能存在晶型等方面的差异,故不适宜作为DSC、TG、粉末X-射线衍射等测定时的对照品。2、对口服固体制剂所用的难溶性原料药,缺少对样品晶型的研究晶型不同,可能会影响到产品的稳定性以及溶解性(最终影响生物利用度),为减少临床研究 的风险,建议对难溶物加强晶型研究。可采用不同的精制方法获取具有潜在晶型差异的样品,并对这些样品进行IR或粉末X-射线衍射测定以确定样品是否具 有多晶型,对具有多晶型的样品尽可能选择成熟路线制备晶型热力学稳定的样品作为制剂的原料,同时应兼顾不同晶型样品的溶解度。(三)质量研究与质量标准 该部分研究是存在问题最多的部分,最突出的是有关物质、残留溶剂方法建立的合理性、可操作性及质量可控性。1、有关物质检查:有关物质检查,包括对产品中残留合成原料、中间体、副产物及可能的降解产物的检查,是控制药品质量的重要指标,同时也是药品稳定性评价中需重点考察的项目。其方法学研究需关注以下几个项目:(1)有关物质检查波长的选择:当采用HPLC法,检测器为紫外检测器时,检测波长选择是否合理直接影响到杂质种类、数量的检出,因此检测波长的选择是 方法学研究的重要内容。审评中常见的问题包括: 直接或间接地以主成分的最大吸收波长作为检测波长,由于有关物质检查的对象是杂质,若将主药的最大吸收波长确定为检测波长,则杂质在此波长下的吸收可能偏 低,某些杂质甚至无吸收,这样会造成对杂质含量的低估甚至漏检,从而不能反映产品的真实质量。以样品进行破坏性试验(酸、碱、热、光照、氧化等)后的溶液 做紫外扫描,将扫描图谱中最大吸收波长确定为有关物质的检测波长。因破坏性试验后溶液中存在尚未破坏的主药、降解产物、辅料等,此溶液的紫外吸收为各成分 紫外吸收的加和,并不能反映降解产物的紫外吸收特性。由于未破坏主药所占比例较大,故破坏性试验后溶液的最大吸收波长一般仍为主药的最大吸收波长。因此在有关物质检查的波长选择时,首推通过二极管阵列检测器考察合成用原料、各中间体、各降解产物、主药的紫外吸收特征,或至少通过紫外扫描的方法考 证上述各样品的紫外吸收特征,选择杂质与原料相近的响应值处的波长为有关物质检查波长。对于响应值相差较大的杂质,应建立相应的检查方法及检测波长,或采 用加校正因子的自身对照法。(2)流动相筛选及方法学验证:从目前原料药的审报情况来看,在流动相筛选及方法学验证中,采用强力破坏以获得各种降解产物,并考查各降解产物与主药的分 离度的方法已被申报单位接受并认同,易被申报单位忽视的是对合成用原料、中间体与主药间分离度的考证。而对于原料药而言,这恰恰是原料药流动相筛选及考证 的重点,尤其是对于已有国家标准的原料药,验证国家标准终收载的有关物质检查方法是否适合自研产品的检验,由于合成工艺的可能不同,需重点验证合成用起始 原料、中间体同主药的分离情况。2、残留溶剂:原料药中的残留溶剂系指在原料药生产中使用,但在工艺过程中未能完全去除的有机溶剂。申报情况反映对于残留溶剂的检查可能存在以下问题:(1)研究内容不全面:未进行或只进行部分残留溶剂的检测,原料药中残留的有机溶剂特别是二类以上溶剂可能会对药物的安全性产生重大影响,其研究的重要性 不言而喻,由于历史原因,部分国家标准未制定有机溶剂检查项,但随着药检技术的发展和对残留溶剂认识的提高,残留溶剂研究成为必要的研究项目,需根据考察 结果(尤其是大生产样品的检验结果)确定是否应将该项检查定入质量标准。对制剂过程中使用的有机溶剂也建议考察其残留情况,特别是脂质体、缓、控释微丸包 衣过程使用的有机溶剂更应引起注意。一般情况下一类溶剂应禁止使用,如要使用,必须首先进行替代试验,证明在合成工艺中无法用其他溶剂替代。一类不论是在 起先还是后续的反应中使用,均应在产品中检测控制。(2)方法学研究不完整:采用GC顶空法进行测定时,研究过程中往往忽视两个非常重要的参数:顶空的平衡温度和平衡时间。平衡温度影响分配系数,并与平衡 时间相关,略高的平衡温度可以缩短平衡时间。平衡时间本质上取决于被测组分分子从样品基质到气相的扩散速度,由于样品的性质千差万别,因此平衡时间难以预 测,需通过一定平衡温度下的试验确定,以保证样品中有机溶剂的充分释出。通过研究确定合理的平衡温度与平衡时间保是保证顶空法测定残留溶剂结果可靠性的重 要前提。(3)检测器选择不当:气相的检测器用于残留溶剂的测定时最常用的是火焰离子化检测器(FID)、热导检测器(TCD)、电子捕获检测器(ECD)。申报 资料中存在的主要问题是忽视研究对象的结构特征,不加研究及选择地使用某一种检测器,如被研究对象是三氯甲烷、四氯化碳等仅含一个活泼氢或不含活泼氢的化 合物,却采用了FID检测器,导致测定结果的不可靠。(四)稳定性考察1、考察项目设置不合理:稳定性研究的考察项目应选择在药品保存期间易于变化,并可能会影响到药品的质量、安全性和有效性的项目,以便客观、全面地反映药 品的稳定性。根据药品特点和质量控制的要求,尽量选取能灵敏反映药品稳定性的指标。目前申报情况反映,有些申报单位易忽视产品的特点,仅以常规或专属性较 差的考察项目代替样品个性的考察,如对手物不考察光学异构体的变化或仅以比旋度进行粗略考察,对于易吸湿的药物不进行水分或干燥失重检查,无法全面、 真实反映样品的稳定性。2、稳定性研究中采用的方法与质量标准的方法不一致。质量标准中的方法是研究者在研发中,经过比较,认为相对合理的、可控制产品质量的方法,因此,两部分 研究中方法应尽量保持一致,以加强对结果的判断。如产品在研发过程中,质控方法进行了修订,需要分析方法变更前后对检验结果的影响。徐州宏鑫医药化工有限公司位于风景秀丽的徐州工业园区,园区地理位置优越,交通便利。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。